
monomers-Платэ-книга
.pdf
561
Полиуретанацетали получают взаимодействием уретангликолей с эфирами гликолей в присутствии кислых катализаторов. Введение уретановых групп способствует улучшению адгезионных свойств полимеров. Линейные полиуретанацетали имеют разрушающее напряжение при растяжении 2,0-2,5 МПа и относительное удлинение при разрыве 700-900%. Их применяют в качестве полимерных пластификаторов, эластифицирующих добавок, компонентов клеевых композиций для склеивания полиэтилентерефталата, полиэтилена, поливинилхлорида, дерева и других материалов.
Гликолькарбаматы являются исходными продуктами и при получении полиуретанов путем элиминирования гликоля нагреванием в присутствии оксида бария или бората цинка:
|
|
|
|
|
|
t0 |
|
|
||
HOCH2CH2 |
|
|
|
OCNH(CH2)6NHCOCH2CH2OH → |
HO—(CH2)2—OH + |
|||||
|
|
|||||||||
O |
O |
Кат. |
|
|
||||||
|
|
|
|
|
|
O |
O |
|||
|
|
|
|
|
|
+ —OCH2CH2 |
|
|
|
|
|
|
|
|
|
|
OCNH(CH2)6NHC—n |
||||
Более перспективным для создания композиционных материалов является получение полиуретанов по реакции циклокарбонатов с циклическими алкилениминами:
R—CH—CH2 + HN |
|
|
CH2 |
HO—CH—CH2—O—C—N |
|
CH2 |
|||||||||||
|
|
||||||||||||||||
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O O |
CH2 |
R |
|
O CH2 |
|||||||||||||
|
C |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|||
|
|
|
|
HOCHCH2[OCNH(CH2)2OCHCH2]nOCN |
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R |
|
|
O |
|
R |
|
O |
|
|
CH2 |
|||
|
|
|
|
|
|
|
R |
|
|
||||||||
Линейные полимеры, получаемые при температуре ниже 373 К, растворимы в воде и в ряде органических растворителей. Термообработкой при 373-423 К они

562
могут быть переведены в сшитые полимеры. Это позволяет применять их в качестве компонентов клеев, красок, связующих для стеклопластиков и т.п.
Довольно широкое распространение получили материалы на основе виниленкарбоната. Обработкой виниленкарбоната аммиаком получают синтетические уретановые олигомеры, используемые в качестве модификаторов каучуков:
CH—O |
|
Кат |
O |
O |
||||
|
|
|
|
|
|
|
||
n |
C=O + nNH3 |
nHC—CH2—O—C—NH2 |
||||||
CH—O
O O OH O
 HC—CH2—[O—C—NH—CH—CH2]n-1—O—C—NH2
HC—CH2—[O—C—NH—CH—CH2]n-1—O—C—NH2
Виниленкарбонат полимеризуется и сополимеризуется с другими виниловыми мономерами в присутствии пероксидов. В дальнейшем их или гидролизуют водными растворами щелочей, получая гидроксилсодержащие водорастворимые полимеры, либо обрабатывают гидроксиалкиламинами и получают линейные полигидроксиуретаны, способные к дальнейшему структурированию под воздействием температуры с образованием высокопрочных и в то же время эластичных материалов. Их применяют для получения эластичных пленок и покрытий.
Полимеры с распределенными по цепи макромолекулы циклокарбонатными группами можно синтезировать полимеризацией карбонатсодержащих эфиров акриловой и метакриловых кислот:
CH2=C—CO—(CH2)n—CH—CH2
R O O O
C=O
Получаемые линейные полимеры при нагревании могут сшиваться с полифункциональными соединениями - алифатическими полиаминами, гликолями, органическими дикислотами, образуя достаточно прочные, прозрачные и окрашенные покрытия, адгезивы.
Способность циклокарбонатов взаимодействовать с незамещенной амидной группой использована при оксиэтилировании поликапроамида этиленкарбонатом, а их способность взаимодействовать с карбоксилсодержащими соединениями применяется при синтезе линейных полиэфиров:

563
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
473-523 К |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
HOOC |
|
|
|
|
|
|
|
COOH + 2CH2—CH2 |
|
- CO2 |
|
|
HO(CH2)2O |
|
С |
|
|
|
|
|
|
|
|
С |
|
O(CH2)2OH |
||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
O |
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C=O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
HO(CH |
) O |
|
С |
|
|
|
|
|
|
|
|
|
С |
|
|
O(CH |
) |
|
OH |
523-573 К |
|
|
|
|
|
||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||
2 |
2 |
|
|
|
|
|
|
|
|
|
|
|
|
2 |
2 |
|
|
|
|
|
|
Кат |
|
|
|
|
|
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
O |
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
HO(CH ) |
O |
|
[C |
|
|
|
|
|
|
|
|
|
|
C |
|
|
O(CH2)2O-]n H |
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
2 2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
+ (n-1)HO(CH2)2OH.
При этом продолжительность процесса сокращается в 10 раз по сравнению с обычно применяемыми методами.
Соединения, содержащие в структуре циклокарбонатную группу
CH3—(CH2)7—CH—CH—(CH2)7—R, O O
C=O
O O X где R = —C N, —C—O—X, —C—N 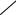 , Y
, Y
используют в качестве пластификаторов галогенсодержащих полимеров. Такой пластификатор не мигрирует к поверхности и придает материалу высокую эластичность, сохраняющуюся при низкой температуре; он не вымывается и не экстрагируется водой и растворителями.
Интенсивные исследования циклокарбонатов, способов их получения и областей применения начались в 50-х годах ХХ столетия. Эти исследования развивались в основном в направлении синтеза алкиленкарбонатов (этиленкарбонат, пропиленкарбонат и т.п.), которые являлись эффективными растворителями некоторых высокомолекулярных соединений при приготовлении прядильных раство-

564
ров. Благодаря способности вступать в реакции присоединения, замещения, полимеризации и конденсации они нашли широкое применение в промышленности органического синтеза для получения гликольуретанов, оксазолидонов, изоцианатов, виниленкарбоната и ряда оксиалкилированных соединений.
14.5.1. Получение циклокарбонатов на основе -оксидов
Впервые реакцию взаимодействия -оксидов с диоксидом углерода осуществил Фирлинг, применив в качестве катализатора едкий натр, нанесенный на активированный уголь:
|
RСН—О |
||
СН2—СН—R + СО2 |
|
|
С=О |
О |
|
|
СН2—О |
|
|||
Выход алкиленкарбоната по этому способу составил всего 30-40%. Принципиальная возможность получения циклокарбонатов из -оксидов и диоксида углерода стимулировали развитие дальнейших работ в этом направлении. Для осуществления процесса карбонилирования были использованы в качестве катализаторов галогениды щелочных и щелочноземельных металлов, третичные амины, галогениды тетраалкиламмония, соль тетраалкилфосфония и триалкилсульфония, азотсодержащие соединения в сочетании с реактивом Гриньяра, ионообменные смолы, содержащие четвертичные аммониевые соединения. Вопреки ожиданию, третичные амины практически не катализируют эту реакцию.
Процесс получения циклокарбонатов проводят, как правило, при 353-473 К и 1-20 МПа. Столь высокое давление обусловлено, очевидно, использованием - оксидов с низкой температурой кипения.
Изучение кинетики и механизма каталитического взаимодействия -оксидов с диоксидом углерода показало, что в апротонных растворителях реакция имеет первый порядок по оксиду и катализатору и нулевой по диоксиду углерода, т.е. скорость реакции не зависит от давления СО2. На основании кинетических исследований предложен следующий механизм реакции:
(CnH2n+1)4NBr  (CnH2n+1)4N+ + Br-
(CnH2n+1)4N+ + Br-
CH2—CH2 + Br- Br—CH2—CH2—O- O
Br—CH2—CH2—O- O
nBr—CH2—CH2—O- (—CH2—CH2—O—)n + nBr-
(—CH2—CH2—O—)n + nBr-

565
Br—CH2—CH2—O- + CO2 Br—CH2—CH2—O—C—O-
Br—CH2—CH2—O—C—O-
O
CH2—O
Br—CH2—CH2—O—C—O- |
C=O + Br- |
O CH2—O
Лимитирующей (самой медленной) стадией, определяющей скорость реакции в целом, является стадия образование галогеналкокси-иона, что и объясняет нулевой порядок по диоксиду углерода.
Исследование механизма каталитической реакции соединениями сурьмы методами ИК- и ЯМР-спектроскопии не обнаружило изменений в смеси катализатора и эпоксида, что указывает на отсутствие координирования эпоксидов по отношению к катализатору, как это наблюдается в случае применения тетраалкиламмонийгалогенидов. Механизм, предполагающий активацию СО2 органическими соединениями сурьмы (Ph4SbBr, Ph3SbBr2), можно представить следующим образом:
|
[CO2]активир CH -CH-H |
|||
|
|
2 |
|
|
|
|
R O |
|
|
|
Sb |
CH-O |
C=O |
|
CO2 |
CH2-O |
|||
|
||||
Следует отметить, что при применении в процессах конденсации эпоксидов и СО2 в качестве катализаторов ряда металлорганических соединений получаются линейные поликарбонаты.
14.5.2. Получение циклокарбонатов на основе хлоргидриновых эфиров
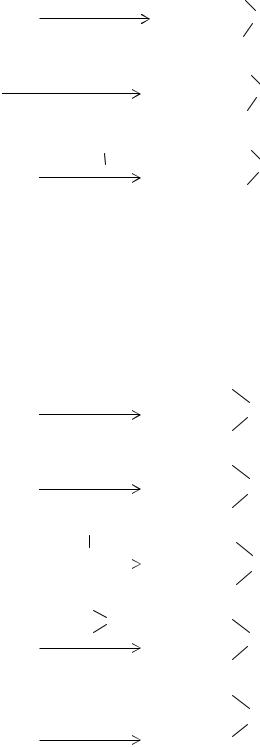
Циклокарбонаты могут быть получены на основе хлоргидриновых эфиров, которые являются промежуточными продуктами синтеза эпоксидных олигомеров конденсацией эпихлоргидрина с гидроксилсодержащими соединениями - фенолами, спиртами, карбоновыми кислотами. Циклокарбонаты получают обработкой хлоргидриновых эфиров карбонатами, гидрокарбонатами или алкиленкарбонатами щелочных металлов:
566
|
|
Na2CO3 |
CH2—O |
||||
|
|
|
|
C=O + NaCl + NaOH |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
R—CH—O |
||
CH2—Cl |
NaHCO3 |
CH2—O |
|||||
|
|
|
|
|
|||
R—CH—OH |
|
|
C=O + NaCl + H2O |
||||
|
|
|
|
|
|||
|
|
|
|
|
R—CH—O |
||
|
|
CH3-O-C-O-Na |
|
CH2—O |
|||
|
|
O |
|
|
|
|
C=O + NaCl + CH3OH |
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
R—CH—O |
||
14.5.3. Получение циклокарбонатов на основе диолов
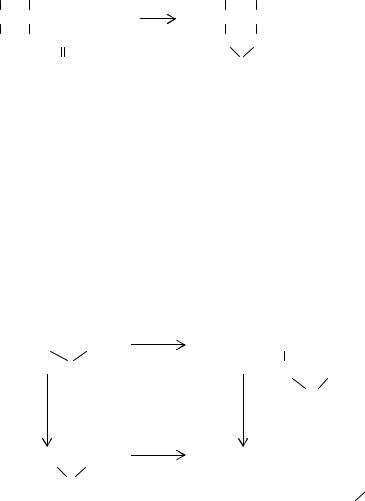
Циклокарбонаты могут быть получены и на основе -, -диолов взаимодействием с хлорангидридом угольной кислоты, со сложными алкиловыми эфирами угольной или хлоругольной кислот, с циклическими эфирами угольной кислоты:
|
|
|
|
|
COCl2 |
|
R—CH—O |
||||
|
|
|
|
|
|
|
|
C=O + 2HCl |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R —CH—O |
||
|
|
|
COCl(OR ) |
R—CH—O |
|||||||
|
|
|
|
|
C=O + HCl + R OH |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
R —CH—O |
||||
|
|
|
|
|
|
R—CH—O |
|||||
|
|
|
R''-O- |
|
C-OR''' |
||||||
R—CH—OH |
|
|
|
C=O + R OH + R OH |
|||||||
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R —CH—O |
||
R —CH—OH |
|
|
|
CH2-O |
|
||||||
|
|
|
|
|
C=O |
R—CH—O |
|||||
|
|
|
|
|
CH2-O |
||||||
|
|
|
|
|
|
|
|
C=O + HOCH2—CH2OH |
|||
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
R —CH—O |
||
|
|
|
|
|
|
|
|
|
R—CH—O |
||
|
|
|
2COCl(OR ) |
|
|
C=O + R 2CO3 + 2NaCl |
|||||
|
|
|
|
|
|
|
|
|
R —CH—O |
||
|
|
|
|
|
|
|
|
|
|||
567
Следует отметить, что эти способы используются только для синтеза низших алкиленкарбонатов ввиду ограниченности ассортимента -, -диолов. Их применение лимитировано высокой токсичностью сырья и коррозионной активностью среды вследствие выделения образующегося хлорида водорода.
Разработан также способ получения алкиленкарбонатов внутримолекулярной циклизацией -галогеналкилкарбонатов в присутствии каталитических солей ртути:
R1 |
R2 |
t0 |
R1 |
R2 |
|
R—C—C—R3 |
R—C—C—R3 + R4X, |
||||
Кат. |
|||||
X |
O—C—O—R4 |
|
O |
O |
|
|
O |
|
CO |
||
где Х – Hal.
14.5.4. Получение полифункциональных циклокарбонатов
Возможность использования полифункциональных циклокарбонатов позволяет получать новые полимеры различного строения на основе циклокарбонатов.
Так, каталитическим присоединением диоксида углерода к -оксидам может быть получен обширный класс полифункциональных циклокарбонатов, содержащих карбонатпропоксигруппу:
Cl—CH2—CH—CH2 |
|
CO2 |
Cl—CH2—CH—CH |
|
2 |
|
|||||
tº, Кат. |
|
|
|||||||||
|
|||||||||||
O |
|
|
|
|
O |
O |
|||||
-HCl R(OH)n |
|
|
|
R(OH)n |
-HCl |
CO |
|||||
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
R—(O—CH2—CH—CH2)n |
|
CO2 |
R—(O—CH2—CH—CH2)n |
||||||||
tº, Кат. |
|||||||||||
|
|
|
|||||||||
O |
|
|
|
|
|
O O |
|||||
 CO
CO
В качестве полигидроксисоединения используют алкиленгликоли – этиленгликоль, пропиленгликоль, и ддругие, полигидроксиалкиленгликоли - диэтиленгликоль, полиоксиэтиленгликоль, полиоксипропиленгликоль и другие, триолы –
568
глицерин, тригидроксиметилпропан, пентаэритрол, многоатомные фенолы – резорцин, гидрохинон, пиргаллол, флороглюцин, алкиленбисфенол.
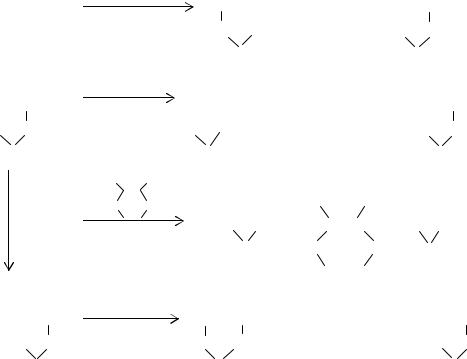
Полифункциональные циклокарбонаты различного строения с карбонатпропоксигруппами могут быть получены и на основе гидроксипропиленкарбоната:
|
|
|
|
|
|
|
|
O |
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
Cl-C-R- |
C-Cl |
|
|
|
|
|
CH2 |
|
CHCH2OCRCOCH2 |
|
CHCH2 |
||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O O |
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CO |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CO |
|||||||||||
|
|
|
|
|
|
|
|
OCN-R-NCO |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
O |
|
|
|
|
|
|
|
|
|
||||||||||||||||||
HOCH2 |
|
CHCH2 |
|
|
CH2 |
|
CHCH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
OCNHRNHCOCH2 |
|
CHCH2 |
||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||
|
|
O O |
|
|
|
|
|
|
|
|
|
O |
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O O |
||||||||||||||||||||||
|
|
|
|
CO |
|
|
|
|
|
|
|
|
|
|
|
CO |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CO |
||||||||||||||||
|
|
|
|
|
|
|
|
Cl |
|
|
Cl |
|
|
|
|
|
|
|
|
|
CH2 |
|
CHCH2O |
OCH2CHCH2 |
|||||||||||||||||||||||||||||
|
|
|
|
COCl2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||
|
|
|
|
|
O |
O |
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O O |
|
|
|
|
|
CHCH |
|
|
O O |
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
CO |
|
|
|
|
O |
O |
|
|
|
CO |
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2CH2 |
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
HO-C6H5- |
|
C-C6H5-OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
O |
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||
|
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
ClCOCH2 |
|
CHCH2 |
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
CHCH2OCOC6H4OCOCH2 |
|
CHCH2 |
|||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||
|
|
|
|
O O |
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O O |
|||||||||||
|
|
|
|
|
|
CO |
|
|
|
|
|
|
|
|
|
|
|
|
CO |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CO |
|||||||||||
Синтезированы также высокомолекулярные полифункциональные циклокарбонаты, например поливиниленкарбонат, и сополимеры виниленкарбоната с другими ненасыщенными соединениями.

570
м- и п-крезолы, 2,3-, 2,4-, 2,5-, 2,6-, 3,4- и 3,5- ксиленолы, и двухатомный фенолрезорзин.
Выделение фенолов из продуктов переработки угля
Фенол, обнаруженный Ф. Рунге в 1834 г. в каменноугольной смоле, был назван им карболовой кислотой. В 1867 г. его синтезировали путем щелочного плавления бензолсульфокислого натрия. Однако лишь незадолго до начала ХХ столетия было организовано промышленное производство фенола по этому способу в связи с большой потребностью в сырье для получения пикриновой кислоты. Особенно значительно спрос на фенол возрос после Второй мировой войны.
Втечение длительного времени фенолы получали только термической переработкой топлив. Развитие химических производств в 30-е годы ХХ в., и, особенно после Второй мировой войны, привело к созданию массового промышленного производства синтетического фенола. Крезолы и ксиленолы до начала 70-х годов также вырабатывали только из продуктов термической переработки топлив.
Фенолы - попутный продукт любых процессов переработки твердых топлив. При переработке топлива значительная часть содержащегося в нем кислорода переходит в состав образующихся фенолов. В настоящее время единственным широко используемым процессом термической переработки твердых топлив является высокотемпературное коксование, основное назначение которого – производство кокса.
Вкаменноугольной смоле коксохимического производства содержится от 0,01 до 0,1% фенолов, в продуктах полукоксования – от 0,5 до 0,7%, в масле, образующемся при гидрогенизации, и в сточных водах – от 0,8 до 3,7%. В смоле бурого угля и в сточных водах полукоксования содержится от 0,1 до 0,4% фенолов, в жидкофазном масле и в сточных водах – от 0,8 до 3,8%.
Состав фенолов зависит от режима коксования. Так, фенолы высокотемпературной каменноугольной смолы кроме фенола, крезолов и небольшого количества ксиленолов содержат в высококипящих фракциях нафтолы, фенилфенолы и их метилпроизводные. В более высококипящих фракциях содержатся также флуоренол, аценафтенол, фенантрол. Состав высококипящих фенолов первичных смол совершенно иной. Здесь широко представлены гомологи фенола с длинными боковыми цепями: этил- и изопропилфенолы, другие алкилфенолы, производные двухатомных фенолов, особенно резорцина, а также гомологи нафтолов.
Втабл. 15.1 приведен изомерный состав получаемых фенолов при различных режимах пиролиза твердого топлива. Как следует из таблицы, при переходе от полукоксования к коксованию увеличивается относительное содержание м- крезола. При этом происходит уменьшение содержания п-крезола, а затем и о- крезола. Таким образом, высокотемпературные каменноугольные смолы отличаются не только высоким содержание наиболее ценных соединений – фенола и крезолов, но и заметно более высоким относительным содержанием м-крезола.
