
monomers-Платэ-книга
.pdf
611
Синтез метилфенилдихлорсилана
Метилфенилдихлорсилан получают дегидроконденсацией метилдихлорсилана и бензола:
CH3SiHCl2 + C6H6 |
CH3(C6H6)SiCl2 + H2. |
Реакцию проводят под давлением при 513-523 К, при соотношении исходных реагентов бензол:метилдихлорсилан, равном 3:1, в присутствии борной кислоты в качестве катализатора.
Гидросилилирование ненасыщенных соединений
Реакция гидросилилирования заключается в присоединении кремнийорганических соединений, имеющих связь Si—H, по кратным связям ненасыщенныхпредельных соединений. Гидросилилирование можно инициировать пероксидами, УФ- и γ-излучением. В качестве катализаторов наиболее широко используется раствор платинохлористоводородной кислоты (H2PtCl6) в спиртах, в качестве сокатализаторов – фосфины, амины. В зависимости от природы исходных компонентов и катализатора гидросилилирование проводят при 273-423 К. Гидросилилирование можно проводить как по периодической схеме в обычных аппаратах с мешалками, так и в непрерывном режиме в проточной установке.
В качестве объектов силилирования могут использоваться олефины. Реакция катализируется пероксидами или соединениями на основе платины:
(C2H5O)3SiH + CH2=CH—CH2NH2  (C2H5O)3SiCH2CH2CH2NH2,
(C2H5O)3SiCH2CH2CH2NH2,
Cl2(CH3)SiH + CH2=CH—CN  Cl2(CH3)SiCH2CH2CN,
Cl2(CH3)SiCH2CH2CN,
Cl2(CH3)SiH + CH2=CHCF3 |
Cl2(CH3)SiCH2CH2CF3, |
|||
RCH=CH2 + SiHCl3 Пероксид RCH2—CH2—SiCl3, |
||||
|
Pt |
|
||
RCH=CH2 + CH3SiHCl2 |
RCH2—CH2—SiCl2. |
|||
|
|
|
CH3 |
|
Силилирование ацетилена позволяет получать винильные кремнийоргани- |
||||
ческие соединения: |
|
|
|
|
Pt |
|
|||
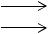
Cl3SiH + HC CH |
|
Cl3Si-CH=CH2 |
||
|
||||
HC CH + RSiHCl2 H2PtCl6 |
CH2=CH—SiRCl2. |
|||
612
Метод высокотемпературной конденсации
Винилтрихлор- и метилвинилдихлорсиланы синтезируют методом высокотемпературной конденсации при 823-843 К и времени контакта 280-300 с:
CH2=CHCl + SiHCl3 |
CH2=CHSiCl3 + HCl, |
CH2=CHCl + CH3SiHCl2 |
CH3(CH2=CH)SiCl2 + HCl. |
Наряду с основными реакциями протекают побочные реакции образования тетрахлорида кремния, а также метана, этана, этилена, водорода, углерода и (при производстве метилвинилдихлорсилана) диметилдихлорсилана.
Производство осуществляется по той же схеме, что и синтез фенилтрихлорсилана. На ректификацию поступают смеси примерно следующего состава (в % (мас.)):
При синтезе винилтрихлорсилана |
|
Винилхлорид, трихлорсилан и тетрахлорид кремния…… |
28 |
Винилтрихлорсилан ………………………………………. |
32 |
Кубовый остаток …………………………………………... |
40 |
При синтезе метилвинилдихлорсилана |
|
Винилхлорид, метилдихлорсилан, диметилдихлорсилан |
|
и тетрахлорид кремния ……………..……………………... |
16 |
Винилтрихлорсилан ………………………………………. |
10 |
Метилвинилдихлорсилан ……………………………….… |
14 |
Кубовый остаток …………………………………………... |
60 |
Винилхлорид, трихлорсилан и промежуточную фракцию возвращают на синтез винилтрихлорсилана. Винилхлорид, промежуточные фракции до и после метилдихлорсилана и метилдихлорсилан возвращают на синтез метилвинилдихлорсилана. При получении метилвинилдихлорсилана, предназначенного для производства каучука, проводят повторную ректификацию метилвинилдихлорсилана.
16.2.3. Получение органохлорсиланов по реакциям диспропорционирования
Органохлорсиланы с различными заместителями у атома кремния могут быть получены с использованием реакций диспропорционирования. Диспропорционирование органохлорсиланов с метильными и фенильными заместителями позволяет получать кремнийорганические мономеры с метильными и фенильными заместителями у одного атома кремния:
C6H5SiCl3 + (CH3)3SiCl C6H5(CH3)SiCl2 +
C6H5(CH3)SiCl2 +
+ C6H5(CH3)2SiCl + (CH3)2SiCl2 + CH3SiCl3.

613
Реакцию обычно проводят при 523-673 К под давлением. В качестве катализаторов применяют кислоты Льюиса.
16.2.4. Пиролитические способы получения органохлорсиланов
Пиролитические способы получения органохлорсиланов обычно реализуют в проточной системе (в газовой фазе) при 773-1023 К. При этом используют полые реактора из стали, меди, керамики или кварца. Из этих способов наибольшее значение имеет термическая конденсация, при которой происходит взаимодействие арилили алкенилхлоридов с трихлорсиланом или органогидридхлорсиланами:
 RR nSiCl3-n + HCl
RR nSiCl3-n + HCl
RCl + HSiR nCl3-n
 RH + R nSiCl4-n
RH + R nSiCl4-n
Наряду с целевой реакцией конденсации с образованием кремнийорганического мономера, протекает также побочная реакция восстановления с образованием углеводорода.
Метод термической конденсации особенно удобен для синтеза органохлорсиланов с двумя различными органическими заместителями у атома кремния:
C6H5Cl + HSiCH3Cl2  C6H5Si(CH3)Cl2 + HCl.
C6H5Si(CH3)Cl2 + HCl.
Его применяют в промышленности для получения винилтрихлорсилана, метилвинилдихлорсилана и фенилтрихлорсилана:
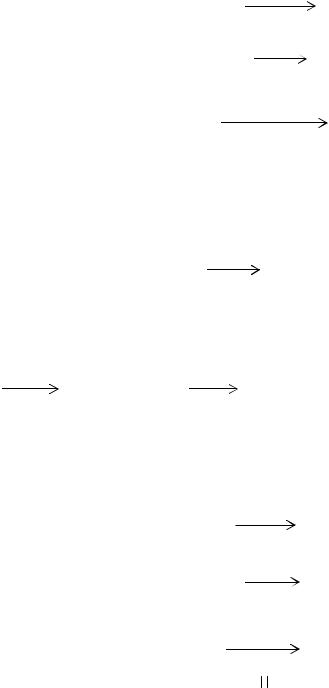
CH2=CHCl + HSiCl3 |
CH2=CHSiCl3 + HCl, |
CH2=CHCl + HSi(CH3)Cl2 CH2=CHSi(CH3)Cl2 + HCl,
CH2=CHSi(CH3)Cl2 + HCl,
C6H5Cl + HSiCl3 |
C6H5SiCl3 + HCl. |
614
16.2.5. Получение кремнийорганических мономеров химическими превращениями органохлорсиланов
Органохлорсиланы могут быть превращены в различные кремнийорганические мономеры проведением реакций замещения по связи Si–Сl. Силанолы можно получать гидролизом кремнийорганических соединений в мягких условиях:
(C6H5)2Si(OCH3)2 + 2H2O-CH3OH |
(C6H5)2Si(OH)2, |
|||
[(CH3)3Si]2NH +2H2O -NH3 |
2(CH3)3SiOH, |
|||
|
RSi—H + H2OКат (Ni, Pt, Pd) |
|
|
|
|
|
|
RsiOH. |
|
|
|
|||
|
-H2 |
|
|
|
|
|
|
|
|
Силанолы с алифатическими заместителями в результате межмолекулярного взаимодействия легко отщепляют воду, превращаясь при этом в силоксаны.
Органосилазаны получают аммонолизом органохлорсиланов:
2(CH3)3SiCl + NH3 -HCl (CH3)3SiNHSi(CH3)3.
Линейные полиорганосилоксаны получают поликонденсацией циклосилоксанов, которые образуются при гидролитической конденсации диорганодихлорсиланов:
|
H2O |
|
|
CH3 |
|
|
Линейные |
||
|
|
|
|
|
|
|
|
||
(CH3)2SiCl2 |
[(CH3)2Si(OH)2] -H2O |
—Si—O— |
+ |
полиметил- |
|||||
-HCl |
|||||||||
|
|
|
|
|
|
||||
|
|
|
|
CH3 |
|
n |
силоксаны |
||
Органоалкокси- и органоацилоксисиланы синтезируют взаимодействием органохлорсиланов соответственно со спиртами, кислотами или их производными - алкоголятами, солями, ангидридами и др.:
|
(CH3)2SiCl2 + 2C2H5OH -HCl |
(CH3)2Si(OC2H5)2, |
|||||||||
|
C6H5SiCl3 + 3CH3COONa |
|
C6H5Si(OCOCH3)3, |
||||||||
|
O |
O |
-NaCl |
|
O |
||||||
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
RSi—Cl + CH3-C—O—C-CH3 |
O |
RSi—O- |
|
C—CH3 |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
- CH3CCl

615
Циклосилоксаны являются мономерами для синтеза линейных полиорганосилоксанов. Они могут быть получены гидролитической конденсацией диорганодихлорсиланов:
|
|
|
|
|
|
|
|
|
H5C6 CH3 |
|
H5C6 C6H5 |
H3C |
|
CH3 |
|
H5C6 |
OSiO |
CH3 |
|||
|
|
|||||||||
|
|
|
|
|
|
Si |
Si |
|||
HOSiOSiOH + ClSiOSi |
-HCl |
|||||||||
|
|
|
|
|
|
|
H3C |
OSiO |
CH3 |
|
H3C CH3 |
H3C CH3 |
|
||||||||
|
|
|
|
|
|
|
|
|
H3C CH3 |
|
Циклосилоксаны могут быть также получены взаимодействием диметилдихлорсилана с метанолом:
ZnCl2
CH3)2SiCl2 + 2CH3OH  2CH3Cl + [— (CH3)2Si—O—]n + H2O.
2CH3Cl + [— (CH3)2Si—O—]n + H2O.
16.2.6 Получение тетрахлорсилана
Тетрахлорсилан, или тетрахлорид кремния, - наиболее доступное соединение кремния, основным сырьем для промышленного производства которого является металлургический ферросилиций. Впервые тетрахлорид кремния был получен взаимодействием кремния с хлором при повышенной температуре:
Si + 2Cl2 |
SiCl4. |
Кремний начинает хлорироваться при 473-513 К. Использование в качестве катализаторов хлоридов калия, кальция или алюминия позволяет снизить температуру синтеза до 413 К. Этот способ нашел мировое промышленное применение. При 1173-1273 К тетрахлорид кремния реагирует с кремнием с образованием дихлорсилена, взаимодействие которого с хлоридом водорода является эффективным способом получения трихлорсилана:
2Si + SiCl4 |
2SiCl2 |
SiCl2 + HCl |
HSiCl3. |
В качестве перехватчиков SiCl2 могут быть использованы и другие соединения, что делает способ синтеза кремнийорганических соединений на базе тетрахлорида кремния весьма перспективным.

616
Тетрахлорид кремния в среде эфира при 333 К реагирует с аммиаком с образованием соединений циклосилазановой структуры и полихлорсилазанов, в основном состава (Cl2SiNH)х.
Гидролитической соконденсацией тетрахлорида кремния с кремнийоргант-
ческими диолами получают органоспиросилоксаны |
|
||
R R |
|
R R |
|
SiO |
|
OSi |
|
O |
Si |
O |
|
SiO |
|
OSi |
|
R R |
|
R R |
, |
где R-органическая группа.
Взаимодействие тетрахлорида кремния с алкоксисиланами позволяет получать кремнийорганические соединения со смешанными функциями:
(CH3)3SiOCH3 + SiCl4 (CH3)3SiCl + CH3OSiCl3.
(CH3)3SiCl + CH3OSiCl3.
В качестве катализаторов применяют HCl и ROH (R=Н, СН3 и др.).
16.2.7. Очистка диорганодихлорсиланов
Для получения высокомолекулярных каучукоподобных полисилоксанов необходимо использовать диорганодихлорсиланы высокой степени чистоты. Особенно высокие требования предъявляются к чистоте диорганодихлорсиланов в тех случаях, когда синтез полимеров осуществляется конденсационными методами. Примеси монофункциональных органических соединений снижают молекулярную массу синтезируемых полимеров, а наличие примесей трифункциональных соединений приводит к разветвлению и сшиванию полимерных цепей, вследствие чего уменьшается растворимость и ухудшаются технологические свойства полимера. Так, при синтезе полидиметилсилоксанового каучука конденсационным способом в исходном диметилдихлорсилане допустимо наличие не более 0,01% (мас.) монофункциональных и не более 0,02% (мас.) трифункциональных кремнийорганических соединений.
При синтезе полисилоксановых эластомеров методом полимеризации циклосилоксанов требования к чистоте исходных диорганодихлорсиланов могут быть несколько снижены, так как для получения циклосилоксанов из продуктов гидролиза проводится их дополнительная очистка.
За исключением специальных случаев, недопустимо наличие в диорганодихлорсиланах примесей кремнийорганических соединений, содержащих кремнийгидридные связи.
Очистка диорганодихлорсиланов от примесей сопряжена с большими трудностями ввиду сложности смесей, близости температур кипения вредных приме

617
сей и целевых продуктов. Так, разница в температурах кипения диметилдихлорсилана (343,1 К) и его основной примеси – метилтрихлорсилана (339 К) составляет ~ 4о. Кроме того, в продуктах прямого синтеза метилхлорсиланов имеется еще примесь этилдихлорсилана, кипящего при 347,5 К.
Диметилдихлорсилан очищают от примесей с помощью многоколонной ректификационной системы непрерывного действия, имеющей в общей сложности более 380 ситчатых и колпачковых тарелок.
16.3. МОНОМЕРЫ ДЛЯ СИЛОКСАНОВЫХ КАУЧУКОВ
Возможность получения и применения высокомолекулярных кремнийорганических соединений была показана К.А. Андриановым в 1935-1936 гг. Из соединений различных классов наибольшее применение нашли полисилоксаны, полимерная цепь которых состоит из чередующихся атомов кислорода и кремния, связанного с заместителями различной химической природы:
R —Si—O—,
R
где R, R – Н, Alk,Alkenyl, Ar (в R, R могут быть различные полярные заместители).
Силоксановые каучуки характеризуются высокой термостойкостью, поскольку прочность связи Si—О составляет 440-495 кДж/моль по сравнению с 360 кДж/моль для связи С—С в карбоцепных полимерах. Кроме того, силоксановые полимеры имеют высокую гибкость цепей, потенциальный барьер вращения молекулы относительно связи Si—О чрезвычайно низок, и полисилоксаны сохраняют эластичность до 213 – 173 К. Гибкость полимерных цепей силоксанов зависит от типа заместителя и по уменьшению гибкости цепи силоксановые звенья располагаются в ряд:
H |
CH3 |
|
|
CH=CH2 |
C6H5 |
C6H5 |
|||||
|
|
|
|
||||||||
—SiO— > —SiO— > —SiO— |
> —SiO— > —SiO— |
||||||||||
|
|
CH3 |
|
|
|
|
|
|
|
|
|
|
CH3 |
CH3 |
CH3 |
C6H5 |
|||||||
16.3.1. Получение силоксановых каучуков
Первые промышленные силоксановые каучуки появились в начале 1950-х годов и к началу 1980-х годов общий объем производства полисилоксанов в мире составил ~200 тыс. т/год. Наиболее массовыми каучуками являются полидиметил

618
силоксановый каучук СКТ |
|
|
||
|
|
CH3 |
CH3 |
|
|
|
|
||
|
|
|
|
|
HO—[—Si—O—]n—Si—OH, (n = 5400-8780) |
||||
CH3 |
CH3 |
|||
и его непредельные аналоги – каучуки СКТВ и СКТВ-1
CH3 |
CH=CH2 |
CH3 |
n = 5400-8780; |
||
|
|
|
|
|
|
HO—[—Si—O—]n—[—Si—O—]m—Si—OH |
m = 5,4-8,78 для СКТВ, |
||||
CH3 |
CH3 |
CH3 |
m = 27-74 для СКТВ-1. |
||
Силоксановые каучуки СКТ, СКТВ и СКТВ-1 могут эксплуатироваться при температурах от 223 до 523 К. Более широким температурным интервалом эксплуатации обладают каучуки, содержащие наряду с метильными и винильными заместителями фенильные группы,
CH=CH2 |
C6H5 |
CH3 |
HO—[—Si—O—]m—[—Si—O—]n—[—Si—O—]k—H m:n:k=3:80:917
|
|
CH3 |
CH3 |
CH3 |
|||
способные работать в интервале температур от 203 до 523 К и кратковременно при 573 К.
Силоксановый каучук, содержащий этильные заместители (СКТЭ)
|
CH3 |
C2H5 |
|
CH3 |
|
|
|
|
|
|
|
HO— [Si—O]m—[Si—O]n—[Si—O]p—H m:n:p=91,87:8:0,03, |
|||||
CH3 |
C2H5 |
CH=CH2 |
|||
имеет более высокую морозостойкость по сравнению с каучуками СКТ и СКТВ. В отличие от органических из силоксановых каучуков не получаются рези-
ны с высокими прочностными показателями. Так, условная прочность резин при растяжении не превышает 10-12 МПа при относительном удлинении не выше
600%.

619
Недостатком силоксановых резин является низкое сопротивление раздиру, а также значительное набухание в маслах и растворителях.
Более высокой маслобензостойкостью обладают силоксановые каучуки, содержащие полярные заместители:
CH3 |
CH2CH2CH2CN |
|
CH3 |
CH3 |
||
|
|
|
|
|
|
|
[—Si—O]n—[—Si—O—]m ; |
[—Si—O]n—[—Si—O—]m |
|||||
CH3 |
CH3 |
CH3 |
CH2CH2R |
|||
Нитрилсилоксановый каучук |
Фторсилоксановый каучук (СКТФ; R = C2F5, |
|||||
|
|
|
|
C3F7 и другие перфторалкилы ) |
||
Производятся также бор- и фосфорсилоксановые каучуки, в которых в основную цепь вводятся атомы бора или фосфора, разделяющие силоксановые группировки. Эти каучуки обладают повышенной термостойкостью и эластичностью, но легко гидролизуются даже под влиянием влаги воздуха.
Биологическая и физиологическая инертность силоксановых резин позволяет широко использовать их в биологии и медицине. Их применяют для изготовления медицинских трубок, искусственных вен и артерий, зондов, митральных клапанов сердца, для имплантации в хирургии.
Низкомолекулярные каучуки СКТН и СКТН-1 используются для производства литых деталей, защитных покрытий, изоляции проводов и кабелей, для герметизации электрических узлов и блоков. Поверхности, покрытые пленкой вулканизатов СКТН и СКТН-1, гидрофобны и препятствуют образованию льда. На основе этих каучуков изготовляют различные заливочные компаунды.
16.3.2. Получение силоксановых мономеров гидролизом диорганодихлорсиланов
Путем гидролиза диорганодихлорсиланов в зависимости от условий реакции
получают циклосилоксаны, силан- и силоксандиолы, , - дихлорполидиорганосилоксаны (хлоролигомеры) или смеси указанных соединений, являющихся исходными веществами для получения соответствующих эластомеров различными методами.
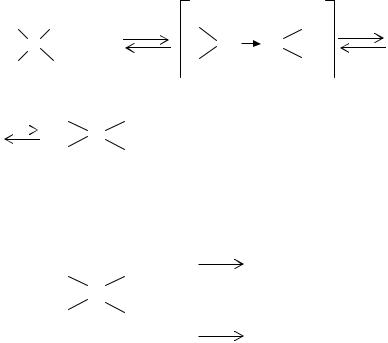
620
Общие сведения о гидролизе диорганодихлорсиланов
Реакция гидролиза диорганодихлорсиланов обычно протекает очень быстро. Предполагается, что вначале образуется промежуточный комплекс с пентакоординационным атомом кремния, распадающийся с выделением хлорида водорода:
R |
Cl |
|
|
H |
|
R |
|
Cl |
|
|
|||||
Si |
+ H2O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O: Si |
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
R |
Cl |
|
|
H |
|
R |
|
Cl |
|
|
|||||
|
R |
Cl |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Si |
+ HCl |
|
|
|
|
|
|
|
|
|
|
|||
|
R |
OH |
|
|
|
|
|
|
|
|
|
|
|||
Образующийся хлорсиланол является неустойчивым соединением. Он не- |
|||||||||||||||
медленно реагирует с водой или диорганодихлорсиланом: |
|
|
|||||||||||||
|
|
|
|
|
|
H2O |
|
|
|
R |
|
|
|||
|
R |
Cl |
|
|
|
|
|
|
|
|
|
||||
|
|
HO—Si—OH |
|||||||||||||
|
Si |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
RR SiCl |
|
R |
|
|
||||||
|
|
|
|
|
|
|
|||||||||
|
R |
OH |
R |
R |
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Cl—Si—O—Si—Cl |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R |
R |
|||||
Полученные силандиол и дихлорсилоксан вступают в дальнейшие реакции конденсации с образованием линейных или циклических олигомеров.
Результаты гидролиза зависят как от свойств хлорсиланов, так и от других факторов: рН среды, температуры, природы растворителей и др.
При проведении гидролиза в строго нейтральной среде получаются силанили силоксандиолы. В последнем случае количество силоксановых звеньев в молекуле определяется главным образом величиной и природой органических радикалов у атома кремния. Силандиолы с объемистыми радикалами конденсируются медленно и образуют 4-8-звенные силоксандиолы.
Гидролиз диорганодихлорсиланов в щелочной среде приводит к преимущественному образованию линейных силоксандиолов, причем их молекулярная масса возрастает при увеличении концентрации щелочи в реакционной среде.
Гидролиз в кислой среде вызывает преимущественное образование циклосилоксанов. Наконец, при гидролизе в сильнокислой среде (в концентрированной соляной кислоте) или в условиях недостатка воды образуются преимущественно-, -дихлорполидиорганосилоксаны.
