
monomers-Платэ-книга
.pdf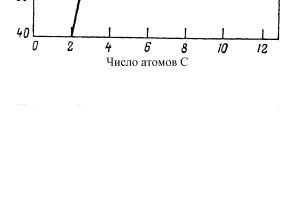
91
В направлении (1) синтез проводят на кобальтовых катализаторах, например
Co-ThO2, Co-ThO2-Mgo или кобальт-циркониевых, при 450-480 К и 0,1-1,5
МПа. В прсутствии катализаторов на основе железа при 500-550 К и 0,5-1,0 МПа реакция проходит по схеме (2). Выход углеводородов составляет до 180 мл на 1 м3 газовой смеси. Основными продуктами процесса являются терминальные олефины ( -олефины).
Синтез углеводородов из СО и Н2 по методу Фишера-Тропша применяется не только для производства моторных топлив, но и в нефтехимической промышленности для получения, в частности, олефинов. В настоящее время производство низкокипящих олефинов как основного продукта синтеза Фишера-Тропша
nСО + 2nН2 СnН2n + nН2О
СnН2n + nН2О
является конкурентоспособным с производством этих олефинов из нефти. При осуществлении процесса в псевдоожиженном слое катализатора ос-
новную часть продуктов синтеза составляют -олефины, которые в результате вторичных реакций частично превращаются в -олефины. Содержание олефинов в продуктах синтеза зависит от условий реакции и свойств катализатора.
На рис. 3.1 представлена графическая зависимость среднего содержания олефинов в углеводородах, синтезированных во взвешенном слое порошкообразного железного катализатора, от числа атомов углерода во фракции. Во фракции С2 содержание этилена обычно состав-
ляет 25-40%.
Рис. 3.1. Зависимость содержания оле финов в углеводородах, полученных методом Фишера-Тропша, от числа атомов углерода во фракции
При использовании железомарганцевых катализаторов, обладающих пониженной гидрирующей способностью, выход олефинов увеличивается и может достигать 85-90%.
Пропилен можно выделить также из полукоксовых газов и газов коксова-
ния.
При полукоксовании каменного угля при 773-873 К образуется 10% газа, содержащего от 1 до 8% пропилена. После выделения из коксового газа водорода содержание олефиновой фракции С3-С4 в оставшемся сжиженном газе достигает 54%, и этот газ может служить источником получения пропилена.
92
Термическое дегидрирование пропана
При термическом дегидрировании пропана получается пропилен с невысоким выходом, так как крекинг пропана с образованием метана и этилена (1) протекает легче, чем реакция дегидрирования (3):
С3Н8 |
СН4 + С2Н4 |
Н = - 67,5 кДж/моль, (1) |
2С3Н8 |
С2Н6 + С3Н6 + СН4 |
(2) |
С3Н8 |
С3 Н6 + Н2 |
Н = - 125,7 кДж/моль (3) |
Превалирующее образование этилена при термическом крекинге пропана объясняется тем, что для разрыва связи С—С нужно значительно меньше энергии (261,9 кДж/моль), чем для разрыва связи С—Н (364,5 кДж/моль для первичного атома углерода, 359,5 кДж/моль для вторичного атома углерода и 347,8 кДж/моль для третичного атома углерода). Кроме указанных продуктов образуются в небольшой степени также метилацетилен, аллен и другие, а также значительное количество кокса.
При повышении температуры равновесие дегидрирования сдвигается вправо. В связи с тем, что реакция протекает с увеличением объема, понижение давления способствует увеличению равновесного выхода пропилена. Термическое дегидрирование пропана осуществляют при температуре 873 К, атмосферном давлении и времени контакта 2,7 с. При этом достигается конверсия пропана 25% (мас.).
Каталитическое дегидрирование пропана и других низших алканов (процесс "Олефлекс")
Каталитическое дегидрирование пропана проводят в присутствии катализаторов - оксидов металлов: Cr2O3, MoO3, V2O5, TiO2 и GeO2. Наиболее эффек-
тивным катализатором является Cr2О3 на носителе -А12О3. Промышленные процессы осуществляют при температуре ~ 873 К. В этих условиях на оксидном хромовом катализаторе селективность по пропилену составляет 75-85% при конверсии пропана - 50-80%.
Дегидрирование ведут в реакторах с неподвижным слоем катализатора. В связи с интенсивным отложением кокса на катализаторе и необходимости его периодической регенерации, как правило, устанавливают в ряд несколько реакторов (не менее трех). Регенерацию катализаторов осуществляют путем выжигания кокса воздухом с последующей продувкой реактора паром. Длительность регенерации 15-25 мин.
Сконца 1980-х годов спрос на низшие олефины – пропилен и изобутилен
–значительно увеличился. Пропилен используют для производства полипропилена, а изобутилен – в основном для производства метил-трет-бутилового эфира (добавка к бензину, повышающая октановое число). На рис. 3.2 показано увеличение потребления этилена и пропилена в 1990-х годах. Около 70% про-

93
пилена производится на установках крекинга с водяным паром, 28% - на установках крекинга с катализатором в "кипящем слое", остальные 7% получают каталитической дегидрогенизацией пропана. Количество пропилена, производимого на установках крекинга, связано с количеством производимого этилена, который является основным целевым продуктом установок крекинга. Таким
образом, |
поскольку |
|
и |
сырье, и |
|
количество |
этилена |
|
определяются |
спросом |
|
на |
полиэтилен, |
|
количество |
|
|
пропилена, |
|
|
производимого |
на |
|
установках |
крекинга, |
|
Рис.3.2. Относительное увеличение потребления этилена и пропилена (потребление этилена и пропилена в 1989 г. принято за 1)
94
Рис. 3.3. Принципиальная технологическая схема установки «Олефлекс» (ЮОП)
1- реактор; 2 – аппарат для регенерации катализатора; 3 – турбоэкспандер; 4 – разделительная колонна.
Потоки: I – свежее и вторичное сырье; II – отходящие газы; III – продукт на дальнейшую обработку.
также зафиксировано и не может соответствовать увеличению потребления. Для увеличения количества пропилена используют процессы дегидрирования пропана.
Первые в мире промышленные установки каталитической дегидрогенизации низших алканов были созданы в 1939-1940 гг. для получения бутенов и бутадиена. Для дегидрирования использовали алюмохромовый катализатор и реактор со стационарным слоем. Однако катализатор имел низкую селективность и быстро дезактивировался. Время цикла между регенерациями варьировалось от 10 до 20 мин в зависимости от условий.
В конце 1960-х годов фирма ЮОП (США) разработала процесс дегидрирования пропана в реакторе с "кипящим слоем" алюмохромового катализатора. Однако в связи с тем, что в состав катализатора входит шестивалентный хром, известный как канцероген, в 1990-х годах компания осуществила процесс дегидрирования алканов керосиновой фракции до моноолефинов на катализаторе Рt/Al2O3. В 1990 г. был внедрен в промышленность процесс "Олефлекс" - дегидрирование пропана или изобутана (или их смеси) до соответствующих моноолефинов в присутствии катализатора Рt/Al2O3.
Установка "Олефлекс" состоит из реакторного узла, секции регенерации катализатора и секции разделения продукта (рис. 3.3). Для предотвращения коксоотложения исходное углеводородное сырье смешивают с циркулирующим газом.
Ниже приведен материальный баланс производства мощностью 250 тыс. т/год пропилена.
|
Количество, |
|
Количество, |
|
т/год |
|
т/год |
Пропановое сырье |
323400 |
Легкие фракции |
37600 |
Пропилен |
250000 |
Отделяемый С4 |
11 |
Водород |
24800 |
|
|
(балансовое количество)
Качество пропилена иллюстрируется табл. 3.6.
Таблица 3.6
Состав продуктов дегидрирования пропилена, получаемых на установке "Олефлекс".
95
|
Содержание |
Требование к |
Компонент |
промышлен- |
|
|
фактическое |
ному продукту |
Пропилен, % (мол.) |
99,5 |
99,92 |
Водород, ррm |
20 |
<5 |
Пропан, % (мол.) |
0,5 |
0,06 |
Этан, % (мол.) |
500 |
52 |
С4, С5 насыщенные углеводороды, ррm |
1000 |
<l |
Этилен, ррm |
100 |
<l |
Бутилены, ррm |
100 |
<l |
Ацетилены, ррm |
5 |
<l |
Проладиен, ррm |
5 |
<l |
Бутадиен, ррm |
10 |
<l |
Кислород, ррm |
2 |
<l |
Моноксид утлерода, ррm |
0,3 |
<0,1 |
Диоксид углерода, ррm |
5 |
<0,1 |
Общее содержание серы, весовых ррm |
1 |
<0,03 |
Метанол, ррm |
5 |
<l |
Пр и м е ч а н и е. ppm – части на 1 млн.
3.1.4.Получение бутена-1
Бутен- 1 (линейный бутен) используют для синтеза бутадиена-1,3, полибутилена, сополимеров с высшими -олефинами и других продуктов. Бутен-1 получают из фракции С4 пиролиза и крекинга нефтепродуктов, димеризацией этилена, дегидрированием н-бутана, дегидратацией бутанола, олигомеризацией этилена и др.
Выделение бутена-1 из углеводородных фракций С4
Первым промышленным методом получения бутена-1 был метод выделения его из фракции С4 различных нефтехимических процессов. Так как состав фракции С4 зависит от технологических условий получения и состава исходного сырья, то содержание бутена-1 в ней изменяется в пределах от 15 до 25%. Разделение фракции С4 и выделение из нее бутена-1 представляет определенные трудности, из-за близких температур кипения и летучести ее компонентов:
Углеводород |
Т. кип., К |
Углеводород |
Т. кип., К |
н-Бутан ................. |
272,50 |
Бутадиен-1,3.............……….. |
268,60 |
2-Метилпропан..... |
261,27 |
Бутин-1 .............…………….. |
281,07 |
Бутен-1 ................. |
266,74 |
Бутин-2 ................…………... |
299,99 |

96
цис-Бутен-2........... |
269,28 |
Бутенин-1(винилацетилен)… |
278,00 |
транс-Бутен-2 ..... |
273,88 |
Метилциклопропан .........….. |
277,50 |
2-Метилпропен-1 |
266,10 |
Циклобутан.........…………... |
286,08 |
Бутадиен-1,2 ........ |
283,85 |
|
|
Легче всего бутен-1 выделяется из фракции С4, получаемой при экстрактивной ректификации продуктов дегидрирования н-бутана. С этой целью в тех-
нологическую схему включают аппаратуру для очистки бутена-1 от примесей 2-метилпропена-1 и бутадиена-1,3. Наряду с традиционным способом разделения 2-метилпропена и бутена-1 экстракцией 2-метилпропена серной кислотой используют также методы, основанные на различной реакционной способности 2-метилпропена-1 и бутена-1: гидратацию, этерификацию первичными спиртами и алкилирование. Бутен-1 выделяют из фракции С4 также адсорбцией на молекулярных ситах.
Бутен-1 можно подвергнуть изомеризации в бутен-2. Гидроизомеризацию бутена-1 в бутены-2 проводят для упрощения схемы последующего разделения компонентов фракции С4 и для получения высокооктановых добавок к топливу - продуктов взаимодействия бутена-2 с изобутаном.
Бутен-1 концентрацией 98,5-99,5% можно получить с использованием н-
пентана в качестве элюента. Способ состоит из стадий предварительной ректификации, удаления бутадиена-1,3 гидрированием на палладиевом (на угле) катализаторе, осушки на цеолите NaA, селективной сорбции на цеолите СаА и ректификации.
Для получения бутена-1 со степенью чистоты, пригодной для полимеризации, его необходимо очистить от примесей, которые отрицательно влияют на катализаторы Циглера-Натта (от воды, кислорода, спирта, органических кислот, ацетиленовых, диеновых, сернистых и карбонильных соединений).
Ацетиленовые и карбонильные соединения удаляют путем гидрирования на палладиевом катализаторе. Диеновые и пероксидные соединения гидрируют на катализаторе Pd/Аl2O3 при 313-423 К.
Каталитическая димеризация этилена
Реакция присоединения этилена к гидриду алюминия и его алкильным производным была открыта К. Циглером. Присоединение этилена по связи алюминий-водород происходит при 333-353 К, а внедрение этилена по связи алюминий-углерод при 373-383 К. Схему процесса можно описать следующим образом:
Al—H + C2H4 |
Al—C2H5,. |
Al—C2H5 + nC2H4 |
Al—(C2H4)n—C2H5. |
Тот факт, что рост алкильной цепи и вытеснение -олефина происходит при разных температурах позволяет вести процесс получения -олефинов нор-
97
мального строения постадийно. Синтез -олефинов, включая бутен-1 был реализован в США в промышленном масштабе. В качестве катализатора использовали коллоидный никель. Процесс осуществляли при температуре 373-393 К, давлении 4,9 МПа, массовом соотношении никель:триэтилалюминий равном 0,01:1,0 и концентрации триэтиллалюминия 5% (мас.). Продолжительность работы катализатора составляла 200 ч. Степень конверсии этилена в бутен-1 достигала 20%, селективность – 90%. При этом получался бутен-1 высокой чистоты.
Димеризацию этилена можно проводить также на других катализаторах. Термическая димеризация этилена в бутен-1 не нашла промышленного
применения из-за низкой селективности процесса.
3.1.5. Получение изобутилена
Изобутилен был впервые описан в 1825 г. М. Фарадеем, который выделил его из продуктов высокотемпературного разложения животных жиров. В 1875 г. изобутилен был получен А. Вюрцем при пиролизе сивушных масел. В 1868 г. А.М. Бутлеров получил изобутилен путем отщепления воды от трет- бутилового спирта разбавленной серной кислотой. Изобутилен используется в производстве бутилкаучука и изопрена.
Выделение изобутилена из углеводородных фракций С4
Одним из основных промышленных способов получения изобутилена является его выделение из бутан-бутеновой фракции производства бензинов или этилена каталитическим или термическим крекингом или пиролизом жидких нефтепродуктов и нефтяных газов. Выход фракции С4 в этих трех процессах составляет соответственно 3-10, 1-2 и 0,4-5% (мас.). Типичный средний состав фракции С4 ( в % (мас.)) термического крекинга приведен ниже:
Компоненты |
Термический |
Каталитический |
крекинг |
крекинг |
|
С3-Углеводороды |
0,3 |
0,5 |
(сумма) |
|
|
н-Бутан |
5,2 |
11,0 |
Изобутан |
1,3 |
33,0 |
Бутен-1 |
16,0 |
12,0 |
цис-Бутен-2 |
5,3 |
11,0 |
транс-Бутен-2 |
6,6 |
14,0 |
Изобутен |
27,4 |
18,0 |
Бутадиен |
37,0 |
Следы |
Ацетилен |
0,4 |
Следы |

98
С5- Углеводороды |
0,5 |
0,5 |
(сумма)
Изобутилен из фракций С4 выделяют путем экстракции 65%-ной серной кислотой (способ А.М. Бутлерова) при температурах близких к комнатной. Экстракция протекает практически количественно. В результате получается трет-бутилсерная кислота
(СН3)2С=СН2 + Н2SО4  (СН3)3СОSО3Н, которую вновь превращают в изобутилен.
(СН3)3СОSО3Н, которую вновь превращают в изобутилен.
По другому способу изобутилен выделяют из бутилсерной кислоты, гидролизом ее острым паром, в результате чего образуется трет-бутиловый спирт:
(СН3)3СОSО3Н + Н2О 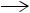 (СН3)3СОН + Н2SО4 .
(СН3)3СОН + Н2SО4 .
Последний дегидратируют 30%-ной серной кислотой до получения изобутилена:
(СН3)3СОН Н2SО (СН3)2С=СН2 + Н2О.
Применение этого способа ограничено высокой стоимостью процесса регенерации серной кислоты.
Более эффективным является способ, в котором реакционную жидкость, полученную экстракцией изобутилена, 65%-ной кислотой, разбавляют водой до концентрации кислоты 45%. При нагревании этого раствора при низком давлении выделяется чистый изобутилен, который промывают щелочью, освобождают от спирта путем охлаждения, промывают водой и сжижают под давлением.
Фирма "Юнион Карбайд" разработала процесс выделения изобутена из фракций С4 парового крекинга путем адсорбции на цеолитах. В этом процессе выделяется также бутен-1, который изомеризуют в изобутилен.
Дегидрирование изобутана
Изобутилен в промышленности получают также каталитическим дегидрированием изобутана. Процесс аналогичен описанным процессам дегидрирования других углеводородов до соответствующих олефинов.
Дегидрирование изобутана осуществляют в присутствии твердых катализаторов - оксидов металлов VI группы Периодической системы Д.И. Менделеева, способных к активированной адсорбции водорода при повышенной температуре. На практике наибольшее распространение получили катализаторы на основе оксида хрома, нанесенного на оксид алюминия. Наиболее активна аморфная форма оксида трехвалентного хрома Cr2O3, содержащая некоторое количество соединений шестивалентного хрома.
99
В промышленности дегидрирование изобутана проводят как в стационарном, так и в подвижном слое катализатора при 823-893 К.
Изомеризация бутена-1
Процесс изомеризации бутена-1 в изобутилен является важным промышленным способом получения изобутилена. Наибольшее развитие в России и за рубежом получили промышленные процессы изомеризации н-бутена на гетерогенных бифункциональных катализаторах (преимущественно, алюмоплатиновых), модифицированных соединениями хлора и фтора.
В 1980-е годы для этого процесса были разработаны каталитические системы на основе цеолитов.
Первые цеолитсодержащие катализаторы для изомеризации н-алканов были получены на основе декатионированных и кальциевых форм цеолитов типа фожазита и морденита введением в них платины или палладия. При замене платины или палладия на родий или иридий изомеризующая активность катализатора резко снижается, а выход продуктов крекинга возрастает.
Промышленный катализатор изомеризации содержит обычно ~0,5 % палладия. Реакцию проводят при температурах в интервале от 573 до 673 К и давлении водорода 2,0-3,0 МПа.
Синтез изобутилена из ацетона
В лабораторных условиях изобутилен может быть получен из ацетона на твердом кислотном катализаторе, например каолине, при 673-723 К. На катализаторе происходит альдольная конденсация двух молекул ацетона с образованием мезитилоксида с последующим разложением его водой до изобутилена и
уксусной кислоты: |
|
|
|
|
|
|
|
|||||
O |
|
|
|
|
|
|
|
|||||
|
|
|
OH- |
CH3—CO—CH2 —C(OH)—CH3 |
|
|||||||
|
|
|
||||||||||
2CH3—C—CH3 |
H2O |
|||||||||||
|
|
|
||||||||||
Ацетон |
|
|
|
|
|
|
|
|||||
|
|
CH3 |
|
|
||||||||
|
|
|
|
|
|
H2O |
|
|
|
|
O |
|
CH3—CO—CH=C—CH3 |
CH3—C—CH |
3 |
+ CH3—C |
|||||||||
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
OH |
||||
|
|
|
CH3 |
|
|
|
|
|||||
|
|
Мезитилоксид |
|
|
|
|
|
|
|
|||
Этот метод не нашел, однако, промышленного применения
3.2.ВЫСШИЕ ОЛЕФИНЫ
3.2.1.Получение высших олефинов димеризацией и содимеризацией олефинов

100
Впервые димеризация олефинов в присутствии серной кислоты была осуществлена А.М. Бутлеровым. Однако эта реакция не нашла широкого практического применения вплоть до открытия К. Циглером в 1952 г. селективной димеризации с помощью алюминийорганических соединений, когда была показана принципиальная возможность синтеза этим путем индивидуальных высших олефинов заданного строения.
Катионная димеризация олефинов
Кислотные катализаторы не применяют для димеризации олефинов из-за их низкой селективности. При димеризации, например, пропилена катион катализатора атакует молекулу пропилена в соответствии с правилом Марковникова:
CH3—CH=CH+ |
|
|
H+ |
+ |
+ |
2 |
|
|
CH3—CH—CH3, |
||
CH3—CH=CH2 + CH3—CH—CH3 |
CH3—CH—CH2—CH—CH3 -H+ |
||||
CH3 |
|
|
CH3 |
|
|
|
—CH—CH=CH—CH3 |
|
|||
|
|
||||
|
CH3 |
|
|
||
Образующийся промежуточный изогексильный катион быстро взаимо- |
|||||
действует со следующей молекулой пропилена с образованием тримера и т.д. Кроме того, этот втор-алкил-катион нестабилен и легко перегруппировывается:
|
|
|
|
|
|
|
|
|
CH3 |
CH3 |
|||||||||||
+ |
|
|
|
CH3 |
|
CHCH2CH=CH2 |
или CH3 |
|
CHCH=CHCH3 |
||||||||||||
|
|
|
|
|
|||||||||||||||||
CH3CHCH2CHCH3 |
|
|
+ |
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
CH3 |
|
CH3 |
|
CHCHCH2CH3 |
|
|
|
|
|||||||||||||
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
+ |
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
CH3 |
|
CHCHCH2CH3 |
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
+ |
|
|
|
|
|
|
|
|
|
|
|
|
+ |
|
|
|
|||||
CH3 |
|
CCH2CH2CH3 |
|
|
|
|
|
|
|
|
|
CH3CHCHCH2CH3 |
|||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
CH3 |
||||||
|
|
|
|
|
|
-H+ |
|
|
|
|
|
|
|
|
|
|
|
|
-H+ |
||
CH2=CCH2CH2CH3 |
|
|
|
|
|
|
|
|
|
CH3CH=CCH2CH3 |
|||||||||||
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|||||||
или CH2 |
|
C=CHCH2CH3 |
|
|
|
|
|
|
|
|
или CH2=CHCHCH2CH3 |
||||||||||
|
|
|
|
|
|
|
|
|
|||||||||||||
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
CH3 |
||||||||
