
- •Организация работы и техника безопасности.
- •Общие правила работы в лаборатории органической химии.
- •2. Меры предосторожности и оказания первой помощи при несчастных случаях.
- •2.2. Работа с легковоспламеняющимися и взрывоопасными веществами
- •Других несчастных случаях.
- •2.4.Тушение местного загорания и
- •Составления отчета.
- •Ацетат натрия метан
- •1. Номенклатура углеводородов.
- •Названия алканов и алкилов
- •2. Номенклатура соединений с функциональными группами.
- •Названия некоторых радикалов, входящих в названия
- •Лабораторная работа № I основные методы очистки органических вешеств и определение их важнейших констант.
- •Вопросы и упражнения
- •Лабораторная работа №2. Свойства алканов, алкенов, алкинов, аренов.
- •Вопросы и упражнения.
- •Лабораторная работа №. 3.
- •Лабораторная работа № 4.
- •Лабораторная работа № 5 углеводы: моносахариды и дисахариды
- •Лабораторная работа №6 пОлисахариды
- •Задачи и упражнения.
- •Лабораторная работа №7 Химические свойства аминов, нитросоединений. Синтез азокрасителей.
- •Задачи и упражнения.
- •Лабораторная работа №8 Химические свойства аминокислот и белков
- •Задачи и упражнения
- •Лабораторная работа №9 Гетероциклические соединения.
- •Вопросы и упражнения.
- •Литература
Лабораторная работа №. 3.
ХИМИЧЕСКИЕ СВОЙСТВА СПИРТОВ И ФЕНОЛОВ. .
Спиртами называются органические соединения, в состав которых входит гидроксильная группа - ОН. По числу гидроксилов, входящих в молекулу, различают одноатомные (алкоголи), двухатомные (гликоли), трехатомные (глицерины) и т. д. спирты. Одноатомные спирты имеют общую формулу R-OH, причем, в зависимости от природы радикалов, бывают предельные, непредельные и ароматические спирты. Если гидроксильная группа связана непосредственно с ароматическим кольцом, то такой спирт называется фенолом. Фенолы также могут быть одно-, двух- и многоатомные.
Свойства спиртов определяются как наличием углеродных радикалов (свойства соответствующих углеводородов), так и гидроксильной группой. В этом разделе рассматриваются только свойства гидроксильных групп. Для спиртов характерны реакции замещения только атома углерода в группе –ОН и окисления.
Например:
2СН3 –СН2 –СН2 –ОН +2К 2СН3 – СН2 –СН2 –ОК +Н2 пропиловый спирт ( Т ) пропилат калия водород 1-пропанол ( С )
С

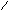


 Н3
О СН3 О
Н3
О СН3 О
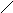


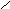 СН
– ОН + СН3
- С -Н2О
СН – О – С – СН3
СН3
ОН
СН3
СН
– ОН + СН3
- С -Н2О
СН – О – С – СН3
СН3
ОН
СН3
Изо-пропиловый спирт (Т) уксусная кислота Изо-пропилацетат
Диметилкарбинол (Р)
3СН3 –СН2 –СН(ОН)-СН3 + РCl3 3C2Н5-СН(Cl)-СН3 + Р (ОН)3 вторичный бутиловый треххлористый 2-хлорбутан ортфосфорная спирт ( Т ) фосфор кислота
При взаимодействии спиртов с металлами образуются алкоголяты, с НСl или PCl3 – галогенопроизводные, при окислении – альдегиды или кетоны. Все гликоли, глицерин, кроме того, взаимодействуют с гидроокисями двухвалентных металлов (Сu (ОН)2 , Са (ОН)2) с образованием растворимых в воде гликолятов, глицератов и т. д.
Фенолы, кроме реакции со щелочными металлами, реагирует также со щелочами с образованием фенолятов и дают яркое окрашивание при взаимодействии с хлоридом железа. Реакция с FеСl3 являются качественной пробой на гидроксил, связанный с бензольным кольцом.
ОПЫТ 12. РАСТВОРИМОСТЬ СПИРТОВ. В отдельные пробирки наливают по 0.5 мл метилового, этилового и любого из предложенных спиртов. В каждую добавляют по 0.5 мл воды и встряхивают. Каплю водного слоя из каждой пробирки наносят на лакмусовую бумагу. В пробирку с третьим спиртом добавляют раствор щелочи и встряхивают.
ОПЫТ 13. РЕАКЦИЯ ЭТИЛОВОГО СПИРТА С НАТРИЕМ.
В пробирку наливают 1 мл этилового спирта (может быть заменен на метиловый или изо-пропиловый спирт) и бросают небольшой кусочек металлического натрия. Отверстие пробирки закрывают пробкой с газоотводной трубкой и поджигают выделяющийся газ. По окончании реакции к реакционной смеси добавляют воду и наносят каплю раствора на лакмусовую бумагу.
Определяют рН среды. ОПЫТ 14. ПОЛУЧЕНИЕ ГЛИЦЕРАта меди.
В пробирку наливают 0.5мл раствора сернокислой меди и 0.5 мл. раствора гидроксида натрия. К полученному осадку добавляют глицерин по капли до растворения. Сравнивают окраску до и после реакции. ОПЫТ 15. ОКИСЛЕНИЕ СПИРТОВ ХРОМОВОЙ СМЕСЬЮ.
Окисление этилового спирта хромовою смесью. Прибавьте в пробирку 3 – 5 капель этилового спирта и добавьте 2 капли 2н. Н2SO4 и 3 капли 0.5н. бихромата калия. Полученный оранжевый раствор нагрейте над пламенем горелки до начала изменения цвета. Обычно, в течении нескольких секунд цвет раствора изменится. Определите цвет и запах раствора. Напишите уравнение реакции окисления этилового спирта хромовой смесью до альдегида.
ОПЫТ 16. ОКРАШИВАНИЕ ФЕНОЛОВ РАСТВОРОМ ХЛОРНОГО ЖЕЛЕЗА.
В разные пробирки наливают по 1мл. раствора фенола и резорцина, а затем добавляют по 1 капле раствора хлорного железа. Что наблюдается? ОПЫТ 17. КИСЛОТНЫЕ СВОЙСТВА ФЕНОЛОВ. Смесь фенола с водой (эмульсия) наливают в пробирки (1мл). Добавляют по капле раствора едкого натрия до полного растворения, к полученному прозрачному раствору добавляют несколько капель соляной кислоты. Запишите наблюдения и реакции.
ОПЫТ 18. БРОМИРОВАНИЕ ФЕНОЛА.
В пробирку с раствором фенола при постоянном взбалтывании добавьте насыщенный раствор бромной воды до образования осадка. Определите цвет осадка и напишите уравнения реакций бромирования фенола. ВОПРОСЫ И УПРАЖНЕНИЯ.
Напишите все изомеры спиртов общей формулы С4Н10О.
Напишите реакции взаимодействия вторичного бутилового спирта с натрием, с хлористым водородом.
Объясните причину понижения растворимости спиртов в воде с увеличением углеводородной части молекулы.
Напишите реакцию окисления изо-амилового спирта хромовой водой.
Напишите реакцию взаимодействия резорцина (м–диоксибензол ) с избытком КОН.
Приведите примеры реакций дегидратации этилового спирта и изо-пропилового спирта.
Назовите по ИЮПАК этил-изо-пропилкарбинол.
Назовите по ИЮПАК диметил-изо-пропилкарбинол.
Назовите по ИЮПАК изо-пропилтрет.бутилкарбонол.
Назовите по ИЮПАК диметилбутилкарбинол.
Назовите по ИЮПАК пропилвтор.бутилкарбинол.
Назовите по ИЮПАК пропилтрет.бутилкарбинол.
Назовите по ИЮПАК диэтилпропилкарбинол.
Назовите по ИЮПАК изо-пропилбутилкарбинол.
Назовите по ИЮПАК триметилкарбинол.
Назовите по ИЮПАК диметилпропилкарбинол.
Назовите по ИЮПАК метилэтилпропилкарбинол.
Назовите по ИЮПАК метилдитрет.бутилкарбинол.
Назовите по ИЮПАК метилвтор.бутилкарбинол.
Назовите по ИЮПАК дитрет.бутилкарбинол.
Назовите по ИЮПАК этилтрет.бутилкарбинол.
Предложите схемы получения этиленгликоля из этилена. С помощью какой реакции можно обнаружить образование этиленгликоля в растворе.
Предложите схему получения глицерина из пропилена.
Приведите реагенты, с помощью которых можно заменить гидроксогруппу спиртов на галоген.
Предложите схему получения бензилового спирта из ацетилена.
Какие качественные реакции на спиртовой гидроксил Вам известны? Перечислите их.
В каких условиях спирты подвергаются межмолекулярной дегидратации, в каких условиях – внутримолекулярной, какие классы органических соединений при этом образуются?
Для каких спиртов можно использовать реакцию образования йодоформа? Почему не образуют йодоформ другие спирты?
Напишите структурные формулы следующих соединений: гидроксобензол, 3-бромфенол, 2,4-динитрофенол, резорцин, пирокатехин, этоксибензол, о-крезол.
Напишите все возможные изомеры триоксибензола. Назовите их по международной и тривиальной номенклатуре.
Получите трибромфенол из хлорбензола.
Предложите схему получения резорцина из бензола.
Напишите схему поликонденсации фенола с формальдегидом в кислой среде. Как называется полученный продукт?
Получите п-крезол из п-толуидина.
Расположите в порядке убывания кислотных свойств, следующие соединения: фенол, п-нитрофенол, п-крезол, гидрохинон, пикриновая кислота.
С помощью, каких реакций можно различить следующие вещества: фенол и бензиловый спирт; фенол и бензол?
Сравните реакционную способность в реакциях нитрования бензола и фенола. Какие при этом получаются продукты реакций?
Почему замещение спиртовой группы на бром действием бромоводорода легко протекает у спиртов и практически не идет у фенолов?
Какое соединение образуется при гидрировании фенола в присутствии никелевого катализатора? Сравните химические свойства фенола и продукта реакции гидрирования.
Сравните способность к окислению о- и п- диоксибензолов с фенолом. Выведите формулы строения теоретически возможных изомеров бутилового спирта и назовите их по рациональной и международной номенклатуре. Кажите первичные, вторичные и третичные спирты.
Выведите формулы строения теоретически возможных изомеров амилового спирта и назовите их по международной номенклатуре. Укажите первичные, вторичные и третичные спирты.
Выведите формулы строения теоретически возможных изомеров двухатомного спирта, происходящего от бутана, и назовите их по международной номенклатуре.
Какой спирт получится из пропилена после присоединения к нему серной кислоты и последующего гидролиза полученного продукта?
Напишите структурные формулы следующих спиртов и назовите их по рациональной номенклатуре: а) 3-метилпентанол-3; б) 2,3-диметилбутанол-2; в) вторичный бутиловый спирт; г) 2-метилбутандиол-2,3.
Напишите структурные формулы следующих соединений: а) метилдиэтилкарбинол; б) метил-изо-пропилкарбинол; в) вторичный бутиловый спирт; г) третичный амиловый спирт; д) метилвинилкарбинол.
Назовите следующие соединения по международной номенклатуре:
а

 )
CH3
– CH – CH – CH2
– CH – CH3
)
CH3
– CH – CH – CH2
– CH – CH3
CH3 OH CH3
 CH3
CH3
б
 )
CH3
– C – CH – CH3
)
CH3
– C – CH – CH3
OH CH3
в )
CH2
= CH – CH – CH3
)
CH2
= CH – CH – CH3
OH
г )
CH3
– CH – CH2OH
)
CH3
– CH – CH2OH
CH3
137. Какие спирты образуются при гидратации следующих этиленовых углеводородов: а) пропилена, б) метилпропена, в) 3,3-диметилбутена -1? Напишите уравнения реакций и назовите полученные вещества.
Напишите уравнения реакций гидролиза водным раствором едкого натра следующих соединений: а) 2-хлорпропана; б) 2-бром-2-метилпропана, в) хлористого амила, г) 1,2-дихлорпропана.
Какие спирты можно использовать для получения следующих углеводородов: а) пропена, б) бутена-2, в) гексена – 1. Напишите уравнения реакций.
Осуществите следующие превращения:
CH4 C2H6 C3H8 C3H6 C3H6Br2 C3H6(HO)2
Какой объем этилена требуется для получения 100 кг этилового спирта?
Какой объем водорода выделится при взаимодействии 0,42 молей метилового спирта с металлическим натрием?
Получите глицерин, исходя из соответствующего галогенопроизводного углеводорода. Напишите уравнения реакции.
Напишите структурные формулы следующих соединений и назовите их по рациональной номенклатуре: а) 2-метилпантенол-3, б) 3,5-диметилгексанол-3, в) 2,2,4-триметилпентанол-3, г) 2-метил-3-этилгексанол-3, д) бутен-3-ол-2.
Напишите структурные формулы следующих соединений: а) трет.-бутиловый спирт, б) метилбутилкарбинол, в) метилэтилпропилкарбинол, г) аллиловый спирт.
Объясните, почему температура кипения бутилового спирта значительно выше, чем температура кипения диэтилового эфира, имеющего ту же формулу (брутто).
Объясните, почему температура кипения третичного бутилового спирта (82,8ºС) существенно ниже, чем температура кипения первичного бутилового спирта (117,9ºС).
Получите гидратацией соответствующих олефинов следующие спирты: а) изо-пропиловый, б) трет.бутиловый.
Гидратацией каких олефинов можно получить бутанол-2? Напишите схемы реакций.
Какие способы используют для промышленного получения метилового спирта?
Как в промышленности получают этиловый спирт? Напишите уравнения реакций.
Из каких альдегидов и кетонов при восстановлении получают: а) метил—изо-пропилкарбинол, б) пентанол -1, в) 2-этилбутанол-1?
Напишите уравнения реакций трехбромистого фосфора со следующими спиртами: а) пропиловый спирт, б) 2-метилпентанол-2.
Какие соединения могут получиться при действии на этиловый спирт концентрированной серной кислоты при различных условиях? Напишите уравнения реакций.
Напишите структурные формулы и назовите по современной международной номенклатуре: а) триметиленгликоль, б) пентаметиленгликоль.
Какие вещества могут образовываться при окислении этиленгликоля? Почему фенол не растворяется в гидрокарбонате натрия, а тринитрофенол растворяется?
Почему фенол растворяется в щелочах, но не растворяется в гидрокарбонате натрия? Какие реакции являются качественными на фенольный гидроксил и многоатомные спирты?
Сравните отношения к бромной воде фенола и бензола. Ответ объясните.
