
- •Организация работы и техника безопасности.
- •Общие правила работы в лаборатории органической химии.
- •2. Меры предосторожности и оказания первой помощи при несчастных случаях.
- •2.2. Работа с легковоспламеняющимися и взрывоопасными веществами
- •Других несчастных случаях.
- •2.4.Тушение местного загорания и
- •Составления отчета.
- •Ацетат натрия метан
- •1. Номенклатура углеводородов.
- •Названия алканов и алкилов
- •2. Номенклатура соединений с функциональными группами.
- •Названия некоторых радикалов, входящих в названия
- •Лабораторная работа № I основные методы очистки органических вешеств и определение их важнейших констант.
- •Вопросы и упражнения
- •Лабораторная работа №2. Свойства алканов, алкенов, алкинов, аренов.
- •Вопросы и упражнения.
- •Лабораторная работа №. 3.
- •Лабораторная работа № 4.
- •Лабораторная работа № 5 углеводы: моносахариды и дисахариды
- •Лабораторная работа №6 пОлисахариды
- •Задачи и упражнения.
- •Лабораторная работа №7 Химические свойства аминов, нитросоединений. Синтез азокрасителей.
- •Задачи и упражнения.
- •Лабораторная работа №8 Химические свойства аминокислот и белков
- •Задачи и упражнения
- •Лабораторная работа №9 Гетероциклические соединения.
- •Вопросы и упражнения.
- •Литература
Вопросы и упражнения
I. Какими методами пользуются для выделения и очистки органических веществ?
2. Как можно определить чистоту полученного вещества?
3. Назовите по ИЮПАК метилэтилпропилтрет.бутилметан. 4. Назовите по ИЮПАК метилдипропилвтор.бутилметан.
5. Назвать по ИЮПАК диэтил-изо-пропилметан.
6. Назвать по ИЮПАК диэтилтрет.бутилметан.
7. Назвать по ИЮПАК диметилдиэтилметан.
8. Назвать по ИЮПАК метилдиэтилтрет.бутилметан.
9. Назвать по ИЮПАК этилвтор.пропилвтор.бутилметан.
10. Назвать по ИЮПАК диметил-изо-пропилметан.
11. Назвать по ИЮПАК диметил-изо-бутилметан.
12. Назвать по ИЮПАК диметилпропил-изо-пропилметан.
13. Назвать по ИЮПАК метилпентаэтилэтан.
14.Назвать по ИЮПАК диметилбутилтрет.бутилметан.
15. Назвать по ИЮПАК этилбутилтрет.бутилметан.
16. Назвать по ИЮПАК триметил-изо-пропилметан.
17. Назвать по ИЮПАК тетраметилметан.
18. Назовите по рациональной номенклатуре 4-метилгептан.
19. Назвать по рациональной номенклатуре 3-этилоктан.
20. Назвать по ИЮПАК изо-бутилацетилен.
21. Назвать по ИЮПАК диэтилацетилен.
22. Назвать по ИЮПАК метилтрет.бутилацетилен.
23. Назвать по ИЮПАК изо-бутилтрет.бутилацетилен.
24. Назвать по ИЮПАК этилацетилен.
25. Назвать по ИЮПАК втор.бутилацетилен.
26. Назовите по рациональной номенклатуре гексин-3.
27. Назовите по ИЮПАК этилтрет.бутилацетилен.
28. Назвать по ИЮПАК изо-бутилтрет.бутилацетилен.
29. Назовите по рациональной номенклатуре бутин-1.
30. Назовите по ИЮПАК изо-пропил-изо-бутилацетилен.
31. Назвать по ИЮПАК пропил-изо-бутилацетилен.
32. Назвать по ИЮПАК ди-изо-пропилацетилен.
33. Назвать по ИЮПАК метил-изо-бутилацетилен.
34. Назвать по ИЮПАК этилвтор.бутилацетилен.
35. Назвать по рациональной номенклатуре бутен-1.
36. Назвать по ИЮПАК симм.этил-изо-пропилэтилен.
37. Назвать по ИЮПАК симм.этил-изо-пропилэтилен.
38. Назвать по ИЮПАК асимм.этил-изо-пропилэтилен.
39. Назвать по ИЮПАК втор.бутилэтилен.
40. Назвать по ИЮПАК симм.вторпропилтрет.бутилэтилен.
41. Назвать по ИЮПАК асимм.метил-изо-пропилэтилен.
42. Назвать по ИЮПАК альфа-метил-бета-этил-альфа-изо-бутилэтилен
43. Назвать по ИЮПАК асимм.метилвтор.бутилэтилен.
44. Назвать по ИЮПАК симм.втор.пропилвторбутилэтилен.
45. Назвать по ИЮПАК триметилэтилен.
46. Назвать по ИЮПАК альфа-бета-диметил-альфа-этилэтилен.
47.Назвать по ИЮПАК альфа-альфа-бета-триметил-бета-изо-пропилэтилен.
48. Назвать по ИЮПАК альфа-бета-диметилтрет.бутилэтилен.
49. Назвать по ИЮПАК симм. дитрет.бутилэтилен.
50.Назвать по ИЮПАК метилдипропилтрет.амилметан.
Лабораторная работа №2. Свойства алканов, алкенов, алкинов, аренов.
Углеводороды – вещества, состоящие из углерода и водорода. Нефть и продукты ее первичной переработки состоят из углеводородов (бензин, керосин и т. д.). Атомы углерода могут связываться между собой разными связями (одинарными, двойными и тройными), а также образовывать циклические и ароматические структуры. Углеводороды с простой, одинарной связью называются парафиновыми или алканами, с одной двойной – олефинами, этиленовыми или алкенами, а тройной – ацетиленовыми или алкинами. Ароматические углеводороды характеризуются наличием бензольного кольца. Следует отметить, что свойства углеводородов являются составной частью любой самой сложной органической молекулы. Свойства каждого класса углеводородов определяются характером связей. Для ординарных связей характерна высокая устойчивость к реагентам при комнатной и невысоких (до 100%) температурах. Двойная и тройная связь очень легко вступают в реакцию с образованием продуктов присоединения. Ароматические углеводороды при нормальной температуре устойчивы, но при незначительном нагревании (40 – 60° С) вступают в реакцию замещения. Например: При температуре не выше 100С или комнатной:
СН3 – СН2 – СН3 Н2 SO4 реакции нет
пропан серная кислота
 OSO3H
OSO3H
СН2 = СН – СН3 НОSO3Н CH3-CH-CH3
Пропилен серная кислота Сложный эфир
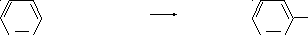
+ HOSO3H +SO3 H2O + SO3H
бензол серная кислота бензолсульфокислота
Предельные и ароматические углеводороды, в отличие от непредельных углеводородов, устойчивы к окислителям, но все углеводороды горят на воздухе.
Опыт 5. Химические свойства парафиновых углеводородов.
В три пробирке налейте по 5 капель предельного углеводорода (гексан, октан и др.) и добавить в одну – равное количество бромной воды, во вторую – столько же раствора марганцовокислого калия, в третью – концентрированной серной кислоты. Что при этом получается?
Опыт 6. Бромирование предельных углеводородов.
В две узкие маленькие пробирке налейте по 1 мл предельного углеводорода и раствора брома в четыреххлористом углеводе. Одну пробирку выставить на свет, а вторую – поместить в темное место.
Когда окраска брома в облученной светом пробирке исчезнет, сравните ее с затемненной пробиркой. В чем разница? Как влияет облучение на бромирование предельных углеводородов? Запишите в протоколы уравнение реакции бромирования гексана.
ОПЫТ 7. Получение и свойства этилена.
Выделяющийся газ этилен, полученный из смеси этилового спирта и концентрированной серной кислоты при нагревании, пропускают через бромную воду и раствор перманганата калия. Продолжающий выделяться газ поджигают. Написать уравнения реакций.
Опыт 8.Обнаружение непредельных соединений в бензине или керосине.
Налейте в одну пробирку 1мл. раствора перманганата, в другую – столько бромной воды. В каждую пробирку влейте 2 – 3 капли бензина или керосина (осторожно, огнеопасно!) и перемешайте. Что наблюдаете? Обратите внимание на удельный вес бензина. Сделайте вывод, содержатся ли во взятых образцах бензина или керосина непредельные углеводороды? Запишите результаты опыта.
Опыт 9. Получение и свойства ацетилена.
В пробирку помещают несколько кусочков карбида кальция, добавляют воды 1 – 2 мл, быстро закрывают газоотводной трубкой. Выделяющийся газ пропускают вначале через бромную воду и раствор перманганата калия, затем собирают в отдельную пробирку и поджигают. Написать уравнение реакций. Опыт 10. Свойства бензола и его гомологов. В пробирку наливают по 1 мл бензола и толуола и добавляют по 1 мл бромной воды (в одну) и раствора перманганата калия (в другую). Встряхнуть, нагревать на водяной бане (1- 2 минуты). Написать уравнение реакций.
Опыт 11. Реакция нитрования бензола или толуола.
В пробирку помещают по 0.5 мл нитрующей смеси 0.5 мл бензола или толуола. Хорошо встряхнуть и поместить в кипящую водяную баню на 5 – 10 минут. Полученный продукт реакции выливают в стаканчик с 50 мл воды и перемешивают. Обратите внимание на тяжелые капли, падающие на дно и запах «горького миндаля». Написать уравнение реакций.
