
- •Химия Учебное наглядное пособие
- •Содержание
- •Раздел 1. Основные понятия и законы химии
- •1.1. Атомно-молекулярное учение
- •1.2. Законы химии
- •Закон сохранения массы вещества
- •Способы выражения количества вещества эквивалентов
- •Раздел 2. Классификация неорганических веществ
- •2.1.Оксиды
- •Химические свойства оксидов
- •2.2. Гидроксиды металлов
- •Химические свойства гидроксидов
- •Доказательство амфотерности
- •2.3. Кислоты
- •2.4. Соли
- •Средние кислые основные
- •Получение солей
- •2.5. Комплексные соединения
- •Раздел 3. Растворы
- •3.1. Способы выражения концентрации растворов
- •3.2. Растворы неэлектролитов
- •3.3. Растворы электролитов. Электролитическая диссоциация
- •3.4. Ионно-молекулярные уравнения реакций
- •3.5. Гидролиз
- •Раздел 4. Элекрохимические системы
- •Законы Фарадея
- •4.1. Степень окисления
- •4.2. Окислительно-восстановительные реакции (овр)
- •Направление овр
- •4.3. Гальванический элемент Даниэля-Якоби
- •4.4. Электродвижущая сила (эдс)
- •Стандартный водородный электрод
- •4.5. Электролиз
- •Электролиз с инертным анодом
- •Электролиз с растворимым анодом
- •4.6. Коррозия и защита металлов от коррозии
- •Защита металлов от коррозии
- •Раздел 5. Периодический закон д.И.Менделеева
- •5.1. Строение атома
- •Состав ядра
- •5.2. Модель состояния электрона в атоме Квантовые числа
- •Возможные значения квантовых чисел
- •5.3.Основные положения строения электронных оболочек атома
- •Ряд последовательного заполнения электронами орбиталей
- •Раздел 6. Химическая связь
- •Раздел 7. Химическая кинетика и равновесие
- •Раздел 8. Химическая термодинамика
- •8.1. Параметры состояния системы
- •8.2. Закон Гесса
- •Раздел 9. Химия элементов
- •Углерод c
- •Физические свойства аллотропных модификаций c
- •Химические свойства с
- •Соединения с
- •Кремний Si
- •Соединения Si
- •Соединения n
- •Соли аммония
- •Особые химические свойства
- •Разложение нитратов: фосфор p
- •Соединения р
- •Халькогены
- •Кислород
- •Соединения s
- •Галогены f, Cl, Br, I хлор Cl2
- •Соединения Cl
- •Подгруппа хрома
- •Хром Cr
- •Подгруппа железа
- •Железо Fe
- •Раздел 10. Органическая химия
- •10.1.Углеводороды Предельные углеводороды. Алканы
- •Непредельные углеводороды. Алкены
- •Диеновые углеводороды
- •Ароматические углеводороды. Ряд бензола. Арены
- •Нефть и ее переработка
- •10.2. Кислородсодержащие органические соединения Спирты
- •Альдегиды
- •Формальдегид
- •Ацетальдегид
- •Поликонденсация
- •Кетоны r – c – r
- •Карбоновые кислоты
- •Определение строения веществ
- •11.1. Методы качественного анализа (реакции обнаружения) Окрашивание пламени (предварительная проба)
- •Реакции осаждения
- •Реакции с выделением газа
- •Качественный элементный анализ
- •Цветные реакции
- •Обнаружения газов
- •Реакции обнаружения органических соединений
- •Индентификация синтетических материалов
- •11.2. Методы количественного анализа Титриметрический анализ (объемный анализ)
- •Кондуктометрическое титрование
- •Потенциометрия
- •Окислительно-восстановительное титрование
- •Комплексонометрия
- •Осадительное титрование
- •Аргентометрия
- •Гравиметрия
- •11.3. Спектроскопические методы анализа
- •Ультрафиолетовая спектроскопия и абсорбционная спектроскопия в видимой области
- •Характерные инфракрасные полосы поглощения
- •Спектроскопия ядерного магнитного резонанса
- •11.4. Дифрактометрический метод анализа
- •Дифракция рентгеновых лучей для определения типа кристаллической решетки
- •Дифракция рентгеновых лучей для определения электронной плотности
- •Раздел 12. Химия окружающей среды Глобальные аспекты
- •Загрязнение окружающей среды
- •Охрана окружающей среды
- •Атмосфера как область окружающей среды
- •Загрязнение воздуха
- •Влияние вредных веществ на окружающую среду
- •Методы очистки воздуха
- •Гидросфера как область окружающей среды
- •Вредные примеси питьевой воды
- •Жёсткость воды
- •Сточные воды
- •Вредные вещества в сточных водах
- •Поступления сточных вод
- •Литосфера как область окружающей среды
- •Удобрения
- •Загрязнение стойкими биоцидами
- •Заражение ядовитыми тяжелыми металлами
- •Методы санации зараженных почв
- •Отходы в окружающей среде
- •Вторичное использование
- •Продовольствие и питание
- •Углеводы в качестве пищевого продукта
- •Жиры в качестве пищевого продукта
- •Протеины как продукт питания
- •Витамины
- •Минеральные вещества
- •Микроэлементы
- •Пищевые добавки
- •Консерванты
- •Раздел 13. Коллоидная химия
- •Адсорбция, ее виды
- •Дисперсные системы
- •Коллоидные растворы
- •Строение коллоидных частиц
- •Приложение а Физико-химические постоянные
- •Групповые названия химических элементов
- •Растворимость веществ в воде при температуре 25 °с
- •Эбуллиоскопические (Кэ) и криоскопические (Ккр) константы некоторых растворителей
- •Произведения растворимости некоторых малорастворимых электролитов при 25 °с
- •Возможные степени окисления элементов
- •Электронное строение атомов в основном состоянии
- •Стандартные термодинамические функции образования
- •Нормальные (стандартные) окислительно-восстановительные потенциалы е0 в водных растворах при 25 0с по отношению к нормальному водородному электроду
- •Рыбалкин Евгений Михайлович Ковалик Ольга Юрьевна химия
- •654007, Г. Новокузнецк, ул. Кирова, 42
Доказательство амфотерности
|
Доказать амфотерность – написать реакции взаимодействия с гидроксидом и кислотой.
M
M
H+2Mn+4O–23 |
2.3. Кислоты
|
Кислотами называют соединения, состоящие из одного или нескольких атомов H+ и кислотного остатка. Кислоты характеризуются кислым вкусом и способностью изменять фиолетовый цвет лакмуса на красный. Носителем кислотных свойств является гидратированный ион водорода (Н+).
HCl → Cl‾, H2S → S2–, HNO3 → NO3‾, H2SO4 → SO42– , H3PO4 → PO43–, H4SiO4 → SiO44–. Заряд кислотного остатка всегда отрицателен и равен числу атомов H в молекуле кислоты. |
|
Классификация кислот | |
|
Сильные кислоты |
Слабые кислоты |
|
HCl, HBr, HI, НNО3, H2SО4, HClO4, HMnO4 |
остальные кислоты |
|
Сила кислоты определяется константой или степенью электролитической диссоциации. | |
|
Одноосновные содержащие один атом H+ |
Многоосновные содержащие 2 и более атомов Н+ |
|
НNO3 ,HCl, HNO2, HClO4 |
Н2SO4, Н2CO3, H2S ,H2SiO3, Н3PO4, H3AsO4 |
|
Бескислородные (б/к) |
Кислородсодержащие (к/с) |
|
HCl, HBr, HI, HF, H2S |
HNO2, НNО3, H2SО4, HClO4, HMnO4, Н2CO3, H2SiO3, Н3PO4, |
|
Кислоты можно разделить на 2 группы: окислительные и неокислительные. К неокислительным кислотам относятся соляная (разбавленная и концентрированная), серная (разбавленная). Их окислительные свойства проявляются за счет иона водорода. Окислительные кислоты – серная (концентрированная), азотная (разбавленная и концентрированная). | ||||
|
Особенности взаимодействия кислот с металлами
| ||||
|
Кислота |
Концентрация |
Металлы (в порядке уменьшения активности)
| ||
|
активные Me Na-Al |
средне активные Al-Pb |
мало активные Me Pb-H2-Ag | ||
|
Соляная НСl |
разб.
|
Соль + H2 |
Соль + H2 |
– |
|
конц.
|
Соль + H2 |
Соль + H2 |
– | |
|
Серная H2SO4 |
разб.
|
Соль + H2 |
Соль + H2 |
– |
|
конц.
|
Соль+H2S+H2O |
Соль+S+H2O |
Соль+SO2+H2O | |
|
Азотная HNO3 |
разб.
|
Соль+NH4NO3+H2O |
Соль+N2+H2O |
Соль+NO+H2O |
|
конц.
|
Соль+N2+H2O |
Соль+NO2+H2O |
Соль+NO2+H2O | |
|
Фосфор наяH3PО4 |
разб. |
Соль + H2 |
Соль + H2 |
– |
|
Концентрированная азотная и серная кислоты обладают способностью пассивировать отдельные металлы (Ti, Al, Cr, Be, Mo, Bi, Co, Fe, Mg, Nb). При пассивации на поверхности металлов образуется защитная плёнка оксида, предотвращающая воздействие на них кислот.
| ||||
|
Химически активными металлами считаются металлы с электродными потенциалами Е0 < –0,4В, а химически малоактивными с Е0 > 0. Между указанными металлами находятся металлы средней активности. Значения электродных потенциалов приведены в таблице Приложения Л.
| ||||
|
Номенклатура кислот | |
|
HСlO – хлорноватистая |
ClO–– гипохлорит-ион |
|
HСlO2 – хлористая |
ClO2– – хлорит-ион |
|
HСlO3 – хлорноватая |
ClO3– – хлорат-ион |
|
HСlO4 – хлорная |
ClO4– – перхлорат-ион |
|
HСl – соляная |
Cl– – хлорид-ион |
|
HBr – бромоводородная |
Br–– бромид-ион |
|
HF – плавиковая |
F– – фторид-ион |
|
HNO2 – азотистая |
NO2– – нитрит-ион |
|
HNO3 – азотная |
NO3– – нитрат-ион |
|
HCN – синильная |
CN– – цианид-ион |
|
HMnO4 – марганцовая |
MnO4– – манганат-ион |
|
H2MnO4 – марганцовистая |
MnO42– – перманганат-ион |
|
H2СO3 – угольная |
СO32– – карбонат-ион |
|
H2SO3 – сернистая |
SO32– – сульфит-ион |
|
H2SO4 – серная |
SO42– – сульфат-ион |
|
H2S2O7 – пиросерная |
S2O72– – пиросульфат-ион |
|
H2S2O3 – тиосерная |
S2O32– – тиосульфат-ион |
|
HCrO2 – метахромистая |
CrO2–– метахромит-ион |
|
H2CrO4 – хромовая |
CrO42– – хромат-ион |
|
H2Cr2O7 – двухромовая |
Cr2O72– – бихромат-ион |
|
HPO2 – фосфорноватистая |
PO2– – гипофосфит-ион |
|
HPO3 – метафосфорная |
PO3– – метафосфат-ион |
|
H3PO4 – фосфорная |
PO43– – фосфат-ион |
|
HBO2 – метаборная |
BO2– – метаборат-ион |
|
H2B4O7 –тетраборная |
B4O72– – тетраборат-ион |
|
H3BO3 – ортоборная |
BO33– – ортоборат-ион |
|
HAlO2 – метаалюминиевая |
AlO2– – метаалюминат-ион |
|
H3AlO3 – ортоалюминиевая |
AlO33– – ортоалюминат-ион |
|
H2SiO3 – кремниевая |
SiO32– – силикат-ион |
|
H3AsO4 – мышьяковая |
AsO43– – арсенат-ион |
|
H2ZnO2 – цинковая |
ZnO22– – цинкат-ион |
|
НСООН – муравьиная |
НСОО– - формиат-ион |
|
CH3COOH – уксусная |
CH3COO– – ацетат-ион |
|
H2C2O4 – щавелевая |
C2O42– – оксалат-ион |
|
C17H35COOH – стеариновая |
C17H35COO– – стеарат-ион |

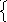 nO2
+ 2H2SO4
→ Mn(SO4)2
+ 2H2O;
nO2
+ 2H2SO4
→ Mn(SO4)2
+ 2H2O;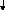 n+4O2
+ 2NaOH → Na2MnO3
+ 2H2O.
n+4O2
+ 2NaOH → Na2MnO3
+ 2H2O.