- •Химия Учебное наглядное пособие
- •Содержание
- •Раздел 1. Основные понятия и законы химии
- •1.1. Атомно-молекулярное учение
- •1.2. Законы химии
- •Закон сохранения массы вещества
- •Способы выражения количества вещества эквивалентов
- •Раздел 2. Классификация неорганических веществ
- •2.1.Оксиды
- •Химические свойства оксидов
- •2.2. Гидроксиды металлов
- •Химические свойства гидроксидов
- •Доказательство амфотерности
- •2.3. Кислоты
- •2.4. Соли
- •Средние кислые основные
- •Получение солей
- •2.5. Комплексные соединения
- •Раздел 3. Растворы
- •3.1. Способы выражения концентрации растворов
- •3.2. Растворы неэлектролитов
- •3.3. Растворы электролитов. Электролитическая диссоциация
- •3.4. Ионно-молекулярные уравнения реакций
- •3.5. Гидролиз
- •Раздел 4. Элекрохимические системы
- •Законы Фарадея
- •4.1. Степень окисления
- •4.2. Окислительно-восстановительные реакции (овр)
- •Направление овр
- •4.3. Гальванический элемент Даниэля-Якоби
- •4.4. Электродвижущая сила (эдс)
- •Стандартный водородный электрод
- •4.5. Электролиз
- •Электролиз с инертным анодом
- •Электролиз с растворимым анодом
- •4.6. Коррозия и защита металлов от коррозии
- •Защита металлов от коррозии
- •Раздел 5. Периодический закон д.И.Менделеева
- •5.1. Строение атома
- •Состав ядра
- •5.2. Модель состояния электрона в атоме Квантовые числа
- •Возможные значения квантовых чисел
- •5.3.Основные положения строения электронных оболочек атома
- •Ряд последовательного заполнения электронами орбиталей
- •Раздел 6. Химическая связь
- •Раздел 7. Химическая кинетика и равновесие
- •Раздел 8. Химическая термодинамика
- •8.1. Параметры состояния системы
- •8.2. Закон Гесса
- •Раздел 9. Химия элементов
- •Углерод c
- •Физические свойства аллотропных модификаций c
- •Химические свойства с
- •Соединения с
- •Кремний Si
- •Соединения Si
- •Соединения n
- •Соли аммония
- •Особые химические свойства
- •Разложение нитратов: фосфор p
- •Соединения р
- •Халькогены
- •Кислород
- •Соединения s
- •Галогены f, Cl, Br, I хлор Cl2
- •Соединения Cl
- •Подгруппа хрома
- •Хром Cr
- •Подгруппа железа
- •Железо Fe
- •Раздел 10. Органическая химия
- •10.1.Углеводороды Предельные углеводороды. Алканы
- •Непредельные углеводороды. Алкены
- •Диеновые углеводороды
- •Ароматические углеводороды. Ряд бензола. Арены
- •Нефть и ее переработка
- •10.2. Кислородсодержащие органические соединения Спирты
- •Альдегиды
- •Формальдегид
- •Ацетальдегид
- •Поликонденсация
- •Кетоны r – c – r
- •Карбоновые кислоты
- •Определение строения веществ
- •11.1. Методы качественного анализа (реакции обнаружения) Окрашивание пламени (предварительная проба)
- •Реакции осаждения
- •Реакции с выделением газа
- •Качественный элементный анализ
- •Цветные реакции
- •Обнаружения газов
- •Реакции обнаружения органических соединений
- •Индентификация синтетических материалов
- •11.2. Методы количественного анализа Титриметрический анализ (объемный анализ)
- •Кондуктометрическое титрование
- •Потенциометрия
- •Окислительно-восстановительное титрование
- •Комплексонометрия
- •Осадительное титрование
- •Аргентометрия
- •Гравиметрия
- •11.3. Спектроскопические методы анализа
- •Ультрафиолетовая спектроскопия и абсорбционная спектроскопия в видимой области
- •Характерные инфракрасные полосы поглощения
- •Спектроскопия ядерного магнитного резонанса
- •11.4. Дифрактометрический метод анализа
- •Дифракция рентгеновых лучей для определения типа кристаллической решетки
- •Дифракция рентгеновых лучей для определения электронной плотности
- •Раздел 12. Химия окружающей среды Глобальные аспекты
- •Загрязнение окружающей среды
- •Охрана окружающей среды
- •Атмосфера как область окружающей среды
- •Загрязнение воздуха
- •Влияние вредных веществ на окружающую среду
- •Методы очистки воздуха
- •Гидросфера как область окружающей среды
- •Вредные примеси питьевой воды
- •Жёсткость воды
- •Сточные воды
- •Вредные вещества в сточных водах
- •Поступления сточных вод
- •Литосфера как область окружающей среды
- •Удобрения
- •Загрязнение стойкими биоцидами
- •Заражение ядовитыми тяжелыми металлами
- •Методы санации зараженных почв
- •Отходы в окружающей среде
- •Вторичное использование
- •Продовольствие и питание
- •Углеводы в качестве пищевого продукта
- •Жиры в качестве пищевого продукта
- •Протеины как продукт питания
- •Витамины
- •Минеральные вещества
- •Микроэлементы
- •Пищевые добавки
- •Консерванты
- •Раздел 13. Коллоидная химия
- •Адсорбция, ее виды
- •Дисперсные системы
- •Коллоидные растворы
- •Строение коллоидных частиц
- •Приложение а Физико-химические постоянные
- •Групповые названия химических элементов
- •Растворимость веществ в воде при температуре 25 °с
- •Эбуллиоскопические (Кэ) и криоскопические (Ккр) константы некоторых растворителей
- •Произведения растворимости некоторых малорастворимых электролитов при 25 °с
- •Возможные степени окисления элементов
- •Электронное строение атомов в основном состоянии
- •Стандартные термодинамические функции образования
- •Нормальные (стандартные) окислительно-восстановительные потенциалы е0 в водных растворах при 25 0с по отношению к нормальному водородному электроду
- •Рыбалкин Евгений Михайлович Ковалик Ольга Юрьевна химия
- •654007, Г. Новокузнецк, ул. Кирова, 42
Раздел 2. Классификация неорганических веществ
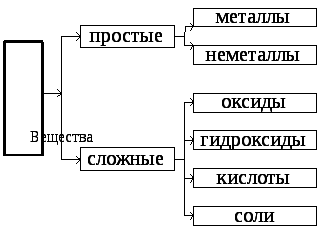
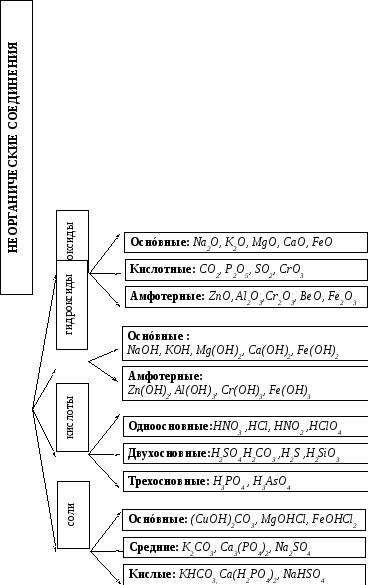
2.1.Оксиды
|
Оксиды – сложные вещества, состоящие из двух элементов, одним из которых является кислород.
| |
|
где Э – элемент, может являться металлом и неметаллом. |
|
Основные оксиды – это такие оксиды, гидратные соединения которых являются основаниями. Образуются типичными металлами и d-элементами в степени окисления +2. |
Кислотные оксиды – это такие оксиды, гидратные соединения которых являются кислотами. Образуются неметаллами и d-элементами в высшей степени окисления. |
Амфотерные оксиды – это такие оксиды, гидратными соединениями которых могут являться и основания, и кислоты. Образуются амфотерными металлами. | ||||
|
оксид |
гидратное соединение |
оксид |
гидратное соединение |
оксид |
гидратное соединение | |
|
Na2O |
NaOH |
СO2 |
H2СO3 |
ZnO |
H2ZnO2 |
Zn(OH)2 |
|
СaO |
Ca(OH)2 |
P2O5 |
H3PO4 |
Al2O3 |
HAlO2 |
Al(OH)3 |
|
FeO |
Fe(OH)2 |
СrO3 |
H2СrO4 |
Cr2O3 |
HCrO2 |
Сr(OH)3 |
Химические свойства оксидов
|
основные оксиды |
|
– основный оксид + кислота = соль + Н2О CaО + 2 НС1 = СaС12 + Н2О; – основный оксид + кислотный оксид = соль Na2O + СO2 = Na2CO3; – оксиды щелочных и щелочноземельных металлов + Н2О = основный гидроксид Na2O + Н2О = 2 NaOH; CaO + Н2О = Ca (OH)2. |
|
кислотные оксиды |
|
– кислотный оксид + гидроксид = соль + Н2О CО2 + Ca(OH)2 = Сa СO3 + Н2О; – кислотный оксид + основной оксид = соль SO2 + Na2O = Na2SO3; – кислотный оксид + Н2О = кислота CO2 + Н2О = H2СO3. |
|
амфотерные оксиды |
|
– амфотерный оксид + кислота = соль + Н2О ZnO + H2SO4 = ZnSO4 + Н2О; – амфотерный оксид + гидроксид = соль + Н2О ZnO + 2 NaOH = Na2ZnO2+ Н2О. |
2.2. Гидроксиды металлов
|
Гидроксиды – это такие вещества, которые диссоциируют в водных растворах с отщеплением аниона гидроксогруппы ОН–.
Носителем основных свойств является гидроксид-ион ОН–. |
|
Получение гидроксидов |
|
Растворимые гидроксиды получаются при взаимодействии: –. щелочных и щелочноземельных металлов с водой 2Na + 2Н2О = 2NaOH + Н2; –. оксидов щелочноземельных металлов с водой СаО + Н2О = Са(ОН)2; –. нерастворимые гидроксиды получаются при взаимодействии шелочей с растворимыми солями соответствующих металлов FeCl3 + 3 NaOH = Fe(OH)3 ↓ + 3 NaCl. |
Химические свойства гидроксидов
|
Основные гидроксиды (основания) |
|
– основный гидроксид + кислота = соль + Н2О Fе(ОН)2 + 2НС1 = FеС12 + 2Н2О; – основный гидроксид + кислотный оксид = соль + Н2О Са(ОН)2 + SO3 = CaSO4 + Н2О; – основный гидроксид + соль = другой основный гидроксид + другая соль 2 NaOH + CuSO4 = Cu(OH)2 ↓ + Na2SO4; – основный гидроксид + основный оксид ≠ NaOH + CuO ≠; – основный гидроксид + основный гидроксид ≠ Са(ОН)2 + NaOH ≠; – нерастворимые в воде гидроксиды разлагаются при нагревании Сu(ОН)2
|
|
Амфотерные гидроксиды |
|
Многие малорастворимые в воде гидроксиды проявляют двойственный химический характер, т.е. в кислой среде реагируют как основания, а в щелочной–как кислоты. Объясняют это тем, что эти молекулы способны диссоциировать по двум типам–по типу кислоты и по типу основания. |
|
К амфотерным гидроксидам относятся: Zn(ОН)2; Ве(ОН)2; Аl(ОН)3; Сr(ОН)3, Fe(OH)3, Pb(OH)2, Mn(OH)4, V(OH)3, Sn(OH)2. |
|
Молекулы Zn(ОН)2 способны диссоциировать и как основание, и как кислота.
Z
H+ + HZnO2- (по типу кислоты) – амфотерный гидроксид + кислота = соль + вода Zn(OH)2 + 2НСl = ZnСl2 + 2Н2О; Zn(OH)2 + 2Н+ = Zn2+ + 2Н2О; – амфотерный гидроксид + щелочь = комплексная соль Zn(OН)2 + 2NaОН- = Na2[Zn(OH)4] ; Zn(OН)2 + 2ОН- = [Zn(OH)4]2-; или амфотерный гидроксид + щелочь = соль + вода Zn(OН)2 + 2NaOH = Na2ZnO2 + 2H2O; Zn(OН)2 + 2ОН-= ZnO22- + 2H2O. |