
terapy / федер рекомендации / федер рекомендации / федеральные рекомендации / гематология / 04 - Лимфопролиферативные заболевания
.pdf
Протокол диагностики и лечения лимфомы Ходжкина
Приложение 1
Программы полихимиотерапии
Программа ABVD
1.Доксорубицин, 25 мг/м2 в/в струйно, дни 1 и 15.
2.Блеомицин, 10 мг/м2 в/в струйно, дни 1 и 15.
3.Винбластин, 6 мг/м2 в/в струйно, дни 1 и 15.
4.Дакарбазин, 375 мг/м2 в/в струйно, дни 1 и 15. Начало очередного курса на 29 й день.
Программа ВЕАСОРР 14
1.Циклофосфамид, 650 мг/м2 в/в, день 1.
2.Доксорубицин, 25 мг/м2 в/в, день 1.
3.Этопозид, 100 мг/м2 в/в, дни 1—3.
4.Прокарбазин, 100 мг/м2 внутрь, дни 1—7.
5.Преднизолон, 80 мг/м2 внутрь, дни 1—7.
6.Винкристин, 2 мг в/в, день 8.
7.Блеомицин, 10 мг/м2 в/в, день 8.
С9 го дня курса назначается препарат Г КСФ в дозе 5 мкг/кг в тече ние 2—3 дней.
Начало следующего курса на 15 й день.
Программа DexaBEAM
1.Дексаметазон, 8 мг 3 раза в сутки внутрь, дни 1—10.
2.Кармустин, 60 мг/м2 в/в, день 2.
3.Мелфалан, 20 мг/м2 в/в, день 3.
4.Этопозид, 250 мг/м2 в/в, дни 4—7.
5.Цитарабин, 100 мг/м2 2 раза в сутки в/в, дни 4—7.
6.Препарат Г КСФ, 300—480 мкг п/к, дни 8—12.
Программа DHAP
1.Дексаметазон, 40 мг внутрь, дни 1—4.
2.Цисплатин, 100 мг/м2 в/в (в 1000 мл физиологического раствора, непрерывное капельное введение инфузоматом в течение суток), день 1.
3.Цитарабин, 2000 мг/м2 в/в (в 1000 мл физиологического раствора в те чение суток), день 2.
* В отсутствие прокарбазина препарат заменяется на дакарбазин, 375 мг/м2 в/в в день 1.
463
Лимфопролиферативные заболевания
Приложение 2
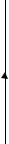 II стадия с неблагоприятными
II стадия с неблагоприятными
Лимфома Ходжкина
 I—II стадии без неблаго
I—II стадии без неблаго
факторами, III—IV стадии

приятных факторов

|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Консолиди |
рующая лучевая терапияна остаточные образова |
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
ПР |
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Клиническийэффект |
|
|
|
|
|
|
|
|
|
|
Клиническийэффект |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
14BEACOPP2x |
|
|
Рестадирование |
|
|
|
|
14BEACOPP2x |
|
|
Рестадирование |
|
|
|
|
|
|
14BEACOPP2x |
|
|
|
Рестадирование |
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ЧР |
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ПХТ2йлинии (DexaBEAM,DHAP), приэффекте— |
высокодознаятера пиясаутоТСКК |
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
Прогрессия |
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Консолидирующая |
лучеваятерапияна |
вовлеченныезоны |
до30Гр |
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
ПР |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Клиническийэффект |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Рестадирование |
|
|
|
|
|
Рестадирование |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Рестадирование |
|
|
|
|
||||||
ABVD2x |
|
|
|
|
|
|
ABVD2x |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ABVD2x |
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
ЧР |
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ПХТ2йлинии |
(DexaBEAM,DHAP), |
|
приэффекте— |
высокодознаятера |
пиясаутоТСКК |
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
Прогрессия |
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ЧР |
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
(>ния см)2
2x BEACOPP14
до 30 Гр Рестадирование
ЧР
464

Протокол диагностики и лечения лимфомы Ходжкина
Литература
1.Eichenauer DA, Engert A, Dreyling M; ESMO Guidelines Working Group. Hodgkin’s lymphoma: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow up. Ann Oncol 2011; Suppl 6:vi55–58.
2.Yahalom J. Superior vena cava syndrome. In: DeVita VT, Hellman S, Rosenberg SA eds. Cancer: Principles and Practice of Oncology. 7th ed. — Philadelphia: Lippincott Williams & Wilkins, 2005; p. 2273–2280.
3.Проценко СА, Новик АВ. Синдром верхней полой вены. Практическая онко логия 2006; № 2:108—112.
4.Bever SL, Messmann RA. Oncologic emergencies and paraneoplastic syndrome // Bethesda Handbook of Clinical Oncology. Eds. Abraham J, Allegra С. — Philadelphia: Williams & Wilkins, 2001; p. 483–493.
5.Byrne TN. Spinal cord compression from epidural metastases. New Engl J Med 1992; 327:614–619.
6.Chan RH, Dar AR, Yu E et al. Superior vena cava obstruction in small cell lung cancer. Int J Radiat Oncol Biol Phys 1997; 38:513–520.
7.Ostler PJ, Clarke DP, Watkinson AF et al. Superior vena cava obstruction: a modern management strategy. Clin Oncol 1997; 9:83–89.
8.Кравченко СК, Аль Ради ЛС, Моисеева ТН и др. Тромботические осложне ния у больных опухолями лимфатической системы. Гематология и трансфу зиология 2011; № 2:3–10.
465



Руководитель протокола |
Е. А. Никитин |
|
тел. +7 (495) 612 5583 |
|
eugene_nikitin@mail.ru |
Координационный центр |
ФГБУ ГНЦ МЗ РФ |

Протокол лечения хронического лимфолейкоза
1. Введение
Хронический лимфолейкоз (ХЛЛ) — опухоль, возникающая из лим фоцитов антигензависимых стадий дифференцировки и характеризую щаяся накоплением в кроветворной, лимфатической и других тканях опухолевых клеток с уникальным иммунофенотипом. Хронический лимфолейкоз вызывает иммунодефицит и часто осложняется развитием аутоиммунных осложнений с выработкой аутоантител, направленных против клеток крови — эритроцитов (10—20% больных), тромбоцитов (5—10% больных), эритрокариоцитов (< 1% больных) и нейтрофилов (< 1%) [1]. Другие аутоиммунные заболевания выявляются при нем не чаще, чем в общей популяции.
Течение хронического лимфолейкоза вариабельно. Около 40% паци ентов (две трети больных, имеющих стадию А в дебюте) имеют медленно прогрессирующее течение, причем продолжительность их жизни близка к общепопуляционной. У небольшой группы больных с «тлеющим» те чением ХЛЛ необходимость в лечении не возникает никогда. Наличие такой группы больных делает обоснованной тактику выжидательного наблюдения до появления показаний к терапии. До сих пор ни в одном исследовании не показано, что раннее начало терапии имеет преимуще ство по сравнению с выжидательным наблюдением.
У других пациентов наблюдается прогрессирующее течение, требую щее раннего назначения терапии. Появление пуриновых аналогов и мо ноклональных антител изменило судьбу большинства больных ХЛЛ. В ретроспективных сравнениях и рандомизированных клинических испы таниях показано увеличение продолжительности жизни пациентов с ХЛЛ [2, 3].
1.1. Развитие терапии ХЛЛ
Монотерапия
Монотерапия алкилирующими препаратами используется в тера пии ХЛЛ с середины 1950 х гг. Полвека хлорамбуцил оставался «золо тым стандартом» лечения ХЛЛ. В 1980 х гг. появились три пуриновых аналога — флударабин, пентостатин и кладрибин. Флударабин стал первым препаратом, который позволил получать качественные ремис сии при ХЛЛ. По выражению M. Keating, этот препарат совершил «бар хатную революцию» в лечении ХЛЛ. В большом межгрупповом иссле довании CALGB показано превосходство флударабина над хлорамбу цилом по частоте ремиссий и беспрогрессивной выживаемости [4]. Од нако общая выживаемость больных не изменилась. Отсутствие различий в общей выживаемости разделило гематологический мир в конце 1990 х гг. на более консервативных приверженцев хлорамбуцила и сторонников более эффективного, но и более токсичного флудараби на. Первые полагали, что интенсивность терапии ХЛЛ должна увеличи ваться по мере нарастания агрессивности болезни; другие считали, что
469

Лимфопролиферативные заболевания
в терапии первой линии должно использоваться наиболее эффективное лечение, поскольку оно позволяет достичь более длительных ремиссий и обеспечить пациенту разумное время без болезни и без лечения. В особенности остро этот вопрос дискутировался применительно к по жилым пациентам, где ожидаемая продолжительность жизни невелика, а непосредственная токсичность терапии особенно опасна. В связи с этим немецкой группой по изучению ХЛЛ было проведено исследова ние CLL5, в котором хлорамбуцил и флударабин сравнивались в группе больных старше 65 лет [5]. В этом исследовании флударабин также ока зался лучше по частоте и длительности ремиссий, но общая выживае мость в группе флударабина была хуже за счет смертей от других опухо лей, синдрома Рихтера и инфекций. В связи с этим хлорамбуцил до сих пор остается препаратом выбора в лечении пожилых больных со мно жеством сопутствующих заболеваний. Преимущества хлорамбуцила за ключаются в его низкой токсичности, низкой цене, удобстве перораль ного приема. Основной недостаток — низкая эффективность. Этот пре парат почти не вызывает полных ремиссий. При длительном использо вании хлорамбуцил может вызывать кумулятивную токсичность, миело дисплазии и вторичные лейкозы.
Более 30 лет в Германии использовался препарат бендамустин. Конец 2000 х гг. ознаменовался большим интересом к этому препарату после демонстрации его высокой эффективности у больных с хроническим лимфолейкозом и вялотекущими лимфомами. В исследовании Knauff и соавт. сравнивалась монотерапия бендамустином и хлорамбуцилом [6]. Бендамустин оказался значительно эффективнее хлорамбуцила по час тоте ремиссий (общий ответ 68% против 31%, число полных ремиссий 31% против 2%), а также по беспрогрессивной выживаемости (медиана 21,6 мес против 8,3 мес). Гематологическая токсичность 3—4 й степени чаще наблюдалась у больных, получавших бендамустин (40% против 19%). В 2008 г. монотерапия бендамустином зарегистрирована FDA как один из вариантов лечения ХЛЛ. Исследование Knauff и соавт. проводи лось без учета возраста и коморбидности. Сегодня в лечении молодых больных ХЛЛ используются комбинированные флударабин содержа щие режимы. Не показано, что комбинированная терапия с бендамусти ном превосходит комбинированные режимы с флударабином. Моноте рапия в настоящее время больше применяется у пожилых пациентов. Препараты, которые вызывают большую миелотоксичность, чем хло рамбуцил, могут не обладать преимуществом у пожилых пациентов и не заменяют старый стандарт. Поэтому роль бендамустина в терапии пер вой линии ХЛЛ пока не определена.
Другим препаратом, активно применявшимся в виде монотерапии, стал алемтузумаб — моноклональные антитела к CD52. Монотерапия алемтузумабом позволяет получить ремиссии у 33—53% больных с ХЛЛ (в том числе с рефрактерностью к флударабину) с медианой продолжи тельности ответа от 8 до 15 мес [7—10]. В исследовании Hillmen с соавт. алемтузумаб сравнивался с хлорамбуцилом [11]. Все показатели эффек тивности были выше в группе алемтузумаба — общий ответ, частота пол
470

Протокол лечения хронического лимфолейкоза
ных ремиссий, беспрогрессивная выживаемость со снижением риска прогрессии и смерти на 42%. Однако алемтузумаб вызывает глубокий иммунодефицит. Высокая токсичность этого препарата препятствует его широкому применению. В настоящее время он используется преимуще ственно для лечения больных с крайне неблагоприятным прогнозом, у которых в дальнейшем планируется трансплантация.
Комбинированная терапия
Флударабин испытывался в комбинациях с разными препаратами. В сочетании с цитарабином он оказался менее эффективен при ХЛЛ по сравнению с монотерапией [12]. Комбинация флударабина с хлорамбу цилом слишком токсична: гематологическая токсичность возрастает вдвое, а частота ремиссий остается такой же, как при монотерапии флу дарабином [4]. Имеющиеся публикации по исследованию комбинаций флударабина и антрациклинов не позволяют сделать убедительный вы вод об эффективности этого лечения [13, 14]. Лучше всего изучена и до казана эффективность при ХЛЛ комбинации FC (флударабин + цикло фосфамид). Флударабин и циклофосфамид имеют разные механизмы действия и частично не перекрещивающуюся токсичность. В исследова ниях in vitro показано, что при одновременном воздействии на клетки ХЛЛ флударабина и циклофосфамида развивается синергичный цито токсический эффект [15]. В трех крупных исследованиях продемонстри ровано, что режим FC значительно превосходит монотерапию флудара бином по эффективности [16—18] и не повышает частоту инфекций не смотря на более частое развитие нейтропении 3—4 й степени. В связи с этими результатами монотерапии флударабином больше не осталось места в лечении ХЛЛ. У молодых пациентов должны использоваться комбинированные режимы, у пожилых — хлорамбуцил.
Иммунохимиотерапия
Монотерапия ритуксимабом (моноклональные антитела к CD20) при хроническом лимфолейкозе менее эффективна, чем при других лимфомах. Поэтому монотерапия ритуксимабом как самостоятельный метод лечения используется при ХЛЛ преимущественно для лечения осложнений. Однако комбинация флударабина и ритуксимаба облада ет синергичным эффектом. Об этом свидетельствуют результаты про токола CALGB 9712, в котором ритуксимаб сочетался с флударабином последовательно или одновременно [19]. Частота ремиссий была выше в группе больных, получавших ритуксимаб и флударабин одновремен но (общий ответ 90% против 77%, полные ремиссии 47% против 28%). В первом исследовании режима FCR (флударабин, циклофосфамид, ри туксимаб) частота общего ответа составила 95%, полных ремиссий — 72%, нодулярных полных ремиссий — 10%, частичных ремиссий из за цитопений — 10% и частичных ремиссий из за минимальной остаточ ной болезни — 6% [20]. Эти результаты послужили основанием для про ведения исследования немецкой группы CLL8, в котором сравнивались режимы FC и FCR.
471

Лимфопролиферативные заболевания
В данном рандомизированном многоцентровом исследовании впер вые в истории терапии ХЛЛ продемонстировано увеличение общей вы живаемости больных [3, 21]. Основные результаты представлены в табл. 1.
Таблица 1. Ключевые результаты исследования CLL8
Показатель |
FCR |
FC |
P |
|
|
|
|
Число больных |
404 |
396 |
|
|
|
|
|
Полная ремиссия, % |
44,1 |
21,8 |
< 0,001 |
|
|
|
|
Общий ответ, % |
95,1 |
88,4 |
|
|
|
|
|
Медиана беспрогрессивной |
32,8 |
51,8 |
< 0,001 |
выживаемости, месяцы |
|
|
|
|
|
|
|
Общая выживаемость при сроке наблюде |
84,1 |
79 |
|
ния 37,7 мес, % |
|
|
|
|
|
|
|
Смерть |
65/404 (16,1%) |
86/396 (21,7%) |
|
|
|
|
|
Нейтропения, % |
33,7 |
21 |
< 0,001 |
|
|
|
|
Всовокупности эти данные показывают, что добавление ритуксимаба
крежиму FC представляет собой значительное достижение у больных ХЛЛ.
Режим FC также тестировался в сочетании с алемтузумабом (FCA) в сравнении с режимом FCR [22]. Протокол был остановлен раньше срока после промежуточного анализа первых 100 больных в связи с большей токсичностью режима FCA. Серьезные побочные эффекты развились у 44% больных в группе FCA и у 19% в группе FCR. Семь больных, получавших FCA, умерли в течение первого года от начала терапии (3 случая — ДБККЛ, 1 — мукоромикоз, 1 — септический шок, вызванный синегнойной инфекцией, 2 — сердечная недостаточность во время нейтропении). Общая частота ответов была выше (96% про тив 85%) [22].
1.2. Основные вопросы, исследуемые в протоколе
Режим FCR является наиболее эффективной терапией ХЛЛ, однако он не всегда переносится хорошо, в том числе молодыми пациентами. У части больных ремиссия достигается очень быстро. Оптимальное число циклов FCR не определено. В данном протоколе тестируется возмож ность сокращения числа циклов FCR у больных с полным ранним отве том. После 2 циклов терапии проводится промежуточная оценка ответа с оценкой остаточных клеток опухоли в крови методом проточной цито флюориметрии. Если после 2 циклов минимальная остаточная болезнь (МОБ) в крови не определяется и получена клиническая ремиссия, па циент получает еще 2 цикла FCR и снимается с протокола. Сравнивается
472
