
terapy / федер рекомендации / федер рекомендации / федеральные рекомендации / гематология / 04 - Лимфопролиферативные заболевания
.pdf
Протокол терапии лимфомы из клеток мантийной зоны у пациентов моложе 65 лет
троля используются ретроспективные данные. Это связано не только с низкой частотой данной патологии, но и со средним возрастом боль ных — около 60 лет, что исключает из исследований интенсивных режи мов терапии до 50—60% пациентов.
Высокодозную ПХТ можно разделить на три основных этапа: индук ция, консолидация и поддерживающая терапия, однако зачастую первые два этапа разделить невозможно, так как высокодозная консолидация (ауто ТСКК) может явиться методом достижения полной ремиссии за болевания.
При использовании курсов полихимиотерапии, основанных на при менении антрациклиновых антибиотиков (с ритуксимабом или без не го), медиана общей выживаемости составляет не более 4 лет, а медиана бессобытийной выживаемости — менее 2 лет. ПХТ по программе R CHOP позволяет добиться 94% общего ответа, однако достижение полной ремиссии возможно только в 34% случаев [14].
В последнее десятилетие рядом исследователей показана высокая эф фективность схем ПХТ, включающих высокие дозы цитарабина и/или метотрексата, с обязательным добавлением к терапии ритуксимаба (на пример, R Hyper CVAD/R HMA, R DHAP, CTAP/VMAC) и последую щим выполнением трансплантации аутологичных стволовых кроветвор ных клеток [15—20].
Одно из первых крупных исследований длительностью более 10 лет, включившее 97 пациентов, выполнено в M. D. Anderson Cancer Center. Схема высокодозной ПХТ по программе R HyperCVAD/R HMA пред ставлена в табл. 1.
Таблица 1. Дозы и режимы введения препаратов по программе R HyperCVAD/R HMA
1, 3, 5, 7 й курсы (R HyperCVAD) |
2, 4, 6, 8 й курсы (R HMA) |
|
|
Ритуксимаб, 375 мг/м2 в/в, день 1 |
Ритуксимаб, 375 мг/м2, день 1 |
|
|
Циклофосфан, 300 мг/м2 в/в в течение 3 ча |
Метотрексат, 1000 мг/м2 в/в постоянная |
сов, 2 введения в сутки, дни 2—4 (всего |
инфузия в течение 24 часов — первые |
6 введений) |
200 мг/м2 за 2 часа, оставшиеся 800 мг/м2 за |
|
22 часа, день 2 |
|
|
Доксорубицин, 16,6 мг/м2/сутки в/в |
Цитарабин, 3000 мг/м2 в/в инфузия в тече |
(50 мг/м2 за 3 дня), постоянная инфузия в |
ние 2 часов 2 раза в сутки, дни 3 и 4 (всего |
течение 72 часов, дни 4—7 |
4 инфузии)1 |
Винкристин, 1,4 мг/м2 в/в (максимум 2 мг), |
|
дни 5 и 12 |
|
|
|
Дексаметазон, 40 мг в/в или внутрь 1 раз в |
|
сутки, дни 2—5 и 12—17 |
|
|
|
Начало очередного курса на 29 й день, считая от начала предыдущего курса (интервал 28 дней)
1 У пациентов старше 60—65 лет или при увеличении уровня креатинина сыворотки выше 1,5 нормы доза цитарабина снижалась до 1000 мг/м2.
623

Лимфопролиферативные заболевания
Данную программу в терапии ЛКМЗ используют более 10 лет, и по следней модификацией является добавление к первой и второй частям курса ритуксимаба, что позволило увеличить частоту полных ремиссий с 38 до 84—89% (в зависимости от возраста пациента). В отсутствие полной ремиссии выполняется ауто ТСКК, в большинстве случаев с режимом кондиционирования по схеме BEAM R/BEAC R.
Пациентам старше 65 лет из за высокой токсичности доза цитараби на снижалась с 3 до 1 г/м2 (4 г/м2 на курс), что позволило косвенным об разом оценить эффективность использования разных доз препарата. Частота полных ремиссий осталась высокой — 84%, но долгосрочные ре зультаты значительно ухудшились: трехлетняя бессобытийная выживае мость снизилась с 73 до 50% [21]. При анализе долгосрочной беспрогрес сивной выживаемости наилучшие результаты были получены в группе больных, которым проводилась высокодозная ПХТ с ритуксимабом и аутологичная трансплантация стволовых клеток крови. Из 11 пациентов лишь у одного развился рецидив между вторым и восьмым годами на блюдения, то есть фактически было достигнуто плато на кривой бессо бытийной выживаемости [19].
Важным негативным моментом в исследовании эффективности схе мы R HyperCVAD/R HMA, выполненном в M. D. Andersen Cancer Cen ter, является невозможность воспроизвести его результаты. Например, в исследовании под руководством E. Epner, включавшем 49 пациентов, полная ремиссия была достигнута только у 58% пациентов (против 87% в MDACC), частичная — у 30% (общий ответ составил 88%). Двухлетняя бессобытийная выживаемость составила 63% против 73% трехлетней бессобытийной выживаемости в MDACC [22].
Одним из самых больших исследований эффективности использова ния высоких доз цитарабина и ритуксимаба в терапии ЛКМЗ, включив шим 201 пациента, является работа Nordic Lymphoma Group (NLG), чьи первые результаты были опубликованы в 2008 г. (табл. 2) [23].
Добавление к терапии высоких доз цитарабина и ритуксимаба увели чило как бессобытийную, так и общую выживаемость: при медиане на блюдения 3,8 года четырехлетняя бессобытийная выживаемость в группе MCL2 составила 63% против 18% в группе MCL1 (P < 0,0001). Это про изошло за счет сокращения процента рецидивов с 76% в группе MCL1 до 37,5% в группе MCL2. При медиане наблюдения 3,9 года четырехлетняя общая выживаемость составила 81% против 55% в группе MCL1 (P = 0,002).
Одно из наиболее значимых исследований, доказавших необходи мость использования высокодозной ПХТ с поддержкой аутологичны ми стволовыми клетками крови, выполнено European MCL network [24]. В качестве индукционной терапии у всех пациентов использовали программы CHOP, R CHOP и CHOP подобные схемы (4—6 курсов). В первую группу (n = 62) были включены пациенты, которым после ин дукционной терапии проводили мобилизующий курс ПХТ по програм ме DexaBEAM с последующим сбором аутологичных CD34+ клеток крови. Затем, после тотального облучения тела и введения высоких доз
624

Протокол терапии лимфомы из клеток мантийной зоны у пациентов моложе 65 лет
Таблица 2. Дизайн первой и второй фаз исследований Nordic Lymphoma Group
Исследование |
MCL1 1996—2000 гг. |
MCL2 2000—2006 гг. |
|
(41 пациент) |
(160 пациентов) |
|
|
|
Индукция |
MaxiCHOP1 21, три |
R2 MaxiCHOP 21/R HD AraC3 |
|
курса |
|
|
|
|
Мобилизация стволовых |
MaxiCHOP 21 |
HD AraC |
клеток |
|
|
|
|
|
Сбор и уменьшение воз |
In vitro при возможности |
In vivo: ритуксимаб в 1 й и 9 й |
можной контаминации |
|
дни курса HD AraC |
ауто СКК |
|
|
|
|
|
В случаях отсрочки сбора стволовых клеток проводились 1—2 курса терапии |
||
|
|
|
Режим |
BEAM4/BEAC5 |
BEAM4: 90 пациентов |
кондиционирования |
|
BEAC5: 55 пациентов |
Лечение при молекулярном |
Не было |
Ритуксимаб, 375 мг/м2/нед, |
рецидиве |
|
4 введения |
|
|
|
1 MaxiCHOP: циклофосфан, 1200 мг/м2, доксорубицин, 75 мг/м2, винкристин, 2 мг, преднизолон, 100 мг внутрь, дни 1—5.
2 Ритуксимаб, 375 мг/м2 в/в в первый день каждого курса, начиная с 4 го курса.
3 Цитарабин, 3 г/м2 (инфузия в течение 3 часов) в/в 2 раза в сутки 2 дня (всего 4 инфузии). У пациен тов старше 60 лет разовая доза цитарабина снижалась до 2 г/м2.
4 BEAM: кармустин (BCNU), 300 мг/м2 1 раз в 1 й день, этопозид, 100 мг/м2 2 раза в сутки в дни 2—5, цитарабин, 400 мг/м2 1 раз в сутки в дни 2—5, мелфалан, 140 мг/м2 1 раз в 6 й день.
5 BEAC: вместо мелфалана вводится циклофосфан, 1,5 г/м2 1 раз в сутки в дни 2—5.
циклофосфамида, выполняли ауто ТСКК. Второй группе пациентов после индукционной ПХТ проводили 2 курса консолидации и в даль нейшем — поддерживающую иммунотерапию интерфероном α (3 раза в неделю по 6 млн ед).
Медиана беспрогрессивной выживаемости у пациентов в первой группе составила 39 месяцев, в то время как во второй группе — всего 17 месяцев (Р = 0,0108) (табл. 3).
Таким образом, на сегодняшний день наиболее эффективной терапи ей пациентов, страдающих лимфомой из клеток мантийной зоны, явля ется использование высоких доз цитарабина (с метотрексатом или без него), ауто ТСКК (BEAM/TBI+Cy) и ритуксимаба. Эффективность поддерживающей терапии ритуксимабом в настоящее время оценивает ся во многих исследованиях, в том числе и в проспективных рандомизи рованных исследованиях MCL European Network.
В последние годы в терапии рецидивов ЛКМЗ и ее рефрактерных ва риантов оказались высокоэффективными схемы ПХТ, основанные на совместном использовании оксалиплатина и гемцитабина [27—30]. На основании этих сообщений в ГНЦ был разработан и апробирован курс ПХТ по схеме R GIDIOX (табл. 4).
625

626
Таблица 3. Результаты терапии первичных пациентов с ЛКМЗ
Автор |
Режим терапии |
Возраст, годы |
Количество |
Частота полных |
Результат |
Медиана на |
|
|
|
пациентов |
ремиссий, % |
|
блюдения, месяцы |
|
|
|
|
|
|
|
Howard [25] |
CHOPR |
31—69 |
40 |
48 |
Медиана БПВ 16,5 месяца |
25 |
|
|
|
|
|
|
|
Dreyling [24] |
CHOP/интерферон |
35—65 |
122 |
28 |
летняя3 БПВ 25% |
25 |
CALGB |
ТСККСHOP/ауто |
|
|
81 |
летняя3 БПВ 54% |
|
|
|
|
|
|||
|
(Cy/TBI) |
|
|
|
|
|
|
|
|
|
|
|
|
Evens [18] |
ТСККаутоCTAP/VMAC |
39—63 |
17 |
76 |
летняя5 БСВ 54% — у достиг |
49 |
ЗападныйСеверо |
(BuCy) |
|
|
|
ших полной ремиссии (13 из 17) |
|
университет, Чика |
|
|
|
|
|
|
го, США |
|
|
|
|
|
|
|
|
|
|
|
|
|
Khouri [15] |
HyperCVAD/HMA |
38—66 |
33 |
1001 |
летняя5 БСВ 43%. |
49 |
MDACC |
ТСККауто (Cy/TBI) |
|
|
|
летняя5 ОВ 77% |
|
|
|
|
|
|
|
|
Romaguera [12] |
HMAHyperCVAD/RR |
41—65 |
65 |
89 |
летняя3 БСВ 73% |
40 |
MDACC |
|
41—80 |
97 |
88 |
летняя3 БСВ 64% |
|
|
|
|
||||
|
|
|
|
|
|
|
Tam [19] |
HMAHyperCVAD/RR |
До 75 |
13 |
85 |
БСВ 77% при наблюдении |
68 |
MDACC |
ТСККауто BEAM)(R |
|
|
|
68 месяцев |
|
|
|
|
|
|
|
|
Geisler [23] |
ТСККаутоMaxiCHOP |
До 65 |
41 |
59 |
летняя4 БСВ 18%. |
|
NLG |
|
|
|
|
летняя4 ОВ 55% |
|
|
AraCMaxiCHOP/HD |
32—65 |
160 |
89,7 |
летняя4 БСВ 63%. |
46 |
|
ТСККауто BEAM)(R |
|
|
|
летняя4 ОВ 81% |
|
|
|
|
|
|
|
|
Gianni [26] |
HighR dose sequential |
23—65 |
28 |
100 |
летняя10 БСВ 50%. |
120 |
|
chemotherapy |
|
|
|
летняя10 ОВ 71,4% |
|
|
Mito+MelAraC(CTX |
|
|
|
|
|
|
Mel) |
|
|
|
|
|
|
|
|
|
|
|
|
БПВ — беспрогрессивная выживаемость; БСВ — бессобытийная выживаемость; ОВ — общая выживаемость.
1 Отсутствие высокочувствительных методов диагностики минимальной остаточной болезни.
заболевания Лимфопролиферативные

Протокол терапии лимфомы из клеток мантийной зоны у пациентов моложе 65 лет
Таблица 4. Схема курса полихимиотерапии GIDIOX
Препарат |
Доза и способ введения |
Дни введения |
||
|
|
|
|
|
Гемцитабин |
800 мг/м2 |
в/в 1 |
раз в сутки (разводят в 500 мл физиологи |
1 и 4 |
|
ческого раствора и вводят в течение 1,5 часа) |
|
||
|
|
|
|
|
Оксалиплатин |
120 мг/м2 |
в/в 1 |
раз (разводят в 500 мл 5% бессолевой |
2 |
|
глюкозы и вводят в течение 6 часов) |
|
||
|
|
|
|
|
Иринотекан |
100 мг/м2 |
в/в 1 |
раз (разводят в 250 мл физиологического |
3 |
|
раствора и вводят в течение 1,5 часа) |
|
||
|
|
|
||
Ифосфамид |
1000 мг/м2 в/в 1 раз в сутки (с использованием месны) |
1—5 |
||
|
|
|
||
Дексаметазон |
10 мг/м2 в/в 1 раз в сутки |
1—5 |
||
Важно отметить, что в России несколько независимых фармацевтиче ских компаний начали выпуск гемцитабина и оксалиплатина, что значи тельно снизило цены на эти препараты, в том числе на импортные аналоги.
Данный курс ПХТ по токсичности является промежуточным между курсами ПХТ по программам CHOP и HMA [12], а его выполнение в пол ных дозах возможно практически у всех пациентов в возрасте до 65 лет, причем возможно проведение 4 и более курсов, с минимальным риском развития острой почечной недостаточности.
Причиной разработки промежуточного по токсичности режима тера пии является невозможность проведения большинству пациентов в воз расте 60—65 лет (а иногда и в возрасте 55—60 лет) индукционной высоко дозной ПХТ с использованием высоких доз цитарабина и метотрексата. Несмотря на это, у пациентов старшей возрастной группы сохраняется возможность выполнения аутологичной трансплантации стволовых кроветворных клеток (BEAM R) с минимальным риском для жизни. Длительность агранулоцитоза составляет в среднем около 8 суток, вос становление количества лейкоцитов более 1,0 × 109/л происходит в сред нем на 10—12 е сутки после переливания CD34+/CD45dim клеток, что делает приемлемым выполнение ауто ТСКК в качестве одного курса консолидации.
В отделении химиотерапии гематологических заболеваний и интен сивной терапии (ХГЗиИТ) ГНЦ разработана тактика терапии пациен тов, страдающих агрессивными вариантами лимфомы из клеток мантий ной зоны, в возрасте до 65 лет. После проведения первого курса ПХТ по программе R EPOCH в стандартных дозах (табл. 5) оценивается перено симость терапии пациентами, на основании чего определяется дальней шая тактика — проведение или высокодозной ПХТ по программе R HD Met AraC (табл. 6), или среднедозной ПХТ по схеме R GIDIOX (рис. 1, табл. 4 и 7). После выполнения 3—4 циклов терапии (6—8 курсов, в зависимости от момента достижения ремиссии) проводится сбор ауто СКК с целью выполнения ауто ТСКК после кондиционирования в режиме BEAM R. Данная терапия помогает индивидуализировать лече ние в группе пациентов в возрасте от 55 до 65 лет — снизить риск смерти в связи с недооценкой статуса пациента.
627
Лимфопролиферативные заболевания
Таблица 5. Схема курса полихимиотерапии EPOCH
Препарат |
Доза и способ введения |
Дни введения |
|
|
|
|
|
Этопозид1 |
50 мг/м2 |
в сутки в/в — круглосуточное введение |
1—4 |
|
|
|
|
Доксорубицин1 |
10 мг/м2 |
в сутки в/в — круглосуточное введение |
1—4 |
Винкристин |
0,5 мг в сутки в/в — круглосуточное введение |
1—4 |
|
|
|
|
|
Преднизолон |
60 мг/м2 |
в сутки внутрь |
1—5 |
|
|
|
|
Циклофосфамид1 |
750 мг/м2 в/в 1 раз |
5 |
|
1 В зависимости от переносимости предыдущего курса дозы препаратов увеличиваются или умень шаются на 20%. Этопозид, винкристин и доксорубицин разводят вместе в одном флаконе в 500—1000 мл физиологического раствора.
Таблица 6. Схема курса полихимиотерапии HD Met AraC (HMA, high dose methotrexate and cytarabine)
Препарат |
Доза и способ введения |
Дни введения |
|
|
|
Метотрексат |
1000 мг/м2 в/в, постоянная инфузия в течение 24 ча |
1 |
|
сов — первые 200 мг/м2 за 2 часа, оставшиеся |
|
|
800 мг/м2 за 22 часа |
|
Цитарабин |
3000 мг/м2 в/в, инфузия в течение 2 часов 2 раза в |
2—3 |
|
сутки |
(4 введения) |
|
|
|
Хорошая |
ь |
|
|
||
перено |
симост |
|
|
|
|
R EPOCH
R HMA 
 R EPOCH/R HMA № 2—3
R EPOCH/R HMA № 2—3
R
R Сбор 
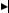 BEAM
BEAM 

 Ауто ТСКК
Ауто ТСКК 
 R — Поддержка
R — Поддержка
переносимоНедостаточная сть
 R GIDIOX
R GIDIOX

 R EPOCH/R GIDIOX ? 2—3
R EPOCH/R GIDIOX ? 2—3
Рисунок 1. Тактика терапии агрессивных форм ЛКМЗ.
К марту 2012 г. в протокол были включены 27 пациентов, индукцион ная терапия и аутологичная трансплантация стволовых кроветворных клеток выполнены у 22 пациентов. Один пациент 60 лет скончался в ре зультате развития острой почечной недостаточности и септического шо ка после курса ПХТ по схеме R HMA в связи с недостаточной оценкой его статуса после первого курса ПХТ по схеме R EPOCH (фактическое развитие агранулоцитоза при общем количестве лейкоцитов 12 × 109/л). Высокодозная терапия по схеме R EPOCH/R HMA и ауто ТСКК вы полнены 12 пациентам. Полная ремиссия достигнута у всех 12 пациен тов, у двоих пациентов развились ранние рецидивы. Медиана наблюде ния после выполнения ауто ТСКК составляет 18 месяцев. Среднедозная
628

Протокол терапии лимфомы из клеток мантийной зоны у пациентов моложе 65 лет
терапия по схеме R EPOCH/R GIDIOX и ауто ТСКК выполнены в пол ном объеме у 10 пациентов. У 9 пациентов из 10 достигнута полная ре миссия. У пациентки с частичной ремиссией заболевания беспрогрес сивная выживаемость составляет 20 месяцев. У одного пациента с пол ной ремиссией развился ранний рецидив через 8 месяцев после заверше ния терапии. Медиана наблюдения составляет 26 месяцев.
Протокол терапии пациентов с ЛКМЗ моложе 65 лет
сиспользованием альтернирующих курсов ПХТ по программам R EPOCH/R GIDIOX
и R EPOCH/R HMA с последующим выполнением высокодозного курса ПХТ по программе BEAM R
споддержкой аутологичными стволовыми кроветворными клетками
Курс R EPOCH фактически является «инфузионным» вариантом курса R CHOP E, токсичность которого не превышает токсичность схе мы CHOP, однако в связи с постоянным внутривенным введением в те чение 96 часов доксорубицина, винкристина и этопозида результаты те рапии улучшаются [32].
Критерии эффективности терапии при лимфоме из клеток мантийной зоны (Revised Response Criteria for Malignant Lymphoma, 2007) [31]
Полная ремиссия — CR
Полная ремиссия недоказанная — CRu (unconfirmed) Частичная ремиссия — PR
Стабилизация — SD Рецидив — RD Прогрессирование — PD
Полная ремиссия
Отсутствие проявлений болезни (клинически и по данным обследо вания).
Отсутствие обусловленных болезнью В симптомов (снижение массы тела, повышенное потоотделение, выраженная общая слабость, по вышение температуры тела без видимых очагов инфекции), нормали зация уровня ЛДГ.
Сокращение размеров лимфоузлов и конгломератов лимфоузлов до «нормальных»: при исходных размерах более 1,5 см сокращение до 1,5 см, при исходных размерах более 1,1—1,5 см — сокращение до 1,0 см (или более чем на 75% общей массы).
Уменьшение размеров всех ранее увеличенных органов.
629

Лимфопролиферативные заболевания
Отсутствие специфического поражения костного мозга при повтор ном исследовании биоптата/аспирата костного мозга с использова нием высокочувствительных методов диагностики.
Отсутствие поражения ЖКТ, в том числе по данным гистологическо го исследования биоптатов слизистых.
Отсутствие очагов повышенного накопления радиофармпрепарата при ПЭТ.
Полная ремиссия недоказанная
Отсутствие признаков болезни, определяемых клинически и объек тивными методами обследования.
Остаточные лимфоузлы размером 1,5 см в максимальном диаметре должны быть результатом регрессии более чем на 75%.
Конгломераты лимфоузлов должны сократиться более чем на 75% (сокращение объема опухолевой массы).
Уменьшение размеров всех ранее увеличенных органов.
Данные исследования костного мозга интерпретируются как «неоп ределенные».
Частичная ремиссия
Уменьшение объема опухоли одной из локализаций более чем на 50% и/или отсутствие костномозговой ремиссии по данным исследования трепанобиоптата.
Отсутствие увеличения размеров других лимфоузлов и ранее увели ченных органов.
Отсутствие новых признаков болезни.
Основные методы оценки полноты достижения ремиссии — КТ, УЗИ, исследование костного мозга с использованием высокочувстви тельных методов диагностики (проточная цитофлюориметрия, опреде ление В клеточной клональности методом ПЦР на основании анализа перестроек генов тяжелых цепей иммуноглобулинов, использование па циент специфичных праймеров). В сложных случаях предполагается (не строго обязательно) проведение ПЭТ.
Отбор больных на лечение по протоколу
На лечение по протоколу принимаются пациенты в возрасте от 18 до 65 лет (64 года и 11 месяцев) с цитогенетически доказанной лимфомой из клеток мантийной зоны, которым до включения в протокол было прове дено не более 2 курсов ПХТ по CHOP подобным схемам.
Лабораторные и инструментальные исследования до начала терапии
1.Общий анализ крови (ретикулоциты + тромбоциты).
2.Биохимический анализ крови (в том числе ЛДГ, АЛТ, АСТ, ЩФ, глюкоза).
630

Протокол терапии лимфомы из клеток мантийной зоны у пациентов моложе 65 лет
3.Общий анализ мочи.
4.Проба Реберга, определение клиренса креатинина.
5.Коагулограмма.
6.Определение маркеров вирусных гепатитов В и С, ВИЧ инфекции.
7.ЭКГ.
8.Гистологическое и иммуногистохимическое исследования лимфати ческого узла или другой ткани опухоли с обязательным определением экспрессии следующих антигенов: CD5, CD10, CD19, CD20, CD23, cyclin D1 и Ki 67, при возможности SOX 11. Возможно выполнение иммунологического исследования методом проточной цитофлюори метрии клеток костного мозга, крови или лимфоузла.
9.Выполнение цитогенетического исследования в клетках лимфоузла, другой ткани опухоли или костного мозга/крови для выявления t(11;14)(q13;q32). При невозможности выполнения стандартного ци тогенетического исследования целесообразно определение t(11;14)(q13;q32) методом FISH на отпечатках лимфоузла (опухоле вой ткани). Возможно выполнение цитогенетического исследования методом FISH на срезах с парафиновых блоков в кариологической ла боратории ФГБУ ГНЦ МЗиСР РФ (г. Москва, Новый Зыковский проезд, дом 4, заведующая д. м. н. Е. В. Домрачева).
10.Трепанобиопсия костного мозга (билатеральная) с выполнением им муногистохимического исследования (CD5, CD19, cyclin D1).
11.Пункция и получение аспирата костного мозга (определение вовле чения костного мозга при отсутствии гистологических признаков; при необходимости — выполнение генетического исследования на наличие t(11;14)(q13;q32) в клетках костного мозга с целью генетиче ского подтверждения диагноза; при достаточном количестве опухо левых клеток в крови возможно выполнение цитогенетического ис следования с использованием мононуклеаров крови).
12.УЗИ органов брюшной полости (печень, селезенка, поджелудочная железа, желчный пузырь, лимфатические узлы, почки, при необходи мости — мягкие ткани), средостения, периферических лимфоузлов, щитовидной железы, у мужчин — предстательной железы, у жен щин — малого таза.
13.Эхокардиография.
14.КТ органов грудной клетки и брюшной полости, при вовлечении па ренхиматозных органов — с внутривенным контрастированием, до лечения и на момент констатации ремиссии.
15.Выполнение люмбальной пункции для исключения нейролейкемии.
16.Эзофагогастродуоденоскопия и фиброколоноскопия с обязательным выполнением слепых биопсий слизистых, даже при отсутствии визу альных признаков вовлечения ЖКТ.
17.Иммунохимическое исследование белков сыворотки и мочи. Анализы крови и мочи, ЭКГ (пункты 1—7, 17) необходимо выполнить
не позднее чем за две недели до начала терапии; УЗИ и КТ органов груд ной клетки, брюшной полости, ЭГДС и ФКС — не позднее чем за месяц до начала терапии; гистологическое, иммуногистохимическое, цитоге
631

Лимфопролиферативные заболевания
нетическое и молекулярные исследования костного мозга, лимфоузла и слизистых ЖКТ — не позднее двух месяцев до начала терапии.
Противопоказания к принятию больного на лечение по протоколу
1.Возраст 65 и старше.
2.Застойная сердечная недостаточность; нестабильная стенокардия; нарушения ритма и проводимости, не поддающиеся медикаментоз ной коррекции; инфаркт миокарда, перенесенный в последние 6 ме сяцев.
3.Тяжелая пневмония, туберкулез, инвазивный аспергиллез.
4.Почечная недостаточность (уровень сывороточного креатинина бо лее 150 мкмоль/л), за исключением случаев, обусловленных лимфо идной инфильтрацией почек, и синдрома распада опухоли.
5.Печеночная недостаточность (за исключением случаев, обусловлен ных лейкемической/лимфоидной инфильтрацией органа), острый гепатит (уровень сывороточного билирубина более 2 норм, актив
ность АЛТ и АСТ более 4 норм, протромбиновый индекс менее 50%). 6. Декомпенсированный сахарный диабет (глюкоза крови выше
15 ммоль/л).
7.Сепсис (септикопиемические очаги, нестабильность гемодинамики; неэффективность антимикробной терапии).
8.Угрожающие жизни кровотечения, за исключением кровотечений из ЖКТ, обусловленных опухолевым процессом.
9.Тяжелые психические нарушения (шизофрения, тяжелый депрессив ный синдром и другая продуктивная симптоматика).
10.Физическая несостоятельность, требующая постоянного ухода; ка хексия (уровень общего белка ниже 35 г/л).
11.Другие сопутствующие онкологические заболевания вне ремиссии.
12.Выявление ВИЧ.
13.Беременность, кормление грудью.
14.Нейролейкемия.
При купировании инфекционных осложнений, декомпенсированно
го сахарного диабета, геморрагических осложнений возможно проведе ние терапии по протоколу.
Алгоритм ведения первичных больных с ЛКМЗ
1.Всем пациентам проводится первый курс ПХТ по программе R EPOCH. В зависимости от переносимости, а именно от степени миелосупрессии, определяется дальнейшая тактика терапии. При лейкопении 3 й степени длительностью более 3 дней или лейкопении 4 й степени пациентам в дальнейшем проводится терапия альтерни рующими курсами по схеме R EPOCH/R GIDIOX. При удовлетво рительной переносимости, отсутствии значимой миелосупрессии и значимых инфекционных осложнений пациентам в дальнейшем про водится терапия по схеме R EPOCH/R HMA (как правило, всем па
632
