
С.А. Мазунин, Г.С. Посягин ОСНОВЫ ФИЗИКО-ХИМИЧЕСКОГО АНАЛИЗА Часть 2. 1999г
..pdf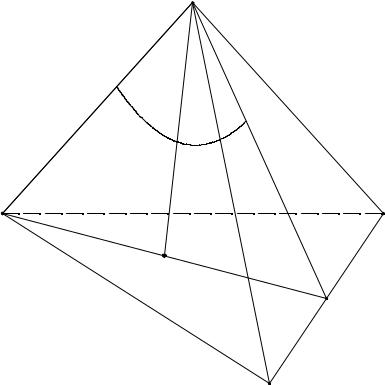
21
D
L
N
 M
M
A C
M'
N' |
B
Рис. 1. 4. Перспективная проекция на грань тетраэдра
Необходимо обратить внимание на одну важную особенность таких проекций: кривая LMN, лежащая в плоскости, проходящей через центр проекций, изображается прямой AM'N'.
Если фигуративная точка М задана соответствующими ей процентными концентрациями a, b, c, d, то не трудно определить координаты ее проекции (a', b',
c') по следующим формулам (%): |
|
a' = 100a/(a+b+c) , |
(1. 13) |
b' = 100b/(a+b+c) , |
(1. 14) |
c' = 100c/(a+b+c) . |
(1. 15) |
2. ОСНОВНЫЕ ТИПЫ ИЗОТЕРМ РАСТВОРИМОСТИ ПРОСТЫХ ЧЕТВЕРНЫХ СИСТЕМ
Применение правила фаз к простым четверным системам позволяет сделать следующие выводы. При постоянных давлении и температуре (изобара и изотерма) система будет нонвариантной при равновесии четырех фаз (В = 4-4+0 = 0), моновариантной - при равновесии трех фаз (В = 4-3+0 = 1), дивариантной - при двухфазном равновесии (В = 4-2+0 = 2), однофазные равновесия являются трива-
риантными (В = 4-1+0= 3).
22
2. 1. Принципиальная схема изотермы и изобары растворимости одного твердого вещества в смеси трех растворителей, неограниченно
смешивающихся друг с другом
Рассмотрим диаграмму растворимости одного твердого компонента А в смеси трех жидкостей В, С и D, смешивающихся во всех отношениях друг с другом, причем эта смесь является индифферентным растворителем. Для изображения изотермы растворимости этой системы воспользуемся обычной тетраэдрической диаграммой, показанной на рис. 2. 1.
Фигуративные точки чистых растворителей В, С и D примем за вершины основания тетраэдра, а фигуративную точку растворяемого компонента А - за его верхнюю вершину. Нанесем на соответствующих сторонах тетраэдра точки, отвечающие концентрациям насыщенных растворов вещества А в чистых растворителях (точки b, c, d), а также экспериментальные точки по растворимости компонента А в различных смешанных растворителях, располагающихся на грани BCD (на рис. 2. 1 они не обозначены). Проведя через эти точки плавную поверхность bcd, получим изотерму растворимости.
На рис. 2. 1 точки b, c и d отвечают растворимости вещества А в чистых растворителях, кривые bc, bd и cd – его растворимости в двойных смесях В+С, B+D, C+D, и, наконец, поверхность bcd – растворимости в тройных смесях B+C+D. Пространство BCDdbcB является геометрическим образом ненасыщенных растворов, объем AbcdA отвечает двухфазному равновесию кристаллов компонента А и насыщенному относительно него раствору.
Если фигуративная точка М исходной реакционной смеси попадает в пространство AbcdA, то система распадается на кристаллы А и насыщенный раствор, состав которого можно определить, соединив точку М с вершиной тетраэдра А и продолжив ее до пересечения с поверхностью bcd. Точка пересечения M' и дает искомый состав насыщенного раствора. Если продолжить эту прямую до пересечения с гранью тетраэдра BCD, то полученная точка M'' покажет состав растворителя, отвечающему этому раствору.
Отношение масс кристаллов А и насыщенного раствора равно по правилу рычага отношению длин отрезков MM' и AM.
2.2. Принципиальная схема изотермы и изобары растворимости двух твердых веществ в смеси двух растворителей, неограниченно
смешивающихся друг с другом
Рассмотрим теперь изотерму растворимости для случая, когда два твердых компонента А и В растворяются в двойной смеси жидкостей C и D при температуре более низкой, чем эвтектическая температура системы А - В (рис.2.2), все пространство тетраэдра распадается на четыре объема: объем Cc'cc''d''dd'DC отвечает ненасыщенным растворам; объем Acdd''c''A - смесям растворов, насыщенных А, но не насыщенных В, с кристаллами А; объем Bcdd'c'B - смесям растворов, насыщенных В, но не насыщенных А, с кристаллами В; наконец, объем AcBdA отвечает смесям растворов, насыщенных веществами А и В, с кристаллами обоих этих
23
веществ. Кроме того, если имеют дело с метастабильными состояниями, то три последних объема отвечают соответствующим перенасыщенным растворам.
A
b M·
d
M'·
c
B D
M"·
C |
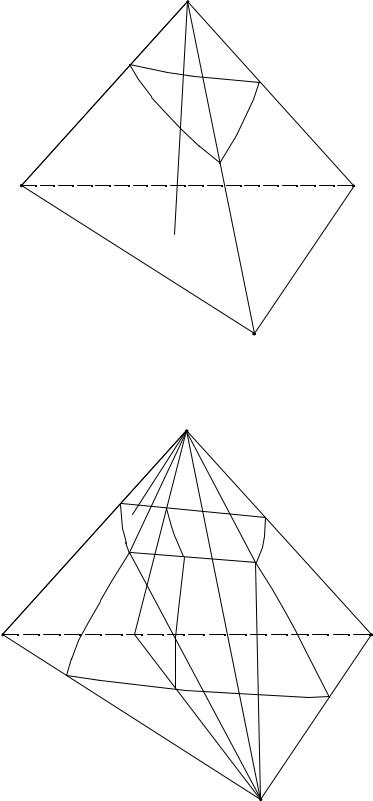
Рис. 2. 1. Изотерма и изобара растворимости четверной системы, образованной твердым компонентом А и тремя жидкостями В, С и D
|
|
A |
|
c" |
M · |
f" |
|
· |
d" |
||
|
M' |
|
|
|
|
|
c
f d
C |
F |
|
D |
|
c' |
f' |
|
|
|
d' |
|
|
|
|
B
Рис. 2. 2. Изотерма и изобара растворимости четверной системы, образованной твердыми компонентом А и В с двумя жидкостями С и D
24
На гранях тетраэдра АВС и АBD мы видим изотермы систем, образованных компонентами А, В и жидкостью С, с одной стороны, и этой же парой с жидкостью D - с другой. Это две оконтуривающие тройные системы простого эвтонического типа, и на указанных гранях мы видим соответствующие изотермы растворимости c''cc' и d''dd' с эвтониками c и d.
Поверхности cdd''c''c и cdd'c'c отвечают четверным растворам, насыщенным одним веществом ( первая - компонентом А и вторая - компонентом В), и называется поверхностями растворимости соответственно компонентов А и В.
Если надо получить изотерму совместной растворимости компонентов А и B в определенной смеси C и D, например в смеси, отвечающей точке F, то через эту точку и вершины тетраэдра А и В следует провести плоскость AFB. Пересечение ее с поверхностями растворимости А и В и даст искомую изотерму f'ff'' с эвтонической точкой f.
Так как на линии cd пересечения поверхностей растворимости лежат все эвтонические точки f систем, образованных компонентами А и В со смесями C и D, то назовем эту линию эвтонической линией. Линия cd не пересекается с ребром тетраэдра АВ, а лежит за ним.
Если фигуративная точка системы попадает в один из объемов, отвечающих смесям твердого вещества с его насыщенным раствором, то система распадается на смесь этого вещества с соответствующим раствором. Пусть фигуративная точка системы М попадает в объем кристаллизации компонента А (рис. 2. 2).Соединим точку М с А прямой и продолжим ее до пересечения с поверхностью cdd''c''с в точке М'. В этом случае наша система распадается на кристаллы твердого вещества А и раствор с фигуративной точкой М'. Количество обеих фаз может быть определено по правилу рычага.
2.3. Принципиальная схема изотермы и изобары растворимости трех твердых веществ в одном растворителе с кристаллизацией чистых компо-
нентов
Четверные системы, образованные тремя твердыми веществами (чаще всего солями с общим ионом) и жидкостью (обычно водой), имеют большое практическое значение. Поэтому мы опишем эти диаграммы подробнее.
На рис. 2.3 изображена изотермическая диаграмма растворимости системы, образованной веществами А, В, С, например тремя солями с одним общим ионом, и растворителем D, например водой.
На боковых гранях нашего тетраэдра показаны тройные системы, образованные двумя из данных веществ, с одной стороны, и растворителем - с другой; точки a, b, c дают растворимость отдельно взятых веществ А, В, С в растворителе D, точки Е1, Е2, Е3 - эвтоники тройных систем. Внутри тетраэдра мы видим: поверхности аЕ1ЕЕ3a, bЕ1ЕЕ2b и сЕ2ЕЕ3c, отвечающие четверным растворам, насыщенным одним веществом; так называемые эвтонические линии Е1Е, Е2Е, Е3Е, отвечающие четверным растворам, насыщенным двумя веществами; точку Е - эвтоники, отвечающую раствору, насыщенному тремя веществами.
25
Не представляет труда применить правило фаз к нашей системе и доказать соответствие геометрических образов в комплексе фаз; поверхность отвечает равновесию с раствором двух твердых фаз, линия - трех, а точка - четырех фаз. Применяя правило фаз, не следует забывать отмеченные ранее ограничительные условия: температура и давление принимаются постоянными.
Укажем еще, что часть тетраэдра DaE1bE2cE3E, ограниченная его боковыми гранями и упомянутыми тремя поверхностями дивариантных равновесий, образует объем или область ненасыщенных растворов.
Три части тетраэдра аЕ1ЕЕ3А, bE1EE2B и сЕ2ЕЕ3С (каждая из которых ограничена одной из указанных поверхностей соответствующим двугранным углом тетраэдра и коническими поверхностями с направляющими - эвтоническими линиями и вершинами - А, В или С) отвечают смесям однонасыщенных растворов, т. е. растворов, насыщенных одним веществом, и одному из твердых веществ А, В, С.
D
|
M |
|
c |
a |
E3 |
b |
|
M' |
|
E2 |
|
M'' |
|
||
|
|
||
E1 |
E |
|
|
A C
B |
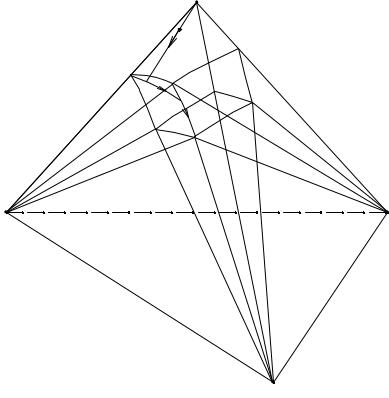
Рис. 2. 3. Изотерма и изобара растворимости четверной системы, образованной тремя твердыми компонентами А, В, С и одним жидким D
Три части тетраэдра Е1ЕАВ, Е2ЕВС и Е3ЕСА, ограниченные соответственно гранями тетраэдра, указанными выше коническими поверхностями и плоскостями ЕАВ, ЕВС и ЕАС, проведенными через стороны основания тетраэдра АВ, ВС, СА и эвтонику Е, отвечают смесям двояконасыщенных растворов, т. е. растворам, насыщенным одновременно двумя веществами, и смесям двух из трех твердых веществ А, В, С.
26
Наконец, только что указанные плоскости ЕАВ, ЕВС, ЕАС вместе с основанием тетраэдра АВС образуют пирамиду АВСЕ, объем которой отвечает области смесей эвтонического раствора, одновременно насыщенного тремя веществами (трояконасыщенный раствор), с твердыми А, В и С.
Посмотрим, как изображается на только что рассмотренной диаграмме процесс изотермического (и изобарического) испарения. Для этого вновь обратимся к рис. 2. 3.
Пусть состав исходного ненасыщенного раствора дается точкой М. При изотермическом испарении сначала удаляется только один растворитель, поэтому фигуративная точка раствора будет двигаться по прямой, соединяющей точки М и D, удаляясь от D. В конце концов указанная фигуративная точка попадает на одну из трех поверхностей, отвечающих однонасыщенным растворам, и с этого момента начинается кристаллизация одного из трех растворенных веществ.
Вданном случае эта точка попадает на поверхность аЕ1ЕЕ3 (точка М'), т. е. при дальнейшем испарении будет происходить кристаллизация вещества А. Теперь фигуративная точка нашего раствора должна оставаться на этой поверхности, а с другой стороны, так как вещества В и С пока еще не выделяются, она должна находиться и в плоскости, проходящей через ребро тетраэдра AD и, конечно, через точку М'. Таким образом, наша фигуративная точка должна двигаться по кривой пересечения указанной выше поверхности с этой плоскостью, так как при своем движении она должна одновременно находиться на обеих этих поверхностях, т. е. на линии М'M'', удаляясь от ребра AD и приближаясь к одной из эвтонических линий.
Легко видеть, что все пути кристаллизации в поле аЕ1ЕЕ3 пройдут через точку а, лежащую на ребре AD. Такая точка, из которой выходят все пути кристаллизации данного поля, называется его полюсом. Эта точка лежит на соответствующем ребре тетраэдра. Наконец, фигуративная точка раствора попадает на соответствующую эвтоническую линию, после чего она будет двигаться по этой линии и начнется совместная кристаллизация двух веществ.
Внашем случае фигуративная точка раствора попадает на линию Е3Е (точка М'') и, таким образом, при продолжающемся испарении вещества А и С будут кристаллизоваться совместно. Затем, по достижении нашей фигуративной точки Е
-эвтоники четверной системы, начнется совместная кристаллизация всех трех растворенных веществ А, В, С, которая будет продолжаться до полного высыхания раствора. Во время эвтонической кристаллизации состав раствора остается неизменным (условно-нонвариантное равновесие). Эвтонический раствор обладает наибольшей концентрацией и вследствие этого наименьшим давлением пара.
Перейдем теперь к изучению проекций только что разобранной диаграммы. На рис. 2. 4 изображена ортогональная проекция изотермы растворимости на солевое основание тетраэдра состава.
На ортогональной проекции изотермы растворимости мы видим следующие элементы: a, b, c - проекции точек, отвечающих составам однонасыщенных растворов чистых солевых компонентов; E1E, E2E, E3E - проекции линий двойного
27
насыщения относительно соответствующих пар солей; aE1EE3a - поле кристаллизации компонента А; bE1EE2b - поле кристаллизации компонента B; cE2EE3c - поле кристаллизации компонента C; Е - проекция состава трояконасыщенного эвтонического раствора.
Надо заметить, что поверхности однонасыщенных растворов, вообще говоря, кривые; поэтому пути кристаллизации на них, представляющие собой пересечение этих кривых поверхностей некоторыми плоскостями (кроме одной, перпендикулярной к основанию АВС), тоже будут кривыми. При описанном выше проецировании мы получим проекции путей кристаллизации тоже в виде кривых линий, что представляет большое неудобство.
E1 |
E |
a
E3 |
B
b
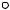 E2
E2
D |
c |
0 |
20 |
40 |
60 |
80 |
100 |
A |
|
|
|
|
C |
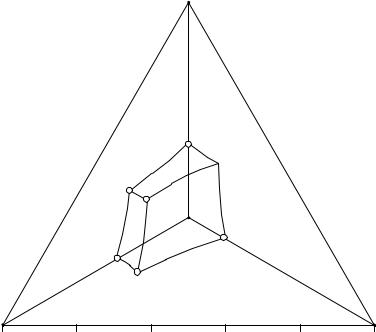
Рис. 2. 4. Ортогональная проекция изотермы растворимости системы А - В - С - H2O на солевое основание
Для решения большинства задач относительно растворимости в четверной системе обычно вполне достаточно одной проекции на основании тетраэдра. Поэтому мы не рассматриваем проекции на другие грани его.
Перейдем теперь к описанию перспективной проекции из точки, отвечающей чистому растворителю D. На рис. 2. 5 показан вид диаграммы с центральной проекцией из вершины, отвечающей растворителю, а на рис. 2. 6 изображена сама эта проекция.
Так как пути кристаллизации на поверхностях однонасыщенных растворов лежат в плоскостях, проходящих через одно из трех ребер тетраэдра DA, DB или DC, то эти пути проецируются здесь в виде прямых. Они показаны на рис. 2.6

28
стрелками, указывающими ход фигуративных точек растворов при изотермическом испарении. Это является большим преимуществом центральной проекции.
D
a |
|
c |
|
|
|
E3 |
b |
|
E1 |
|
E2 |
|
E |
|
|
|
|
E3' |
|
|
A |
|
C |
E1' |
E' |
E2' |
B
Рис. 2. 5. Построение перспективной проекции диаграммы растворимости четверной системы простого эвтонического типа
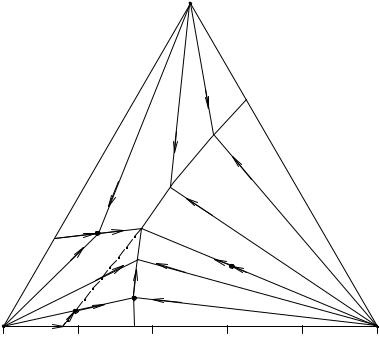
Проследим для примера, пользуясь этой проекцией, испарение раствора, характеризующегося фигуративной точкой М. Так как эта фигуративная точка попадает в поле АЕ1'Е'Е3'A, то первым начинает кристаллизоваться компонент А. При этом фигуративная точка раствора движется по прямой АМ1 от М к М1. По достижении М1 начинается совместная кристаллизация компонентов А и В, причем фигуративная точка раствора движется по кривой Е1'Е' от точки М1 к эвтонической точке Е', а суммарный состав твердой фазы (точка твердой фазы) - от точки А до точки М2 на стороне АВ. Наконец, по достижении последней точки E' происходит окончательное высыхание раствора. При этом состав раствора и давление его пара остаются неизменными до полного улетучивания растворителя и из него одновременно кристаллизуются все три вещества А, В и С, количества которых выделяются из раствора в этой последней стадии в том же отношении, в каком они находятся в эвтоническом растворе, а суммарный состав твердой фазы меняется по прямой М2Е' от точки М2 до точки М. Когда фигуративная точка твердой фазы приходит в М, исчезает последняя капля эвтонического раствора.
Если исходный раствор находится на одной из нод АЕ', СЕ' или ВЕ' (точка N), то после первичной кристаллизации (компонент В, суммарный состав твердой фазы также равен В) сразу начинается третичная кристаллизация эвтонического
29
раствора, суммарный состав твердой фазы при этом меняется по прямой ВЕ' от точки В до N.
C
E2'
|
E3' |
O |
|
|
|
E' |
N |
|
|
|
|
|
M |
M1 |
|
|
|
|
|
A |
M2 |
E1' |
B |
Рис. 2. 6. Перспективная проекция диаграммы растворимости четверной системы простого эвтонического типа
Третья последовательность кристаллизации наблюдается у растворов, находящихся на линиях моновариантного равновесия двух твердых и жидкой фаз Е1'Е', Е2'Е' или Е3'Е' (точка О). В этих случаях кристаллизация начинается сразу с выделения двух твердых фаз (А и С, первичное выделение одного компонента отсутствует), при дальнейшем изотермическом испарении состав жидкой фазы изменяется по линии Е3'Е' от точки О до Е', точка твердой фазы при этом перемещается приблизительно от точки Е3' до О.
Четвертый способ кристаллизации характерен для тройного эвтонического раствора (точка Е'). В этом случае отсутствует первичная и вторичная кристаллизации. Состав раствора и суммарный состав твердой фазы до полного затвердевания находятся в точке Е'.
Из других предложенных методов изображения диаграмм растворимости трех нереагирующих между собою солей в одном растворителе укажем метод Енеке. Изотермическая диаграмма растворимости трех солей с общим ионом строится следующим образом. Состав солевой массы наносят на треугольник Гиббса-Розебома, принимая сумму солей за 100, строят перпендикуляры к плоскости этого треугольника и откладывают на них содержание воды в определенном количестве раствора или количество воды, приходящееся в нем на определенное количество солевой массы. Получается пространственная диаграмма в виде призмы, аналогичная диаграмме состояния тройных систем плавкости. Входящую в ее
30
состав изотермическую поверхность растворимости можно ортогонально спроецировать на плоскость концентрационного треугольника; соединяя линией точки, отвечающие одинаковому содержанию воды, получают "изогидры" (см. п. 11. 4 ).
2.4. Принципиальная схема изотермы и изобары растворимости трех твердых веществ в одном растворителе с образованием
кристаллогидратов или двойных солей
Если одно, два или все три вещества образуют гидраты только одного состава и на всех стадиях испарения не происходит обезвоживания, то перспективная проекция изотермы растворимости будет иметь тот же вид, что и в случае выделения безводных веществ. При этом полюсами соответствующих полей будут служить фигуративные точки безводных компонентов: эти точки являются проекциями всех соответствующих кристаллогидратов и насыщенных относительно них растворов.
Если мы пользуемся ортогональной проекцией, то дело обстоит иначе: каждому гидрату будет отвечать своя проекция полюса; при этом, конечно, проекции полюсов всех гидратов данного вещества будут лежать на проекции соответствующего ребра.
Предположим теперь, что один из компонентов, например А, образует гидрат A·nH2O, причем по достижению известных концентраций одного вещества (В) раствор обезвоживает этот кристаллогидрат и переводит его в кристаллы чистого А. Тогда на перспективной проекции (см. рис. 2. 7), согласно принципу соответствия, мы должны иметь поле гидрата A·nH2O и поле безводного вещества А.
На рис. 2.7 изображена схема такой центральной проекции; на ней ApPe3 - поле гидрата A·nH2O, pPEe1 - поле кристаллизации безводного А, Ce2EPe3 - поле C, Be1Ee2 - поле В. Кристаллизация в поле безводного А является продолжением тех же путей в поле гидрата, так как проекция полюсов этих полей совпадает (точка А).
Проследим для примера испарение раствора, заданного точкой М. Пока происходит испарение растворителя из насыщенного раствора, проекция фигуративной точки последнего находится в точке М, так как в это время фигуративная точка раствора движется по лучу, соединяющему исходную точку с вершиной тетраэдра D, а этот луч как раз и является проектирующим. При изображении диаграммы в ортогональной проекции дело обстоит сложнее: на ней процессу испарения растворителя без выделения растворенного вещества будет отвечать прямолинейный отрезок.
Первым начинает кристаллизоваться гидрат A·nH2O, причем фигуративная точка раствора движется (рис. 2.7) от М к p1. По достижении точки p1 раствор начинает обезвоживать этот гидрат; таким образом, раствор, гидрат A·nH2O и безводный компонент А будут находиться в равновесии, и, пока весь гидрат не будет обезвожен, фигуративная точка раствора не сойдет со своего положения (точка p1). Когда же последние кристаллики гидрата исчезнут, фигуративная точка раствора сойдет с места и будет двигаться по тому же лучу кристаллизации, но уже в
