- •Основные понятия
- •1.2. Степень окисления или окислительное число атома в соединениях
- •Восстановители, окислители. Процессы окисления и восстановления
- •1.3.1. Восстановители
- •1.3.2. Окислители
- •1.4. Классификация окислительно-восстановительных реакций (типы овр)
- •1.4.1. Реакции межатомного или межмолекулярного окисления-восстановления
- •1.4.2. Реакции внутримолекулярного окисления – восстановления
- •1.4.3. Реакции диспропорционирования (самоокисления – самовосстановления)
- •2. Составление уравнений реакций окисления – восстановления
- •2.1. Метод электронного баланса
- •2.2. Метод ионно-электронного баланса (метод полуреакций)
- •Овр, протекающие в кислой среде
- •2.2.2. Овр, протекающие в щелочной среде
- •2.2.3. Овр, протекающие в присутствии молекул воды в левой части схемы
- •3.Некоторые особые случаи уравнений
- •3.1. Одновременное окисление атомов, находящихся
- •3.2. Овр в присутствии перекиси водорода (h2o2) и её соединений
- •3.3. Проявление восстановительной и окислительной способности разных атомов одного и того же элемента, входящих в состав разных веществ или одного и того же вещества
- •3.4. Особенности протекания овр при термитной сварке
- •3.5. Овр в присутствии окислителя – озона (о3)
- •3.6. Овр с участием органических соединений
- •4. Эквиваленты окислителей и восстановителей
- •5. Количественная характеристика окислительно-восстановительных реакций и направление овр
- •5.1. Электродный потенциал и его возникновение
- •5.2. Общие понятия о работе гальванического элемента
- •5.3. Стандартный электродный потенциал
- •5.4. Окислительно-восстановительные потенциалы
- •5.4.1. Направление овр в зависимости от значения величины энергии Гиббса ∆g
- •5.4.2. Условия, влияющие на величину овп и направление овр
- •5.4.3. Влияние на направление овр растворимости продукта реакции восстановленной формы
- •5.4.4. Константы равновесия окислительно-восстановительных реакций
- •5.4.5. Примеры решения задач на определение направления окислительно-восстановительных реакций
- •5.4.6. Задачи для самостоятельного решения
- •6. Механизмы некоторых реакций
- •7. Тестовый промежуточной контроль по теме овр
- •Задание: Коэффициент перед восстановителем в реакции
- •Задание: Константа равновесия окислительно-восстановительной системы пристандартных условиях ; равна:
- •Задание: Направление окислительно-восстановительной реакции при указанных условиях будет:
- •Задание: Окислительно-восстановительная реакция
- •Ответы: 1) 0,56 в; 2) 1,21 в; 3) 0,7 в; 4) 0,8 в; 5) 0,82 в.
- •Задание: Константа равновесия окислительно-восстановительной реакции
- •Задание: Константа равновесия реакции
- •Для стандартных условий равна:
- •8. Лабораторные работы
- •8.1. Рекомендации для подготовки к лабораторным занятиям
- •8.2. Реакции межмолекулярного окисления-восстановления Опыт 1. Окислительные свойства дихромата калия
- •Опыт 2. Окислительные свойства перманганата калия (kMnO4) в разных средах
- •Опыт 4. Восстановительные свойства галогенидов
- •Опыт 5. Взаимодействие растворов солей железа (ш) и иодида калия
- •8.3. Реакции внутримолекулярного окисления-восстановления
- •Опыт 2. Термическое разложение перманганата калия (kMnO4)
- •Опыт 3. Термическое разложение нитрата меди (II) (Cu(no3)2·2h2o)
- •8.4. Реакции диспропорционирования (самоокисления, самовосстановления) Опыт 1. Взаимодействие йода со щелочами
- •Опыт 2. Термическое разложение сульфита натрия
- •8.5. Двойственное поведение пероксида водорода в овр Опыт 1. Восстановительные свойства пероксида водорода
- •Опыт 2. Окислительные свойства пероксида водорода
- •8.6. Зависимость направления овр от рН среды Опыт 1 Влияние рН раствора на направление овр
- •8.7. Реакции, в которых окислитель или восстановитель
- •Расходуются также на связывание получаемых продуктов
- •Опыт 1. Окисление хлорид-иона концентрированной соляной кислоты
- •Двуокисью свинца (PbO2)
- •8.8. Учебно-исследовательская работа
- •10. Вопросы для домашнего задания
5.2. Общие понятия о работе гальванического элемента
Гальванический элемент состоит обычно из двух полуэлементов, каждый из которых представляет собой электрод, опущенный в ионную среду. Ограничимся рассмотрением гальванических элементов, в которых ионной средой выступают водные растворы электролитов, например в общем виде:
|
- Металл I |
Электролит I |
|
Электролит II |
Металл II + |
На этих схемах одна вертикальная черта обозначает границу раздела твердой и жидкой фаз, т.е. электрод-электролит. Две вертикальные черты обозначают границу раздела двух жидких фаз, между которыми не возникает диффузионный потенциал Δφдиф. Если катионы и анионы, переходящие из одного электролита в другой, имеют разные подвижности, то на границе раздела фаз возникает диффузионный потенциал Δφдиф. В этом случае границу раздела двух жидких фаз разделяют на схеме пунктирной чертой.
Согласно Международной конвенции о системе знаков в схеме гальванического элемента (Стокгольм, 1953 г.) слева записывается электрод, на котором происходит окисление, а на правом электроде должна протекать реакция восстановления. При этом левый электрод (анод) будет иметь более отрицательный электродный потенциал φа по сравнению с электродным потенциалом правого электрода (катод) φк. При работе гальванического элемента, таким образом, возникает разность потенциалов, названная электродвижущей силой (ЭДС) элемента:
Δφ = φк – φа
ЭДС возникает при самопроизвольном протекании электродных реакций за счет убыли энергии Гиббса ΔG. При этом совершается полезная работа (электрическая), которая в условиях равновесия электрохимических реакций максимальна, положительна и равна
A = n F (φк – φа)
Если гальванический элемент работает при постоянстве температуры и давления, то
ΔG = -А = - n F Δφ,
где n – число электронов, участвующих в электрохимических реакциях окисления и восстановления;
F = 96485 Кулон
Электродные процессы представляют собой окислительно-восстановительные реакции, которые можно записать в следующем виде:
aA + bB + nē ↔ cC + dD
Если в электродном процессе участвует только одно вещество в окисленной и восстановленной формах, то запись реакции упрощается:
Ох + nē ↔ Red
Различают обратимые и необратимые электроды. При перемене направления электрического тока на обратимых электродах возникают реакции, противоположные по направлению, на необратимых – протекают реакции не обратные друг другу. Примером обратимого электрода служит медь в растворе, содержащем Cu2+. При прохождении тока в противоположных направлениях идут реакции Cu → Cu2+ + 2ē. К необратимым электродам относится, например, медь в растворе кислоты. Перемена направления тока приводит к реакциям 2H+ + 2ē → H2 и Cu → Cu2+ + 2ē. Общая реакция в электрохимической цепи будет
Ox1 + Red2 ↔ Ox2 + Red1
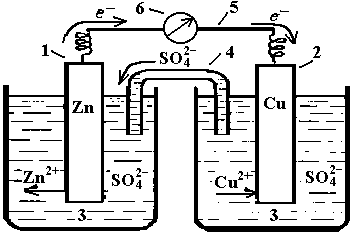
Примером обратимой цепи служит элемент Даниэля-Якоби. состоящий из цинкового и медного полуэлементов (рис. 3).
В цинковом полуэлементе металлическая цинковая пластина погружена в водный раствор соли цинка с концентрацией [Zn2+]=1 моль/л. В медном полуэлементе – металлическая медная пластина погружена в водный раствор соли меди (II) с концентрацией [Cu2+]=1 моль/л. Цинковая и медная пластины соединены металлическим проводником, растворы солей – «солевым мостиком» («электролитический ключ»).
|
|
|
Рис. 3. Гальванический элемент Даниэля-Якоби: 1- цинковая пластина (электрод); 2- медная пластина (электрод); 3,3- растворы электролитов (ZnSO4, CuSO4); 4- внутренняя цепь (U-образная трубочка, заполненная раствором электролита - KCl); 5- внешняя цепь – медная проволока; 6- гальванометр |
До замыкания цепи на каждой из металлических пластин на границе с раствором устанавливаются равновесия:
Cuo(тв.)
![]() Сu2+(р-р)
+ 2ē(на
мет.);
Сu2+(р-р)
+ 2ē(на
мет.); ![]()
Zno(тв.)
![]() Zn2+(р-р)
+ 2ē(на
мет.);
Zn2+(р-р)
+ 2ē(на
мет.); ![]()
Цинковая пластина
заряжена более отрицательно, чем медная.
Между ними возникает разность потенциалов.
При замыкании системы в цепь равновесия
на границе металл–раствор нарушаются.
По внешней цепи – металлическому
проводнику – избыток электронов с
цинковой пластины переходит на медную
пластину, где их концентрация меньше,
так как
![]() <
<![]() .
.
В результате, равновесие на цинковой пластине смещается вправо, идет окисление металлического цинка. На медной пластине равновесие смещается влево, протекает восстановление ионов меди (II).
Анод Zn(мет) – 2ē → Zn2+(р-р) (процесс окисления)
Катод Cu2+(р-р) + 2ē → Сu(мет) (процесс восстановления)
В ионном виде эти два процесса запишутся как:
Zn(мет) + Cu2+(р-р) → Zn2+(р-р) + Cu(мет)
Молекулярное уравнение суммарной реакции
Zn + Cu(NO3)2 → Zn(NO3)2 + Cu
Между растворами электролитов также возникает разность потенциалов. В цинковом полуэлементе в результате растворения цинка увеличивается концентрация ионов Zn2+, в растворе создается избыток положительно заряженных ионов. В медном полуэлементе в результате осаждения меди концентрация ионов Cu2+ уменьшается и в растворе создается избыток отрицательно заряженных ионов. По внутренней цепи – «солевому мостику» – катионы и анионы перемещаются навстречу друг другу. Таким образом, в системе возникает направленное перемещение заряженных частиц, т.е. возникает электрический ток.
Электродвижущая сила – ЭДС – гальванического элемента определяется разностью потенциалов катода и анода:
![]() > 0
> 0
В таком неравновесном режиме элемент Даниэля-Якоби будет работать до тех пор, пока полностью не растворится цинковая пластинка или полностью не восстановятся ионы меди Cu2+.
Для обозначения гальванического элемента используют символическую запись, упрощающую их описание, например, элемент Даниэля-Якоби может быть описан следующей краткой схемой:
ө Zn|
ZnSO4
| | CuSO4
| Cu
![]()
полуэлемент полуэлемент
анод катод