
- •Основные понятия
- •1.2. Степень окисления или окислительное число атома в соединениях
- •Восстановители, окислители. Процессы окисления и восстановления
- •1.3.1. Восстановители
- •1.3.2. Окислители
- •1.4. Классификация окислительно-восстановительных реакций (типы овр)
- •1.4.1. Реакции межатомного или межмолекулярного окисления-восстановления
- •1.4.2. Реакции внутримолекулярного окисления – восстановления
- •1.4.3. Реакции диспропорционирования (самоокисления – самовосстановления)
- •2. Составление уравнений реакций окисления – восстановления
- •2.1. Метод электронного баланса
- •2.2. Метод ионно-электронного баланса (метод полуреакций)
- •Овр, протекающие в кислой среде
- •2.2.2. Овр, протекающие в щелочной среде
- •2.2.3. Овр, протекающие в присутствии молекул воды в левой части схемы
- •3.Некоторые особые случаи уравнений
- •3.1. Одновременное окисление атомов, находящихся
- •3.2. Овр в присутствии перекиси водорода (h2o2) и её соединений
- •3.3. Проявление восстановительной и окислительной способности разных атомов одного и того же элемента, входящих в состав разных веществ или одного и того же вещества
- •3.4. Особенности протекания овр при термитной сварке
- •3.5. Овр в присутствии окислителя – озона (о3)
- •3.6. Овр с участием органических соединений
- •4. Эквиваленты окислителей и восстановителей
- •5. Количественная характеристика окислительно-восстановительных реакций и направление овр
- •5.1. Электродный потенциал и его возникновение
- •5.2. Общие понятия о работе гальванического элемента
- •5.3. Стандартный электродный потенциал
- •5.4. Окислительно-восстановительные потенциалы
- •5.4.1. Направление овр в зависимости от значения величины энергии Гиббса ∆g
- •5.4.2. Условия, влияющие на величину овп и направление овр
- •5.4.3. Влияние на направление овр растворимости продукта реакции восстановленной формы
- •5.4.4. Константы равновесия окислительно-восстановительных реакций
- •5.4.5. Примеры решения задач на определение направления окислительно-восстановительных реакций
- •5.4.6. Задачи для самостоятельного решения
- •6. Механизмы некоторых реакций
- •7. Тестовый промежуточной контроль по теме овр
- •Задание: Коэффициент перед восстановителем в реакции
- •Задание: Константа равновесия окислительно-восстановительной системы пристандартных условиях ; равна:
- •Задание: Направление окислительно-восстановительной реакции при указанных условиях будет:
- •Задание: Окислительно-восстановительная реакция
- •Ответы: 1) 0,56 в; 2) 1,21 в; 3) 0,7 в; 4) 0,8 в; 5) 0,82 в.
- •Задание: Константа равновесия окислительно-восстановительной реакции
- •Задание: Константа равновесия реакции
- •Для стандартных условий равна:
- •8. Лабораторные работы
- •8.1. Рекомендации для подготовки к лабораторным занятиям
- •8.2. Реакции межмолекулярного окисления-восстановления Опыт 1. Окислительные свойства дихромата калия
- •Опыт 2. Окислительные свойства перманганата калия (kMnO4) в разных средах
- •Опыт 4. Восстановительные свойства галогенидов
- •Опыт 5. Взаимодействие растворов солей железа (ш) и иодида калия
- •8.3. Реакции внутримолекулярного окисления-восстановления
- •Опыт 2. Термическое разложение перманганата калия (kMnO4)
- •Опыт 3. Термическое разложение нитрата меди (II) (Cu(no3)2·2h2o)
- •8.4. Реакции диспропорционирования (самоокисления, самовосстановления) Опыт 1. Взаимодействие йода со щелочами
- •Опыт 2. Термическое разложение сульфита натрия
- •8.5. Двойственное поведение пероксида водорода в овр Опыт 1. Восстановительные свойства пероксида водорода
- •Опыт 2. Окислительные свойства пероксида водорода
- •8.6. Зависимость направления овр от рН среды Опыт 1 Влияние рН раствора на направление овр
- •8.7. Реакции, в которых окислитель или восстановитель
- •Расходуются также на связывание получаемых продуктов
- •Опыт 1. Окисление хлорид-иона концентрированной соляной кислоты
- •Двуокисью свинца (PbO2)
- •8.8. Учебно-исследовательская работа
- •10. Вопросы для домашнего задания
10. Вопросы для домашнего задания
1. Укажите, какие из нижеприведенных ионов (атомов, молекул) могут являться только восстановителями? Теоретически обоснуйте ответ.
|
Вариант I |
Ca0 |
CO32- |
MnO32- |
FeO2- |
Cl- |
|
Вариант II |
Se2- |
SeO32- |
PbO2 |
CrO42- |
SnO32- |
|
Вариант III |
Sn4+ |
Al3+ |
Sn4+ |
Mn6+ |
N3- |
|
Вариант IV |
As3- |
As0 |
As2O3 |
AsO33- |
AsO33- |
|
Вариант V |
Li0 |
N3+ |
Mn7+ |
Cr6+ |
S6+ |
|
Вариант VI |
B3+ |
S4+ |
Pb3+ |
Al3+ |
Br- |
|
Вариант VII |
BiO3- |
Ge2+ |
Se4+ |
P3- |
SbO2- |
|
Вариант VIII |
SO2 |
TeO62- |
S0 |
Mg0 |
ClO2- |
|
Вариант IX |
N3- |
S2- |
P3+ |
ClO2 |
Mn3+ |
|
Вариант X |
Si4- |
SiO32- |
NO2 |
Au3+ |
Pb4+ |
2. Укажите, какие из нижеприведенных ионов (атомов, молекул) могут являться только окислителями? Теоретически обоснуйте ответ. Дайте определение окислителю.
|
Вариант I |
MnO2 |
MnO32- |
MnO42- |
Mn2+ |
MnO4- |
|
Вариант II |
Cr2O72- |
Cr3+ |
CrO2- |
CrO |
Cr(OH)3 |
|
Вариант III |
SeO42- |
Se2- |
SeO2 |
AsH3 |
AsO33- |
|
Вариант IV |
AsO33- |
NH3 |
PbO |
NO2- |
HN3 |
|
Вариант V |
HAuCl4 |
Au0 |
Zn0 |
Fe2+ |
Co2+ |
|
Вариант VI |
V4+ |
Sn2+ |
NO |
H2SO4 |
Br- |
|
Вариант VII |
Cr |
H2C2O4 |
HCOOH |
P |
CO2 |
|
Вариант VIII |
Co |
As3+ |
C |
NO2- |
PO43- |
|
Вариант IX |
H2 |
Fe2+ |
S |
NH3 |
SnO32- |
|
Вариант X |
VO3- |
NO |
Fe2O3 |
WO2 |
J- |
3. Укажите, при каком переходе имеет место окисление? Теоретически обоснуйте ответ. Дайте определение окислителю.
|
Вариант I |
Cl- |
Fe2O3 |
Cl2 |
2JO4- |
Sn4+ |
|
Вариант II |
Cr2O72- |
NO3- |
MnO4-
|
MnO4- |
Pb2+
|
|
Вариант III |
SeO42- |
AsO43 |
As2S3 |
VO3- |
BrO3- |
|
Вариант IV |
Br2 |
BrO- |
Br2 |
Br2O5 |
Br2O |
|
Вариант V |
CrO30 |
CrO3
|
Cr2O72- |
Cr2O72- |
Cr3+ |
|
Вариант VI |
NO3- |
MnO4- |
Cl20 |
As2O3 |
2BiO33-
|
|
Вариант VII |
Mn2+ |
CrO30 |
S0 |
S6+ |
NO3- |
|
Вариант VIII |
Cl- |
Fe2O3 |
Cl20 |
2JO4- |
Sn4+ |
|
Вариант IX |
MnO20
|
MnO4- |
MnO44- |
MnO2 |
MnO4-
|
|
Вариант X |
N3- |
N2 |
N2 |
NO3- |
NO3 |
4. Укажите, при каком переходе имеет место восстановление? Теоретически обоснуйте ответ. Укажите что такое восстановление.
|
Вариант I |
Mn2- |
Mn4+ |
MnO2 |
MnO32- |
MnO4-
|
|
Вариант II |
J- |
J- |
J- |
J2 |
J- |
|
Вариант III |
ZnO2 |
Cr3+ |
NO2- |
ClO2- |
2Cl |
|
Вариант IV |
Cr(OH)3 |
As2O3
|
J2 |
CuO
|
Mn2+ |
|
Вариант V |
BeO |
Be0
|
2Bi0 |
La |
J2 |
|
Вариант VI |
Po2+ |
Po0 |
Pt |
PtO2 |
PdO2 |
|
Вариант VII |
Po2+ |
Po0 |
Pt |
PtO2 |
PdO2 |
|
Вариант VIII |
Os0 |
OsO2 |
OsO2 |
SnO2- |
Zn2+
SnO |
|
Вариант IX |
PbO32-
|
PbSO4 |
H2S |
S2- |
2Ag+
|
|
Вариант X |
Sn2+ |
Ti2+ |
Ti3+ |
GeO
|
Ca2+ |
5. Укажите, атом или молекула какого элемента играет роль окислителя в нижеприводимых окислительно-восстановительных реакциях? Теоретически обоснуйте ответ. Дайте определение окислителю. Подберите коэффициенты в данной ОВР.
|
Вариант I |
Bi2O3
+ Cl2
+KOH |
|
Вариант II |
Na2SO3
+ KMnO4
+H2O
|
|
Вариант III |
CrBr3
+ H2O2
+NaOH |
|
Вариант IV |
AgNO3
+J2
+ H2O
|
|
Вариант V |
NaNO3
+Hg + H2SO4
|
6. Укажите, атом какого элемента играет роль восстановителя в нижеприводимых окислительно-восстановительных реакциях? Теоретически обоснуйте ответ. Дайте определение восстановителю. Подберите коэффициенты в рассматриваемой ОВР.
|
Вариант I |
MgJ2
+H2O2
+ H2SO4 |
|
Вариант II |
Mn(NO3)2
+PbO2
+ HNO3 |
|
Вариант III |
AgNO3
+AsH3
+ H2S |
|
Вариант IV |
Na3AsO3
+ K2Cr2O7
+ H2SO4
|
|
Вариант V |
CS2
+KOCl + KOH |
7. Какие из нижеприведенных ионов или молекул могут играть роль одновременно и окислителя, и восстановителя? Теоретически обоснуйте ответ. Когда проявляется окислительно-восстановительная двойственность?
|
Вариант I |
SO42- |
PO43- |
NO2- |
AsO43- |
MnO4- |
|
Вариант II |
MnO32- |
MnO4- |
PbO2 |
SnO22- |
SnO32- |
|
Вариант III |
SO32- |
BiO3- |
WO42- |
CO2+ |
FeO42- |
|
Вариант IV |
Br- |
N3+ |
P5+ |
S6+ |
S2- |
|
Вариант V |
Cl5+ |
Mn7+ |
Cl- |
P5+ |
Ca2+ |
|
Вариант VI |
Cl- |
K+ |
P4+ |
O2- |
J7+ |
|
Вариант VII |
SO32- |
PO3- |
Mn2O |
PbO2 |
S2- |
|
Вариант VIII |
FeO42- |
WO3 |
Mg |
FeO2- |
Cl2O7 |
|
Вариант IX |
SbO2- |
SbO3- |
Ta2O5 |
SnO32- |
HNO2 |
|
Вариант X |
NH4+ |
N2O |
PbO32- |
GeO |
SeO32- |
8. Какие из нижеприведенных ОВР относятся к реакции диспропорционирования? Теоретически обоснуйте ответ. Дайте определения таким реакциям. Подберите коэффициенты в рассматриваемой ОВР.
Вариант I
|
1) |
P
+
KOH + H2O |
|
2) |
FeS2
+HCl
+ HNO3 |
|
3) |
Zn
+
H2SO4
|
|
4) |
P
+ HNO3
|
|
5) |
H2SO4
+
HJ
|
Вариант II
|
1) |
Al
+ CuSO4
|
|
2) |
Na2V4O9
+HCl
|
|
3) |
N2H4
|
|
4) |
KClO3
+ J2
+
H2O
|
|
5) |
Bi
+
HNO3
|
Вариант III
|
1) |
Fe2O3
+ CO
|
|
2) |
Bi2O3
+
Cl2
+ KOH
|
|
3) |
Zn
+
HNO3 |
|
4) |
HClO3
|
|
5) |
Ag
+
H2SO4
|
Вариант IV
|
1) |
S
+ KOH
|
|
2) |
Fe2
(SO4)3
+
AsH3
|
|
3) |
CrCl3
+
H2O2
+
NaOH
|
|
4) |
CuS
+ HNO3
|
|
5) |
CaO
+ CO2
|
Вариант V
|
1) |
Zn
+ H2SO4
|
|
2) |
H2O2
+
KJ + HCl
|
|
3) |
KJ
+
Br2
|
|
4) |
KClO3
|
|
5) |
CuSO4
+ Fe
|
Вариант VI
|
1) |
K2SO3
|
|
2) |
SnCl2
+
HgCl2
|
|
3) |
AgNO3
+
KCN
|
|
4) |
MnSO4
+ KMnO4
+
H2O
|
|
5) |
HJ
+
Cl2
+
H2O
|
Вариант VII
|
1) |
Cu
+ H2SO4
|
|
2) |
Cu
+
Hg(NO3)2
|
|
3) |
Mn2(SO4)3
+
H2C2O4
|
|
4) |
KOH+
MnO2
+
KClO3
|
|
5) |
ClO2
+
Ba(OH)2
|
Вариант VIII
|
1) |
KJO3
+ HF
|
|
2) |
Br2
+
Cl2
+
H2O
|
|
3) |
Ag
+ O3
|
|
4) |
H2S
+ Br2
+
H2O
|
|
5) |
HNO2
|
9. Какая из нижеприведенных реакций является окислительно-восстановительной? Дайте определение ОВР. Укажите окислитель и восстановитель. Укажите коэффициенты в данной ОВР.
Вариант I
|
1) |
H3PO4
+ 3NaOH |
|
2) |
Cr2
(SO4)3
+
6RbOH
|
|
3) |
BaCl2
+
(NH4)2C2O4
|
|
4) |
2FeSO4
+ Ag2SO4
|
|
5) |
KCl
+
NaNO2
|
Вариант II
|
1) |
HgCl2
+ 2KJ |
|
2) |
Fe(OH)
2 +
HCl
|
|
3) |
H2
+
Br2
|
|
4) |
Cr(OH)3
+ 3HCl
|
|
5) |
6HCl
+
Al2(SO4)3
|
Вариант III
|
1) |
HNO3
+ P + H2O
|
|
2) |
Zn(NO3)2
+
Na2S
|
|
3) |
CaCO3
|
|
4) |
H2SO4
+ BaCl2
|
|
5) |
Na2S
+ H2O
|
Вариант IV
|
1) |
Cr2S3
+ 6H2O
|
|
2) |
Hg(NO3)2
+
NaOH
|
|
3) |
H2S+
Br2
|
|
4) |
Fe2O3+
6HCl
|
|
5) |
NH3
+
H2O
|
Вариант V
|
1) |
Fe2O3
+ CO
|
|
2) |
Al2O3
+
3H2SeO4
|
|
3) |
2CuSO4
+
2H2O
|
|
4) |
Zn(OH)2+
H2SO4
|
|
5) |
SeO2
+
H2O
|
Вариант VI
|
1) |
H2S
+ Cd(NO3)2
|
|
2) |
Zn
+
H2SO4
|
|
3) |
AlCl3
+2H2O
|
|
4) |
Pb(NO3)2+
H2S
|
|
5) |
3MnSO4
+
2Al(OH)3
|
Вариант VII
|
1) |
Mg
+ HNO3
|
|
2) |
MnSO4
+
2NaNO3
|
|
3) |
FeCl3
+3NH4CNS
|
|
4) |
K2CrO4
+
2AgNO3
|
|
5) |
SnCl2
+
H2O
|
Вариант VIII
|
1) |
SbO3
+ 2H2O
|
|
2) |
SnCl2
+
H2S
|
|
3) |
PbO
+
2HNO3
|
|
4) |
Pb(OH)2+
2KOH
|
|
5) |
2PbO2
|
Вариант IX
|
1) |
PbO
+ 2HCl
|
|
2) |
Al2S3
+
H2O
|
|
3) |
SnS2
+
3O2
|
|
4) |
NaOH+
SO2
|
|
5) |
SO3
+
H2O
|
Вариант X
|
1) |
2H2S
+ H2SO3
|
|
2) |
2H2SO2
|
|
3) |
NaCl
+NaHSO4
|
|
4) |
CaF2+
H2SO4
|
|
5) |
KClO4
+
H2SO4 |
10. Какая из нижеприведенных ОВР относится к реакции внутримолекулярного окисления-восстановления? Дайте определение реакции внутримолекулярного окисления-восстановления.
Вариант I
|
1) |
2NaCl + Zn(NO3)2 = 2NaNO3 + ZnCl2 |
|
2) |
Cu + 2H2SO4 = CuSO4 + SO2 + 2H2O |
|
3) |
NH4NO3 = N2O + 2H2O |
|
4) |
SO2+ H2O = H2SO3 |
|
5) |
Zn + 2HCl = ZnCl2 + H2 |
Вариант II
|
1) |
2La
+ 3Cl2 |
|
2) |
3Mg
+ N2
|
|
3) |
H2
+
CuO
|
|
4) |
2Al +Cr2O3 = 2Cr+ Al2O3 |
|
5) |
2AgNO3 = 2Ag0 + 2NO2 + O2 |
Вариант III
|
1) |
3Zn + 2AuCl3 = 2Au + 3ZnCl2 |
|
2) |
Fe(NO3)2 + AgNO3= Ag + Fe(NO3)3 |
|
3) |
4Al +3O2 = 2Al2O3 |
|
4) |
2КClO3 = 3O2+ 2KCl |
|
5) |
Cu + 8HNO3 = 3Cu(NO3) 2 + 2NO + 4H2O |
Вариант IV
|
1) |
3Zn + 2AuCl3 = 2Au + 3ZnCl2 |
|
2) |
2Al + 3CuSO4 = 3Cu + Al2 (SO4)3 |
|
3) |
H3PO4 +3NaOH = 3H2O + Na3PO4 |
|
4) |
2Ag2O = O2+ 4Ag |
|
5) |
2FeSO4 + Ag2SO4 = 2Ag + Fe2(SO4)3 |
Вариант V
|
1) |
2Rb + H2O = H2 + 2RbOH |
|
2) |
Zn + NaNO3 + 7NaOH + 6H2O = NH3 +4Na2[Zn(OH)4] |
|
3) |
5Cd +KMnO4 + 8H2SO4 = 5CdSO4+ K2SO4 + 2MnSO4 + 8H2O |
|
4) |
Na2HPO4+ H2O = NaH2PO4 + NaOH |
|
5) |
4КClO3 = 3КClO4 + KCl |
11. На основании величин стандартных окислительно-восстановительных потенциалов указать, какой из ионов, молекул является наиболее сильным окислителем? Дайте объяснение
Вариант I φ0В
|
1) |
3N2 + 2H+/+2ē+2HN3 -3,1B |
|
2) |
N2 + 2H2O+4H+/+2 ē+ (2NH4OH) +H+ -1,87B |
|
3) |
2HNO2+4 H++4ē /N2O + 3H2O +1,29B |
|
4) |
N2H4+ 4H2O+2ē/2NH4OH+2OH- +0,1B |
|
5) |
NH2OH+ 2H2O+2ē/ NH4OH+2OH- +0,42В |
Вариант II φ0В
|
1) |
2BrO¯/Br2 + 0,45 В |
|
2) |
BrO3 ¯ /BrO¯ + 0,54 В |
|
3) |
Br2/2Br- + 1,087В |
|
4) |
2BrO3¯ /Br2 + 1,52 В |
|
5) |
2HBrO + 2H+ + 2e-/Br2+ 2H2O + 1,59 В |
Вариант III φ0В
|
1) |
V2++2ē/V – 1,175B |
|
2) |
V2++ē/ VO+ – 0,044 B |
|
3) |
V2O5 + 6H++ 6 ē /2VO+ + 3H2O + 0,958 B |
|
4) |
H2VO4+ 4H++ ē /VO2++ 3H2O + 1,314 B |
|
5) |
VO43о –+ 6H++ 2 ē /VO++ 3H2O – 1,125 B |
Вариант IV φ0В
|
1) |
MnO2 + 4H+ +2ē/Mn0 +2H2O + 1,228 B |
|
2) |
Mn2O3 + 6H++ 2 ē /2Mn2 +3H2O + 1,443 B |
|
3) |
MnO4–+ 8H+ +5 ē / Mn2 + 4 H2O + 1,509 B |
|
4) |
Mn2+/ Mn0 - 1,48 B |
|
5) |
2H2O +MnO4–+ 3 ē/Mn02+4OH- + 0,69 В |
Вариант V φ0В
|
1) |
J2 + 2e-/2J- + 0,536 B |
|
2) |
2JCN + 2H+ + 2ē/J2 + 2HCN + 0,63 B |
|
3) |
HJO + H+ + 2ē/J¯ + H2O + 0,99 B |
|
4) |
2HJO + 2H+ + 2ē/J2 + 2H2O + 1,45 B |
|
5) |
JO3- + 3H2O + 6ē/J¯ + 6OH- + 0,26 B |
12. На основании величин стандартных окислительно-восстановительных потенциалов указать, какой из ионов (молекул, атомов) является наиболее сильным восстановителем? Объясните.
Вариант I φ0В
|
1) |
Li/Li+ - 3,02 В |
|
2) |
K/K+ - 2,922 В |
|
3) |
Ca/Ca2+ - 2, 87 В |
|
4) |
Na/Na+ - 2, 712 В |
|
5) |
Mg/Mg2+ - 2,64 В |
Вариант II φ0В
|
1) |
H2/2H+ 0,00 В |
|
2) |
Fe3+/Fe0 - 0,036 В |
|
3) |
Pb0/Pb2+ - 0,126 В |
|
4) |
Co/Co2+ - 0, 277 В |
|
5) |
Cr2 / Cr3+ - 0,41 В |
Вариант III φ0В
|
1) |
Mn0 /Mn2+ – 1,05 В |
|
2) |
Te2- / Te0 – 0,92 В |
|
3) |
SO32- + 2OH-/SO42-+ H2O – 0,90 В |
|
4) |
Zn/Zn2+ – 0,76 В |
|
5) |
S2 - /S0 – 0,508 В |
Вариант IV φ0В
|
1) |
H2C2O4/2CO2 + 2H+ – 0,49 В |
|
2) |
Fe0/Fe2+ – 0,44 В |
|
3) |
H2/2H+ – 0,414 В |
|
4) |
H3PO3 + H2O / H3PO4 + 3H+ – 0, 20 В |
|
5) |
Sn/Sn2+ – 0,136 В |
Вариант V φ0В
|
1) |
H2S/S + 2H+ + 0,141 В |
|
2) |
Sn2+ +/Sn4+ +0,15 В |
|
3) |
Cu/Cu2+ + 0,34 В |
|
4) |
S + 3H2O/H2SO3 + 4H+ + 0, 45 В |
|
5) |
2J¯/J2 + 0,53 В |
13. При каком значении Δφ0 реакции перманганат калия KMnO4 может окислять хлорид олова SnCl2 в кислой среде? Дайте объяснение.
E0 MnO4 ¯ /Mn = +1,51 В E0Sn2 + /Sn4- =+0,15 В
1) э.д.с. = 0,64 В 2) э.д.с.=1,66 В 3) э.д.с.=+1,36 В
4) э.д.с.=+10,06 В 5) э.д.с.=0,0
14. В каком из нижеследующих пунктов правильно определено, что барий эффективнее взаимодействует с разбавленной соляной кислотой, чем никель? φ0Ba/Ba2+ = -2,90 В φ0Ni/Ni2+ = -0,25 В
φ0H2/2H = -0,00 В
1) –2.90-0.00=-2,90 В 2) 0,00+(-2,90) = -2,90 В
3) –2,90-(-0,25)= -1,65 В 4) –2,9+(-0,25) = -3,15 В
5) 0,00-(-2,90)= 2,90 В 6) 0,00-(-0,25) = 0,25 В
15. В каком из действий впервые при нахождении коэффициентов следующей ОВР допущена ошибка? Объясните причину?
Вариант I
CuS + HNO3
 S + Cu(NO3)2
+ NO + H2O
S + Cu(NO3)2
+ NO + H2OCuS + H+ = NO3-
 S0
+ Cu2+
+ 2NO3-
+ NO + H2O
S0
+ Cu2+
+ 2NO3-
+ NO + H2O
3) CuS – 2e- = Cu2+ + S0 1
 NO3-+
e-
= NO0
2
NO3-+
e-
= NO0
2
4)
CuS + 2NO3-
![]() Cu2+
+ S0
+
2NO
Cu2+
+ S0
+
2NO
CuS + 2HNO3
 Cu(NO3)2
+ S
+
2NO+ H2O
Cu(NO3)2
+ S
+
2NO+ H2O
Вариант II
K2Cr2O7
+ Fe2SO4
+ H2SO4
![]() Cr2(SO4)3
+ K2SO4
+ Fe2(SO4)3
+H2O
Cr2(SO4)3
+ K2SO4
+ Fe2(SO4)3
+H2O
2K++Cr2O72-+Fe2++ SO42- +2H+ + SO42-
 2Cr3++3SO42-
+2K+
+SO42-+2Fe3+
+3SO42
+H2O
2Cr3++3SO42-
+2K+
+SO42-+2Fe3+
+3SO42
+H2OCr2O72-+Fe2++2H+
 2Cr3++2Fe3++H2O
2Cr3++2Fe3++H2OC
 r2O72-
+
14H+
+
9e-
=
2Cr3+
+
7H2O
2
r2O72-
+
14H+
+
9e-
=
2Cr3+
+
7H2O
2
2Fe2+ – 2e- = 2Fe3+ 9
4)
2Cr2O7
+
28H+
+ 18Fe2+
![]() 4Cr3+
+
14H2O
+ 18Fe3+
4Cr3+
+
14H2O
+ 18Fe3+
5) 2 K2Cr2O7 + 14H2SO4 + 18FeSO4 = - 2Cr2(SO4)3+ 2K2SO4+ 9Fe2(SO4)3+ 14H2O
Вариант III
As2S3
+HNO3
+ H2O
![]() H3AsO4
+ NO + H2SO4
H3AsO4
+ NO + H2SO4
As2S3 +H+ + NO3- + H2O
 3H+
+
AsO4
3-+
NO + 2H+
+ SO42-
3H+
+
AsO4
3-+
NO + 2H+
+ SO42-As2S3 + H2O + NO3-
 AsO4
3-+
NO + SO42-
AsO4
3-+
NO + SO42-A
 s2S3
+ 20H2O
–
28e-
s2S3
+ 20H2O
–
28e-
 2AsO4
3-+
3SO42-
+ 4OH+
1
2AsO4
3-+
3SO42-
+ 4OH+
1
NO3-
–
ē![]() NO 28
NO 28
As2S3 + 2H2O + 2NO3-
 2AsO4
3-+
3SO42-+
4OH-
+ 28NO
2AsO4
3-+
3SO42-+
4OH-
+ 28NOAs2S3 +2HNO3 + 2H2O
 2H3AsO4
+ 3H2SO4
+ 28NO
2H3AsO4
+ 3H2SO4
+ 28NO
Вариант IV
NaCrO2
+ Br2
+ NaOH
![]() Na2CrO4
+ NaBr + H2O
Na2CrO4
+ NaBr + H2O
1)
Na+
+ CrO2-
+ Br2-
+ Na++OH-
![]() 2Na+
+
CrO42+
+ Na+
+ Br-
+ H2O
2Na+
+
CrO42+
+ Na+
+ Br-
+ H2O
CrO2- + Br2 + OH-
 CrO42-
+
2H2O
CrO42-
+
2H2OC
 rO2
–
3 ē + 4OH-
rO2
–
3 ē + 4OH-
 CrO42-
+
2H2O
1
CrO42-
+
2H2O
1
Br2
+
ē
![]() Br¯ 3
Br¯ 3
CrO2- + 4OH- + 3Br2 = CrO42- + 2H2O + 3Br2-
5)
NaCrO2
+ 4NaOH + 3Br2![]() Na2CrO4
+ 2H2O
+ 3NaBr
Na2CrO4
+ 2H2O
+ 3NaBr
Вариант V
PbO2
+ MnSO4
+ HNO3
![]() HMnO4
+ PbSO4
+ Pb(NO3)2
+H2O
HMnO4
+ PbSO4
+ Pb(NO3)2
+H2O
Pb4+ + 2O2- + Mn2+ + SO42- + H+ + NO3-
 H+
+MnO4-
+ Pb2+
+
SO42-
+ Pb2+
2NO3-
+H2O
H+
+MnO4-
+ Pb2+
+
SO42-
+ Pb2+
2NO3-
+H2OPb4+ + Mn2+ + H+
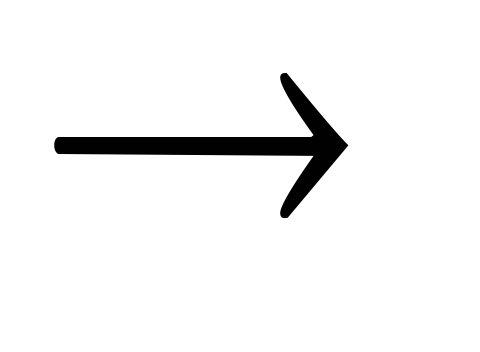 MnO4-
+ Pb2+
+
H2O
MnO4-
+ Pb2+
+
H2OP
 b4+
+ 2 ē = Pb2+ 5
b4+
+ 2 ē = Pb2+ 5
Mn2+ + 4H2O – 5e- = MnO4- + 8H+ 2
5Pb4+ + 2Mn2+ + 8H2O = 5Pb2+ + 2MnO4- + 16H+
5) 5PbO2 + 2MnSO4 + HNO3 = 2PbSO4 + 3Pb(NO3)2 + 2HMnO4 + 8H2O
Вариант VI
MnSO4
+ (NH4)2S2O8
+ H2O
![]() HMnO4
+ (NH4)2SO4+H2SO4
HMnO4
+ (NH4)2SO4+H2SO4
Mn2+ + SO4 2- +2NH4+ + S2O82- +2 H+ + O2-
 H+
+MnO4-
+ 2NH4+
+
2H+
+SO42-
H+
+MnO4-
+ 2NH4+
+
2H+
+SO42-Mn2+ + S2O82-
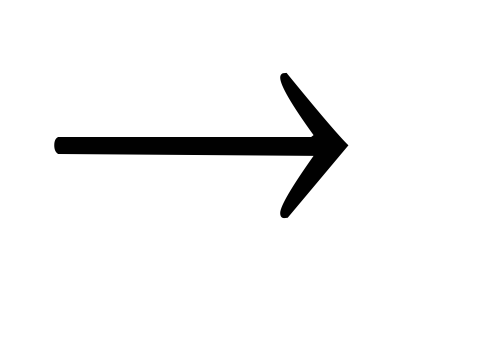 MnO4-
+ SO42-
+
H2O
MnO4-
+ SO42-
+
H2O Mn2+
+ 4H2O
-5 ē = MnO4-+
8H+ 2
Mn2+
+ 4H2O
-5 ē = MnO4-+
8H+ 2
S2O82- + 2 ē = 2SO42- 5
2Mn4+ + 8H2O + 5 S2O82- = 2MnO4- + 16H+ + 10SO42-
5)
2MnSO4
+5(NH4)2
S2O8
+ 8H2O
![]() 2HMnO4
+ 5(NH4)2SO4
+
7H2
SO4
2HMnO4
+ 5(NH4)2SO4
+
7H2
SO4
16. В следующих ОВР укажите из числа нижеприведенных пар ту, в которой правильно составлен ионно-электронный баланс.
Вариант I
Sb2S5
+ HNO3
+
H2O
![]() H5SbO4
+
H2SO4
+ NO
H5SbO4
+
H2SO4
+ NO
1
 )
Sb2S5
+ 4H2O
– 5e-
= SbO43-
+ 8H+1
)
Sb2S5
+ 4H2O
– 5e-
= SbO43-
+ 8H+1
NO3- – ē = NO 5
2
 )
Sb2S5
+ 28H2O
– 46 ē = 2SbO4
+
5SO42-
+ 56H+
3
)
Sb2S5
+ 28H2O
– 46 ē = 2SbO4
+
5SO42-
+ 56H+
3
NO3- + 4H+– 3 ē = NO + 2H2O 16
3
 )
Sb2S5
+ 28H2O
– 50e-
= 2SbO43-
+ 5SO4
+
56H+
1
)
Sb2S5
+ 28H2O
– 50e-
= 2SbO43-
+ 5SO4
+
56H+
1
 NO3-
–
ē = NO + 2H2O
50
NO3-
–
ē = NO + 2H2O
50
4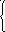 )
Sb2S5
+ 12H2O
– 16e-
= 2SbO43-
+ SO42-
+
24H+
3
)
Sb2S5
+ 12H2O
– 16e-
= 2SbO43-
+ SO42-
+
24H+
3
 NO3-
+
4H+
+
3 ē = NO + 2H2O 16
NO3-
+
4H+
+
3 ē = NO + 2H2O 16
5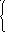 )
Sb2S5
+ 28H2O
– 40e-
= 2SbO43-
+ 5SO42-
+
56H+
3
)
Sb2S5
+ 28H2O
– 40e-
= 2SbO43-
+ 5SO42-
+
56H+
3
NO3- + 4H+ + 3 ē = NO + 2H2O 40
Вариант II
M n(NO3)2
+ AgNO3
+ NH4OH
n(NO3)2
+ AgNO3
+ NH4OH
![]() MnO2
+ Ag
+
NH4NO3
MnO2
+ Ag
+
NH4NO3
1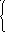 )
Mn2+
+ 2H2O
– 2 ē = MnO2
+ 4H+
1
)
Mn2+
+ 2H2O
– 2 ē = MnO2
+ 4H+
1
 Ag+
+
ē = Ag0
2
Ag+
+
ē = Ag0
2
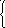 Mn2+
+
2H2O
+ 6 ē = MnO2
+ 4OH¯
1
Mn2+
+
2H2O
+ 6 ē = MnO2
+ 4OH¯
1
Ag+ + ē = Ag0 6

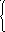 Mn2+
+
3OH-
- 3 ē = MnO2
+ H2O
+ H+
1
Mn2+
+
3OH-
- 3 ē = MnO2
+ H2O
+ H+
1
Ag + ē = Ag0 3
M

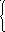 n2+
+
4OH-
- 2 ē = MnO2
1
n2+
+
4OH-
- 2 ē = MnO2
1
Ag0 + ē = Ag0 2
-
5
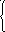
 )
Mn2+
+
4OH-
- 2 ē = MnO2+
2H2O
)
Mn2+
+
4OH-
- 2 ē = MnO2+
2H2O1
Ag+ + ē = Ag0
2
Вариант III
H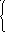 NO2
+ Br2
+ H2O
NO2
+ Br2
+ H2O
![]() HNO3
+ HBr
HNO3
+ HBr
1 )
NO2
–
ē = HNO3
1
)
NO2
–
ē = HNO3
1
Br2 + ē = Br- 1
2
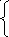 )
NO2
+
H2O
- 2 ē = NO3-
+
2H+
1
)
NO2
+
H2O
- 2 ē = NO3-
+
2H+
1
Br2 + ē = Br- 2
3
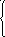 )
NO2
+
2H2O
+ 4e-
= NO3-
+
4H+
1
)
NO2
+
2H2O
+ 4e-
= NO3-
+
4H+
1
 Br2
+
2 ē = 2Br-
2
Br2
+
2 ē = 2Br-
2
4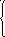 )
HNO2
+
H2O
- 2 ē = NO3-
+
2H+
1
)
HNO2
+
H2O
- 2 ē = NO3-
+
2H+
1
Br2 + 2 ē = 2Br- 1
Вариант IV
K
 2Cr2O7
+ H2S
+ H2SO4
2Cr2O7
+ H2S
+ H2SO4
![]() Cr2(SO4)3
+ S + K2SO4
+H2O
Cr2(SO4)3
+ S + K2SO4
+H2O
Cr2O72- - 2 ē = 2Cr3+ 1

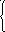 S22-
–
2 ē = S0
4
S22-
–
2 ē = S0
4
Cr2O72- + 10 ē = 2Cr3+ + 7O2- 1
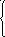 S22-
–
2 ē = S0
5
S22-
–
2 ē = S0
5
 3)
Cr2O72-
–
8 ē = 2Cr3+
+
7H2O
1
3)
Cr2O72-
–
8 ē = 2Cr3+
+
7H2O
1
S22- + 2 ē = S0 4
4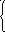
 )
Cr2O72-
+
14H+
+
6 ē = 2Cr3+
+
7H2O
1
)
Cr2O72-
+
14H+
+
6 ē = 2Cr3+
+
7H2O
1
 S22-
+
2 ē = S0
3
S22-
+
2 ē = S0
3
5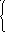 )
Cr2O72-
+
14H+
+
6 ē = 2Cr3+
+
7H2O
1
)
Cr2O72-
+
14H+
+
6 ē = 2Cr3+
+
7H2O
1
S22- - 2 ē = S0 3
Вариант V
KMnO4 + FeSO4 + H2SO4 = MnSO4+ Fe2(SO4)3+ K2SO4+ 14H2O
1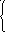
 )
MnO4
– 3 ē = Mn2+
1
)
MnO4
– 3 ē = Mn2+
1
Fe2+ – 3 ē = Fe3+ 3
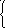
 2)
MnO4-
– 3 ē = Mn2+
+
4H2O
4
2)
MnO4-
– 3 ē = Mn2+
+
4H2O
4

 Fe2+
– 4 ē = 2Fe3+ 3
Fe2+
– 4 ē = 2Fe3+ 3
3) MnO4- + 8H+ + 5 ē = Mn2+ + 4H2O 4
Fe2+ – 4 ē = 2Fe3+ 5
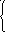
 4)
MnO4-
+
8H+
+
5 ē = Mn2+
+
4H2O
1
4)
MnO4-
+
8H+
+
5 ē = Mn2+
+
4H2O
1
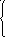
 Fe2+
– ē = 2Fe3+
5
Fe2+
– ē = 2Fe3+
5
5) MnO2- + 8H+ + 5 ē = Mn2+ + 4H2O 2
2Fe2+ – 2 ē = 2Fe3+ 5
17. Для указанной гальванической пары опишите принцип ее работы:
1) составьте схему гальванического элемента;
2) напишите уравнения процессов протекающих на электродах, суммарное уравнение;
3) определите направление движения электронов во внешней цепи;
4) рассчитайте ЭДС;
5) в каком случае работа указанного гальванического элемента прекратиться?
-
Вариант I
Fe / FeSO4 //
CuSO4/ Cu
1 моль/л
0,2 н
-
Вариант II
Sn / SnCl2 //
Pb(NO3)2/ Pb
2 моль/л
0,02 н
-
Вариант III
Ni / NiSO4 //
AgNO3/ Ag
0,6 н
1 моль/л
-
Вариант IV
Al / Al2(SO4)3 //
ZnSO4/ Zn
0,5 моль/л
0,04 н
11. ВАРИАНТЫ ДОМАШНЕГО ЗАДАНИЯ
|
Номер варианта |
1,2,3,4 – номер вопроса домашнего задания (x,xy); 4) – номер варианта ДЗ; (5,6) – номера ОВР, глава 10 | ||||||
|
1 |
2 |
3 |
4 |
5 |
6 | ||
|
среда | |||||||
|
кислая |
щелочная | ||||||
|
1 |
1(1,2) |
7(3,4) |
10(4) |
3(7,8) |
1Т |
| |
|
2 |
1(3,4) |
7(5,6) |
10(5) |
3(9,10) |
2Т |
12Т | |
|
3 |
1(5,6) |
7(7,8) |
11(1) |
2(3,4) |
3Т |
4Т | |
|
4 |
1(7,8) |
7(9,10) |
11(2) |
2(7,8) |
5Т |
8Т | |
|
5 |
1(9,10) |
8(1) |
11(3) |
2(9,10) |
7Т |
6Т | |
|
6 |
2(1,2) |
8(2) |
11(4) |
5(1,2) |
9Т |
16Т | |
|
7 |
2(3,4) |
8(3) |
11(5) |
6(2,3) |
45Т |
44Т | |
|
8 |
2(5,6) |
8(4) |
12(1) |
3(1,2) |
57Т |
59Т | |
|
9 |
2(7,8) |
8(5) |
12(2) |
4(5,6) |
10Т |
64Т | |
|
10 |
2(9,10) |
8(6) |
12(3) |
15(1) |
11Т |
66Т | |
|
11 |
3(1,2) |
8(7) |
12(4) |
1(3,4) |
29Т |
67Т | |
|
12 |
3(3,4) |
8(8) |
12(5) |
14(1) |
31Т |
69Т | |
|
13 |
3(5,6) |
17(1) |
7(1,2) |
16(2) |
68Т |
72Т | |
|
14 |
3(7,8) |
17(2) |
6(4,5) |
4(9,10) |
77Т |
73Т | |
|
15 |
3(9,10) |
9(1) |
8(1) |
2(9,10) |
89Т |
79Т | |
|
16 |
4(1,2) |
9 (2) |
4(3,4) |
1(3,4) |
98Т |
83Т | |
|
17 |
4(3,4) |
9 (3) |
13(1) |
8(6) |
131Т |
120Т | |
|
18 |
4(5,6) |
9 (4) |
14(1) |
12(6) |
129Т |
115Т | |
|
19 |
4(7,8) |
9 (5) |
15(1) |
16(1) |
124Т |
94Т | |
|
20 |
4(9,10) |
9 (6) |
16(1) |
8(8) |
118Т |
93Т | |
|
21 |
5(1,2) |
9(7) |
16(2) |
1(1,2) |
114Т |
125Т | |
|
22 |
5(3,4) |
9(8) |
16(3) |
17(5) |
111Т |
80Т | |
|
23 |
5(5) 6(1) |
9(10) |
16(4) |
17(4) |
104Т |
76Т | |
|
24 |
6(2,3) |
10(1) |
16(5) |
17(3) |
62Т |
49Т | |
|
25 |
6(4,5) |
10 (2) |
16(6) |
17(2) |
32Т |
41Т | |
|
26 |
7(1,2) |
10(3) |
4(1,2) |
17(1) |
84Т |
13Т | |
*В кислой среде все ионы металлов с зарядностью от 1 до 3 соединяются с кислотными остатками с образованием солей.
**В щелочной среде все образующиеся кислотные остатки (отрицательные ионы) соединяются с положительными ионами металлов с образованием солей.
*Здесь и далее приняты сокращения; в-ль-восстановитель, ок-ль-окислитель, в-е-восстановление, ок-е-окисление.
