
- •Ярославский государственный университет
- •Часть I. Механика
- •Глава 1. Кинематика
- •1.1. Общие понятия
- •1.2. Векторные величины. Действия над векторами
- •1.3. Производная
- •1.4. Траектория, путь, перемещение, скорость
- •1.5. Ускорение
- •1.6. Кинематика вращательного движения
- •Глава 2. Динамика материальной точки
- •2.1. Общие понятия
- •2.2. Виды взаимодействия и сил в природе
- •2.3. Первый закон Ньютона. Инерциальные системы отсчета
- •2.4. Масса и импульс тела
- •2.5. Второй закон Ньютона
- •2.6. Третий закон Ньютона
- •2.7. Преобразования Галилея. Принцип относительности Галилея
- •8. Упругие силы
- •2.8.1. Деформация растяжения – сжатия
- •2.8.2. Деформация сдвига
- •2.9. Силы трения
- •2.10. Сила тяжести. Вес тела
- •2.11. Тело на наклонной плоскости
- •Глава 3. Законы сохранения
- •3.1. Сохраняющиеся величины
- •3.2. Кинетическая энергия
- •3.3. Работа
- •3.4. Консервативные силы. Потенциальная энергия
- •3.5. Потенциальная энергия во внешнем поле сил тяжести Земли
- •3.6. Потенциальная энергия упругой деформации
- •3.7. Условия равновесия механической системы
- •3.8. Закон сохранения импульса
- •3.9. Соударение двух тел
- •Глава 4. Механика твердого тела
- •4.1. Кинематика твердого тела
- •2. Кинетическая энергия при вращательном движении. Момент инерции тела
- •4.3. Основной закон динамики вращательного движения. Момент силы
- •Глава 5. Неинерциальные системы отсчета. Силы инерции
- •5.1. Неинерциальные системы отсчета. Силы инерции
- •5.2. Силы инерции при прямолинейном движении системы отсчета
- •5.3. Центробежная сила инерции
- •5.4. Сила Кориолиса
- •Глава 6. Общие вопросы теории относительности
- •1. Специальная теория относительности (релятивистская механика)
- •6.2. Общая теория относительности
- •Глава 7. Гидродинамика
- •7.1. Основные понятия гидродинамики. Уравнение неразрывности
- •7.2. Уравнение Бернулли и его следствия
- •7.3. Следствия уравнения Бернулли
- •7.3.1. Горизонтальная струя жидкости
- •7.3.2. Истечение жидкости из отверстия
- •7.4. Силы внутреннего трения
- •7.5. Ламинарное и турбулентное течения
- •7.6. Течение жидкости в круглой трубе
- •7.7. Движение тел в жидкостях и газах
- •7.8. Определение вязкости жидкости с использованием формулы Стокса
- •Часть 2. Колебания и волны
- •1. Колебательное движение. Свободные, затухающие, вынужденные колебания
- •2. Упругие волны
- •3. Уравнение упругой волны
- •Часть 3. Молекулярная физика и термодинамика
- •1.1. Агрегатные состояния вещества
- •1.2. Жидкое состояние. Поверхностное натяжение
- •1.3. Давление под изогнутой поверхностью
- •1.4. Равновесие на границе раздела: твердое тело, газ и жидкость
- •1.5. Капиллярные явления
- •Глава 2. Основы термодинамики
- •2.1. Внутренняя энергия системы
- •2.2. Первое начало термодинамики
- •2.3. Идеальный газ
- •2.3.1. Уравнение состояния идеального газа
- •2.3.2. Внутренняя энергия и теплоемкость идеального газа
- •2.4. Изопроцессы
- •2.4.1. Изотермический процесс. Закон Бойля-Мариотта
- •2.4.2. Изобарный процесс. Закон Гей-Люсака
- •2.4.3. Изохорный процесс. Закон Шарля
- •2.4.4. Адиабатический процесс
- •2.5. Газ Ван-дер-Ваальса
- •2.6. Осмос
- •1. Микро и макро состояния. Энтропия
- •2. Термодинамические потенциалы
- •2.1. Внутренняя энергия
- •2.2. Свободная энергия
- •2.3. Энтальпия
- •2.4. Термодинамический потенциал Гиббса
- •3.Тепловые двигатели
- •Глава 3. Элементарная молекулярно кинетическая теория газов
- •3.1. Характер теплового движения молекул. Распределение Максвелла по скоростям молекул
- •3.2. Давление газа на стенку. Основное уравнение молекулярно-кинетической теории газов
- •3.3. Барометрическая формула. Распределение Больцмана по энергиям молекул
- •Глава 4. Фазовые равновесия и превращения
- •4.1. Фазовые состояния и диаграммы
- •4.2.Фазовые переходы испарения и конденсации. Равновесие жидкости и насыщенного пара
- •4.3. Пересыщенный пар и перегретая жидкость
- •Часть I. Механика
- •Глава 1. Кинематика
- •Глава 2. Динамика материальной точки
- •Глава 3. Законы сохранения
- •Часть 2. Колебания и волны
- •Глава 3. Основы молекулярно кинетической теории газов
- •Глава 4. Фазовые равновесия и превращения
3.2. Давление газа на стенку. Основное уравнение молекулярно-кинетической теории газов
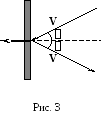
Стенки сосуда, в котором заключен газ, испытывают непрерывные соударения со стороны молекул газа. В результате этих ударов на стенку действует сила, обусловливающая давление газа. Это давление можно легко рассчитать, сделав предположение, что все молекулы имеют среднюю скорость движения. Для расчета необходимо определить силу, с которой действует на стенку одна молекула при ударе и затем умножить на число молекул, ударяющихся о единичную площадку в единицу времени. Поскольку удар молекул о стенку абсолютно упругий, он происходит по закону зеркального отражения, рис. 1. Скорость молекулы при ударе по абсолютной величине не изменяется, а проекция Vхменяется на противоположную. Согласно второму закону Ньютона сила,cкоторой одна молекула будет действовать на стенку
сосуда будет равна изменению импульса частицы:
f1х = m(dVx/dt) = 2mVx/dt . (5)
За время dtо площадку площадьюSударятся молекулы из объемаdv=Sdl=SVхdt. Если концентрация молекул газа равнаn, то число таких молекул будет
dN= (1/2)ndv= (1/2)nSVxdt. (6)
Множитель (1/2) поставлен постольку, поскольку в сторону стенки (в силу равно вероятности всех направлений) летит половина всех молекул.
Для определения давления газа на стеку осталось посчитать суммарную силу, действующую на площадку S, то есть умножить силуf1х(5) на число ударовdN(6) и поделить эту силу на площадьS. При этом надо предположить, что все молекулы имеют некоторую среднюю скоростьVх ср:
р = [(2mVx ср/dt) (1/2)nSVx срdt]/S=nmVx2 ср. (7)
Поскольку все направления движения равновероятны, можно считать, что:
Vx2 ср=Vу2 ср=Vz2 ср. (8)
Учитывая (8) и то, что
V2 ср=Vx2 ср+Vу2 ср+Vz2 ср= 3Vx2 ср(9)
выражение для давления (7) можно переписать:
р = nmVx2 ср=(nmV2 ср)/3. (10)
Или, учитывая, что (mV2 ср)2 = Ек ср– средняя кинетическая энергия молекулы
р = (nmV2 ср)/3 = (2/3)nЕк ср. (11)
Уравнения (10), (11) связывают макроскопический параметр – давление с микроскопическими: массой молекулы, концентрацией молекул и их средним квадратом скорости (концентрацией молекул и их средней кинетической энергией). Уравнение носит название основного уравнения молекулярно-кинетической теории газа.
Сопоставляя (11) и уравнение состояния идеального газа в виде p=nkTможно заключить, что
Ек ср= (3/2)kT. (12)
Считая, что молекула имеет три степени свободы поступательного движения (х, у и z), исходя из (12) говорят, что на каждую степень свободы поступательного движения молекулы приходится средняя кинетическая энергия, пропорциональная термодинамической температуре
Ек ср= (1/2)kT, (13)
где коэффициентом пропорциональности является постоянная Больцмана – k
Соотношение (12) всегда справедливо для одноатомных молекул. Если молекула состоит из двух или более атомов, свой вклад в среднюю энергию могут давать вращательные (поkT/2) иколебательные(поkT) степени свободы и в общем случае справедливо уравнение:
Ек ср= (i/2)kT, (12)
где i– общее число степеней свободы молекулы. Однако свой вклад вращательные и колебательные степени свободы дают только при высоких температурах.
