
Полезные материалы за все 6 курсов / Ответы к занятиям, экзаменам / Недзьведь_М_,_Черствый_Е_Патологическая
.pdfКлиническая картина воздушной эмболии зависит от количества и темпа поступления воздуха: медленное поступление не вызывает резких функциональных расстройств, а быстрое поступление даже относительно небольшого количества воздуха приводит к смерти. Смерть наступает от обтурации сосудов или сердца (воздух, который попадает в правую половину сердца может перекрывать (воздушный пузырь) устье легочной артерии).
Газовая эмболия развивается при высвобождении газов крови, бывших до того в растворенном состоянии, с последующей закупоркой сосудов пузырьками газа. Это наблюдается главным образом при резком снижении давления наружной среды на тело человека или животного. Кровь при этих условиях как бы вскипает. Классическим примером газовой эмболии является кессонная болезнь, когда человек работает в условиях повышенного атмосферного давления, кровь его при этом растворяет атмосферные газы в большем количестве, чем в норме. Быстрый переход от повышенного атмосферного давления в условия с нормальным давлением (водолазы, рабочие, занятые на кессонных работах при быстром подъеме с глубины) способствует высвобождению газообразного азота, углекислоты, кислорода. Закупорка капилляров происходит главным образом пузырьками азота. Газовая эмболия наблюдается в большом круге кровообращения.
Газовая эмболия лежит в основе так называемой болезни авиаторов, когда при подъеме на большие высоты масса альвеолярного воздуха диффундирует в капиллярную систему малого круга. Опасности газовой эмболии подвергаются пассажиры самолетов и космонавты при авариях и разгерметизации воздушных судов. Газовая эмболия может наблюдаться также при анаэробной гангрене. Существует мнение, что именно газовая эмболия жизненно важных органов является причиной смерти при этом заболевании.
Газовая и воздушная эмболии могут проявляться одинаково. На первый план выступают признаки асфиксии, потеря сознания, судороги. Эмболы способны привести к развитию очаговых некрозов в мозге, хорошо васкуляризированных костях и в других органах и тканях. В легких могут возникнуть отек, геморрагии, очаговые ателектазы или эмфизема, которые способствуют развитию респираторного дистресссиндрома.
Тканевая эмболия наблюдается при попадании в сосуды и перемещении комплексов клеток (клетки злокачественных опухолей – метастазы); кусочков ткани или органа (возможны отрывы и переносы с кровью частей клапанов сердца при язвенном эндокардите, кусочков разных тканей при травмах, клеток злокачественных опухолей, прорастающих сосуды); кристаллов холестерина при разрушении атеросклеротических бляшек.
90
Тканевая эмболия возможна при разрушении тканей в связи с травмой (родовая травма плода) или патологическим процессом, ведущим к попаданию кусочков тканей (клеток) в кровь. К тканевой эмболии относят также эмболию плотными частицами околоплодных вод – проникновение амниотической жидкости в материнский кровоток с последующим развитием шока и ДВС-синдрома. Это становится возможным лишь при разрыве плодных оболочек и шейки матки, некоторых случаях кесарева сечения. На вскрытии и при гистологическом исследовании наблюдаются изменения, характерные для шока, ДВС-синдрома и эмболии. В сосудах микроциркуляторного русла легких выявляются фибриновые, тромбоцитарные и гиалиновые тромбы, а также эмболы, состоящие из эпителиальных чешуек (слущенные клетки плоского эпителия кожи плода) и лануго (волоски кожи плода), а также жира и слизи. Перечисленные частицы представляют собой нормальные элементы околоплодных вод. Наличие именно этих частиц позволяет отнести эмболию околоплодными водами к тканевым эмболиям. Ранее этот вид эмболии расценивали как эмболию жидкостью.
Особую категорию тканевой эмболии составляет эмболия клетками злокачественных опухолей, так как эта эмболия лежит в основе метастазирования опухолей (от греч. metаstasis – перемещение), являющегося результатом переноса кровью эмболов, содержащих элементы, которые способны развиваться на месте переноса. Очаг, образующийся в результате такого переноса, называют метастазом.
Микробная эмболия возникает в тех случаях, когда в крови циркулируют комочки склеившихся бактерий или грибов, животных паразитов или простейших. На месте закупорки сосуда бактериальными эмболами образуются метастатические гнойники (септикопиемия как одна из форм сепсиса).
2.4. Нарушения лимфообращения
Лимфатическая система служит поддержанию метаболического равновесия между кровью и тканью. Она выполняет дренажную функцию путем всасывания из тканей воды и высокомолекулярных веществ (белки, эмульгированные липиды и др.).
Выделяют несколько видов недостаточности лимфатической системы: механическую, динамическую и резорбционную.
Механическая недостаточность лимфатической системы развива-
ется в связи с воздействием факторов, препятствующих току лимфы, что приводит к ее застою. К таким факторам относятся сдавление или закупорка лимфатических сосудов, блокада лимфатических узлов, недостаточность клапанов лимфатических сосудов.
91
Динамическая недостаточность лимфатической системы возника-
ет из-за усиленной фильтрации в капиллярах. В результате этого процесса лимфатические сосуды не в состоянии удалить всю отечную жидкость из интерстиция.
Резорбционная недостаточность лимфатической системы развива-
ется в результате изменений биохимических и дисперсных свойств белков тканей или уменьшения проницаемости лимфатических капилляров, что приводит к застою жидкости в тканях.
Однако следует отметить, что на практике в подавляющем большинстве случаев встречаются комбинированные формы недостаточности лимфообращения.
Морфологические проявления недостаточности лимфатической системы, независимо от ее формы, однотипны и представлены застоем лимфы, расширением лимфатических сосудов, развитием коллатерального лимфообращения, перестройкой лимфатических капилляров и сосудов, образованием лимфангиэктазий, коагулянтов белков (тромбов), образованием хилезного асцита, хилоторакса. Эти морфологические изменения отражают последовательные стадии недостаточности лимфатической системы. Застой лимфы и расширение лимфатических сосудов – первые проявления нарушенного лимфооттока, которые возникают, когда блокируется большая часть лимфатических сосудов. Застой лимфы приводит к включению адаптивных реакций, развитию коллатерального лимфообращения. При этом происходит не только использование резервных коллатералей, но и новообразование лимфатических капилляров и сосудов и их структурная перестройка, так как пластические возможности лимфатической системы весьма значительны.
Недостаточность лимфообращения в течение длительного времени может быть относительно компенсированной, однако, приспособление лимфатической системы в условиях застоя лимфы со временем оказывается недостаточным. Тогда большая часть капилляров и сосудов переполняется лимфой и превращается в тонкостенные широкие полости (лимфангиэктазии), в отводящих сосудах появляются многочисленные выпячивания стенок (варикозное расширение лимфатических сосудов). Эти морфологические изменения указывают на декомпенсацию лимфообращения, клиническим выражением которой является лимфогенный отек – лимфедема. В ряде случаев может возникать острая лимфедема, однако чаще она имеет хроническое течение.
Острая и хроническая лимфедема может быть общей или местной. Острая общая лимфедема встречается редко, например при двустороннем тромбозе подключичных вен. В этом случае при повышении венозного давления в полых венах и грудном протоке развивается ретроградный застой, который распространяется вплоть до лимфатических капилляров.
92
Хроническая общая лимфедема – закономерное явление при хроническом венозном застое, т.е. при хронической недостаточности кровообращения, поэтому она имеет большое клиническое значение.
Острая местная (регионарная) лимфедема возникает при заку-
порке отводящих лимфатических сосудов (например, раковыми клетками) или их сдавлении (перевязка во время операции), при остром лимфадените, экстирпации лимфатических узлов и сосудов. Обычно она исчезает при восстановлении коллатерального лимфообращения. Местная лимфедема имеет самостоятельное значение, ее разделяют на врожденную и приобретенную. Врожденная лимфедема обычно связана с аплазией или гипоплазией лимфатических сосудов нижних конечностей. Приобретенная – развивается в связи со сдавлением (опухоль) или запустеванием (хроническое воспаление, склероз) лимфатических сосудов; хроническим воспалением, склерозом или удалением большой группы лимфатических узлов (например, подмышечных при радикальной операции на молочной железе по поводу рака).
Хронический застой лимфы ведет к гипоксии тканей и поэтому обладает склерогенным действием. В условиях нарастающей гипоксии усиливаются коллагенсинтезирующая активность фибробластов и их пролиферация. Ткань, чаще кожа и подкожная клетчатка конечностей, увеличивается в объеме, становится плотной, утрачивает обычную форму и вид, т.е. возникают изменения, которые называют слоновостью (рис. 33 на цв. вкл.).
ГЛАВА 3. ВОСПАЛЕНИЕ
3.1. Определение, фазы, этиология, классификация, номенклатура
Воспаление – это компенсаторно-защитная реакция организма на воздействие патогенного агента (раздражителя), реализующаяся на микроциркуляторном уровне и направленная на элиминацию вызвавшего повреждение агента, а также некротизированных клеток и тканей. Процесс воспаления обычно заканчивается восстановлением целостности и функции поврежденной ткани.
Еще во II в. до н.э. римским ученым Aulus Celsus были описаны четыре клинических признака воспаления: rubor – покраснение, calor – повышение температуры, tumor – припухлость и dolor – боль.
Хотя воспаление играет главным образом протективную роль, в определенных условиях воспалительные процессы могут угрожать жизни пациента (перитонит, долевая пневмония).
93
Более того, хроническое воспаление лежит в основе многих хронических заболеваний, значительно ухудшающих качество жизни пациента и зачастую приводящих к инвалидизации и смерти: ревматоидный полиартрит, гломерулонефрит, хронический колит, гепатит и др.
Результатом воспаления может явиться образование рубцовой ткани
иатрофия органа, что также негативно сказывается на функции органа (цирроз печени, кардиосклероз, пилоростеноз).
Воспаление – многокомпонентный процесс, в нем участвуют циркулирующие в крови клетки, белки плазмы крови, компоненты стенки сосудов, клетки и внеклеточный матрикс тканей. Как уже упоминалось выше, обязательным компонентом любого воспаления является выход жидкости, белков плазмы и клеток из сосудистого русла в поврежденнуюткань. Выходжидкостиибелковплазмыпривоспаленииназывается «экссудацией». Этот термин следует отличать от «транссудации» – выхода жидкости и белков плазмы при отсутствии воспаления. Классическими примерами «транссудатов» являются асцит при циррозе печени, отеки нижних конечностей при хронической сердечной недостаточности, а также отек легких при острой левожелудочковой недостаточности. Выход клеток из сосудистого русла в поврежденную ткань носит название «инфильтрации». Чаще всего в воспаленной ткани определяется инфильтрация нейтрофилами, лимфоцитами, плазмоцитами или моноцитами, также может быть инфильтрация эозинофилами или базофилами.
Воспаление инициируется повреждающим агентом, который запускает механизм, приводящий к выбросу химических медиаторов (табл. 4). Медиаторы усиливают начальный воспалительный ответ и влияют на его течение путем регуляции сосудистой и клеточной реакции (рис. 34). Воспаление заканчивается, когда повреждающий агент элиминирован,
ивсе медиаторы воспаления разрушены.
Причины (этиология) воспаления:
микроорганизмы (бактерии, вирусы, паразиты, грибы); инородные тела (асбест, соли кремния, пыльца); эндогенные факторы:
–аутоантигены;
–выход крови за пределы сосудистого русла;
–диссеминированные опухолевые клетки;
–отложения эндогенных веществ в виде кристаллов (холестерин, мочевая кислота, оксалат и фосфат кальция);
деструкция тканей, вызванная:
–механическими факторами (травма);
–химическими веществами (кислоты, щелочи и др.);
–физическими факторами (действие высоких и низких температур, ионизирующее излучение).
94
Таблица 4. Основные медиаторы воспаления и их эффекты
Эффект |
Медиаторы |
Расширение сосудов |
Простагландины |
|
Оксид азота |
Повышение проницаемости сосудов |
Вазоактивные амины (гистамин, серотонин) |
|
Фракции комплемента С3а и С5а (через индук- |
|
цию выброса вазоактивных аминов) |
|
Брадикинин |
|
Лейкотриены С4, D4, Е4 |
|
Фактор активации тромбоцитов |
Хемотаксис, активация лейкоцитов |
С5а |
|
Лейкотриен В4 |
|
Микробные вещества |
|
Хемокины, например ИЛ-8 |
Лихорадка |
ИЛ-1, ИЛ-6, фактор некроза опухолей |
|
Простагландины |
Боль |
Простагландины |
|
Брадикинин |
Повреждение тканей |
Лизосомальные ферменты нейтрофилов и ма- |
|
крофагов |
|
Метаболиты кислорода |
|
Оксид азота |
|
|
Терминология и номенклатура воспаления. Наименование воспале-
ния той или иной ткани или органа образуется от их названия, к русскому названию прибавляют окончание «-ит», к латинскому или греческому – окончание «-itis». Например, воспаление головного мозга – энцефалит (encephalitis), воспаление желудка – гастрит (gastritis). Чаще используются латинские названия, реже – греческие, например воспаление мягкой мозговой оболочки – лептоменингит (leptomeningitis). Из этого правила имеются исключения, например воспаление легких называют пневмонией.
Номенклатура воспаления представлена названиями воспалительных процессов различных отделов той или иной системы организма. Например, воспаление различных отделов желудочно-кишечного тракта: хейлит, гингивит, глоссит, фарингит, эзофагит, гастрит, энтерит (дуоденит, еюнит, илеит), колит (тифлит, сигмоидит, проктит).
Классификация воспаления. Классификация воспаления учитывает его этиологию, патогенез, морфологические формы в зависимости от преобладающего типа тканевой реакции.
Знаниеэтиологиивоспалениянеобходимодляподбораадекватноголечения, особенновслучаяхтехилииныхинфекционныхзаболеваний. Привос-
95
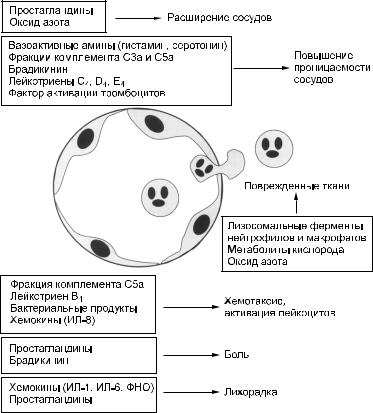
Рис. 34. Значение медиаторов воспаления
палительныхзаболеванияхснеустановленнойэтиологией лечебнаятактика определяетсяпатогенезомболезнииосновананапатогенетическихпринципах, напримеркакэтобываетприиммунопатологическихпроцессах.
Всоответствии с приведенными принципами воспаление может быть
сустановленной или неустановленной этиологией.
Хроническое воспаление бактериальной этиологии подразделяется на банальное и специфическое. Специфическим называют воспаление при следующих хронических инфекционных заболеваниях: туберкулезе, сифилисе, лепре, риносклероме и сапе.
По течению различают острое и хроническое воспаление. Острое воспаление характеризуется немедленной и ранней реакцией на пато-
96
генный фактор, короткой продолжительностью (минуты, дни), выраженной экссудативной реакцией и инфильтрацией поврежденной ткани преимущественно нейтрофилами.
Хроническое воспаление имеет большую длительность (недели, месяцы) и сопровождается инфильтрацией лимфоцитами и макрофагами, новообразованием сосудов (ангиогенез) и разрастанием соединительной ткани (фиброз). Однако нередко признаки острого и хронического воспаления могут накладываться друг на друга, что делает границу между этими двумя типами воспаления нечеткой.
При некоторых заболеваниях выделяют также подострый тип воспаления, однако критерии его достаточно условны.
По типу преобладающей тканевой реакции (морфологии) различают экссудативное и продуктивное воспаление, каждое из которых в свою очередь подразделяется на несколько видов (см. ниже при изложении отдельных видов воспаления).
Закономернымисходомлюбоготипавоспаления(особеннопродуктивного) являетсярепарация– процессвосстановленияцелостноститкани.
Репарацию трудно дифференцировать с пролиферативной фазой воспаления (они разделены лишь условно), так как пролиферация клеточных элементов, и прежде всего фибробластов, в очаге воспаления начинается уже в первые сутки после повреждения.
Различают три варианта репарации поврежденной ткани: восстанавливается в результате регенерации паренхиматозных
клеток; замещается путем заполнения дефекта соединительной тканью
(рубцевание); восстанавливается в результате комбинации перечисленных выше
процессов.
Какой вариант репарации будет в каждом случае, зависит от многих условий, но в первую очередь – от размеров повреждения и способности клеток данной ткани к пролиферации (регенерации).
3.2. Острое воспаление
Острое воспаление – форма воспалительной реакции, развивающейся немедленно после воздействия повреждающего агента. Острое воспаление характеризуется преобладанием экссудативной тканевой реакции, быстрым завершением с элиминацией повреждающего агента и репарацией ткани.
Реакция сосудов. В очаге воспаления в сосудах микроциркуляторного русла (МЦР) последовательно происходят три вида изменений:
97
транзиторная вазоконстрикция артериол – длится от нескольких секунд до нескольких минут;
вазодилатация прекапиллярных артериол – сменяетвазоконстрикцию и приводит к повышению притока артериальной крови («гиперемия»), следствием чего является местное повышение температуры и покраснение;
повышение проницаемости эндотелиального барьера – ведет к экссудации, что проявляется отеком и припухлостью.
Повышение проницаемости сосудов может быть связано с несколькими механизмами.
Сжатие эндотелиальных клеток ведет к образованию щелей в эндотелиальной выстилке венул. Это наиболее частый механизм повышения проницаемости, связанный с непосредственным влиянием медиаторов воспаления (гистамина, брадикинина, лейкотриенов и др.) на клетки эндотелия венул. Эндотелий других сосудов, например артериол и капилляров, остается интактным. Сжатие эндотелиальных клеток под воздействием медиаторов является обратимым процессом, возникает почти немедленно от момента соединения медиаторов со своими рецепторами и длится около 15–30 мин.
Сокращение эндотелиальных клеток под воздействием клеточ-
ных медиаторов (фактора некроза опухолей и интерлейкина-1) связано с реорганизацией цитоскелета эндотелиоцитов, что ведет к сокращению клетки и разрыву межклеточных контактов. Этот феномен также является обратимым, однако, в отличие от сжатия эндотелиоцитов, отмечается через 46 ч от начала действия медиаторов и длится 24 ч и более.
Прямое повреждение эндотелия (некроз эндотелия) из-за ожогов или инфекций возникает сразу после повреждения и длится до тех пор, пока поврежденные сосуды не будут тромбированы или восстановлены.
Повреждение эндотелия лейкоцитами может возникнуть при на-
коплении лейкоцитов в ходе воспалительного процесса. Лейкоциты выделяют активированные формы кислорода и протеолитические ферменты, что может приводить к повреждению эндотелия.
Потеря жидкости в сосудах при экссудации приводит к сгущению крови, что в свою очередь способствует замедлению тока крови – стазу. Микроскопически этот феномен проявляется многочисленными расширенными мелкими сосудами, переполненными эритроцитами. Возникновение стаза приводит к тому, что клетки, в первую очередь нейтрофилы, начинают аккумулироваться вдоль поверхности эндотелия сосудов – маргинация. Маргинация, или краевое стояние нейтрофилов (рис. 35 на цв. вкл.), является первым этапом миграции этих клеток в воспаленную ткань (см. ниже).
98
Инфильтрация клетками воспаления. Процесс выхода лейкоци-
тов из сосудистого русла в очаг воспаления включает последовательные стадии:
маргинацию и роллинг; адгезию и трансмиграцию между эндотелиальными клетками; хемотаксис в очаг воспаления.
Роллинг, адгезия и транмиграция опосредованы связыванием молекул адгезии (табл. 5).
Таблица 5. Молекулы адгезии эндотелиоцитов, соответствующие молекулы
лейкоцитов и значение их взаимодействия
Молекула эндотелиоцитов |
Молекула лейкоцитов |
Основная функция |
|
|
|
Р-селектин |
Sialyl-Lewis Х-модифициро- |
Роллинг (нейтрофилов, |
|
ванный белок |
моноцитов, лимфоцитов) |
GlyCam-1, CD34 |
L-селектин |
Роллинг (нейтрофилов, |
|
|
моноцитов) |
Е-селектин |
Sialyl-Lewis Х-модифициро- |
Роллинг и адгезия (нейтро- |
|
ванный белок |
филов, моноцитов, |
|
|
Т-лимфоцитов) |
VCAM-1 |
VLA-4 интегрин |
Адгезия (эозинофилов, |
(иммуноглобулиновое |
|
моноцитов, лимфоцитов) |
суперсемейство) |
|
|
ICAM-1 |
CD 11/СЕН 8 интегрины |
Адгезия, остановкаи |
(иммуноглобулиновое |
(LFA-1, Мас-1) |
трансмиграция(нейтрофи- |
суперсемейство) |
|
лов, моноцитов, лимфоцитов) |
CD31 (РЕСАМ-1) |
CD31 (РЕСАМ-1) |
Остановка и трансмиграция |
|
|
(нейтрофилов, моноцитов, |
|
|
лимфоцитов) |
Маргинация и роллинг. Из-за сгущения крови и стаза в сосудах микроциркуляторного русла лейкоциты в токе крови занимают положение вблизи эндотелия. Это приводит к тому, что определенные молекулы адгезии лейкоцитов получают возможность взаимодействовать с соответствующими молекулами на поверхности эндотелиоцитов венул, что, в свою очередь, приводит к замедлению движения лейкоцитов и роллингу, т.е. медленному качению лейкоцитов по поверхности эндотелия. Роллинг обусловлен молекулами из семейства селектинов, обеспечивающих слабую адгезию лейкоцита к эндотелию сосудов. Микроскопически этот процесс выглядит в виде «краевого стояния» лейкоцитов.
Адгезия и трансмиграция лейкоцитов. Слабая адгезия лейкоци-
тов к эндотелию сменяется плотной, обусловленной молекулами из им-
99
