
- •Технология лекарств
- •Под редакцией академика а. И. Тихонова
- •Часть первая общие вопросы технологии лекарств
- •Глава 1
- •Технология лекарств как научная дисциплина
- •Основные термины и понятия технологии лекарств
- •Понятие о лекарственой форме и лекарственном препарате
- •Глава 2 исторические данные о развитии технологии лекарств
- •Технология лекарственных препаратов в древнюю эпоху
- •Технология лекарственных препаратов в средние века (V—XII)
- •Технология лекарственных препаратов в период XIII—XVIII вв.
- •Технология лекарственных препаратов в период XIX—XX вв.
- •Глава 3 общие сведения о биофармации и ее значение для теории и практики технологии лекарств
- •Фармацевтические факторы и их содержание
- •Понятие о биологической доступности лекарственных веществ
- •Глава 4 аптека, ее задачи и функции
- •Устройство и оборудование аптеки
- •Требования к производственным помещениям и оснащению аптек
- •Глава 5 государственное нормирование производства лекарственных препаратов
- •Право на приготовление лекарственных препаратов (на фармацевтическую работу)
- •Нормирование состава прописей лекарственных препаратов
- •Нормирование качества лекарственных средств
- •Нормирование условий и технологического процесса приготовления лекарственных препаратов
- •Глава 6 лекарственные средства ядовитые и сильнодействующие лекарственные средства
- •Понятие о дозе лекарственных средств
- •Пути введения лекарственных препаратов в организм
- •Глава 7 классификация лекарственных форм
- •Классификация лекарственных форм по агрегатному состоянию, способу применения и путям введения
- •Дисперсологическая (технологическая) классификация
- •Дисперсологическая характеристика лекарственных форм по а. С. Прозоровскому
- •Глава 8 тара и укупорочные материалы, применяемые в аптечной практике
- •Материалы, применяемые для изготовления тары
- •Укупорочные материалы
- •Мойка и обеззараживание посуды
- •Глава 9 измерения по массе и объему в аптечном производстве лекарств
- •Дозирование по массе
- •Метрологические свойства весов
- •Дозирование по объему и каплями
- •Глава 10 средства механизации технологических процессов, лекарственных препаратов аптечного производства средства механизации для мытья, дезинфекции и стерилизации аптечной посуды
- •Средства механизации в технологии твердых лекарственных форм
- •Средства механизации в технологии жидких лекарственных форм
- •Средства механизации в технологии мягких лекарственных форм
- •Средства механизации в технологии инъекционных и асептических лекарственных форм
- •Средства механизации вспомогательных операций в технологии лекарственных форм
- •Технология лекарственных препаратов
- •Раздел 1 твердые лекарственные формы
- •Глава 11 порошки (pulveres) характеристика порошков
- •Классификация и способы прописывания порошков
- •Технологические стадии приготовления порошков
- •Потери твердых лекарственных веществ при растирании их в ступке № 1
- •Частная технология порошков
- •Оценка качества и совершенствование технологии порошков
- •Глава 12 сборы (species) характеристика и классификация сборов
- •Способы прописывания сборов
- •Приготовление сборов
- •Оценка качества, хранение и отпуск сборов
- •Раздел 2
- •Глава 13 общие вопросы технологии жидких лекарственных форм
- •Классификация жидких лекарственных форм
- •Технологические стадии приготовления жидких лекарственных форм
- •Оценка качества и оформление жидких лекарственных препаратов к отпуску
- •Глава 14 растворы (solutiones) общая характеристика растворов. Понятие о растворимости
- •Обозначение концентрации растворов и их прописывание
- •Водные растворы
- •Концентрированные растворы для бюреточной установки
- •Приготовление жидких лекарственных форм с использованием концентрированных растворов и сухих лекарственных веществ
- •Стандартные фармакопейные растворы
- •X Расчет: Раствора формальдегида 36,5—37,5 %
- •Неводные растворы
- •Совершенствование качества и технологии растворов
- •Глава 15 капли (guttae) характеристика капель
- •Капли для внутреннего применения (guttae pro usu interno)
- •Капли для наружного применения (guttae pro usu externo)
- •Оценка качества и совершенствование технологии капель
- •Глава 16 растворы высокомолекулярных соединений
- •Классификация высокомолекулярных соединений
- •Приготовление растворов неограниченно набухающих вмс
- •Приготовление растворов ограниченно набухающих вмс
- •Глава 17
- •Характеристика коллоидных растворов
- •Приготовление растворов защищенных коллоидов
- •Растворы полуколлоидов
- •Глава 18 суспензии (suspensiones) характеристика суспензий
- •Факторы, влияющие на устойчивость гетерогенных систем. Закон стокса
- •Способы приготовления суспензий
- •Оценка качества, хранение и совершенствование суспензий
- •Глава 19 эмульсии (emulsa) характеристика эмульсий
- •Теоретические основы образования эмульсий
- •Технология эмульсий
- •Оценка качества, хранение и совершенствование эмульсий
- •Глава 20 настои и отвары (infusa et decocta) характеристика настоев и отваров
- •Теоретические основы процесса экстракции лекарственного растительного сырья
- •Аппаратура, применяемая в технологии водных извлечений
- •Технология водных извлечений
- •Особые случаи приготовления водных извлечений. Авторские прописи
- •Технология водных извлечений с использованием экстрактов-концентратов
- •Оценка качества, хранение и совершенствование водных извлечений
- •Раздел 3 мягкие лекарственные формы
- •Глава 21 линименты (linimenta)
- •Характеристика и классификация линиментов
- •Общие правила приготовления линиментов
- •Частная технология линиментов
- •Контроль качества, хранение и совершенствование технологии линиментов
- •Глава 22 мази (unguenta) характеристика и назначение мазей
- •Классификация мазей
- •Основы для мазей, требования к ним и их классификация
- •Гидрогенизированного сульфожира 8,0
- •Прописывание мазей
- •Общие правила приготовления мазей
- •Частная технология мазей
- •Концентраты и полуфабрикаты для приготовления мазей
- •Подготовка вспомогательных веществ
- •Совершенствование технологии мазей
- •Глава 23 суппозитории (suppositoria) характеристика суппозиториев
- •Суппозиторные основы
- •Прописывание суппозиториев
- •Технология суппозиториев
- •Приготовление суппозиториев на гидрофобных основах.
- •Коэффициенты замещения жировых и желатино-глицериновой основ для некоторых лекарственных веществ
- •Количество лекарственных веществ и основы, необходимое для приготовления 30 суппозиториев методом выливания в формы емкостью 2 см3
- •Оценка качества и хранение суппозиториев
- •Совершенствование технологии суппозиториев
- •Глава 24 пилюли (pilulae) характеристика пилюль
- •Вспомогательные вещества
- •Общие правила приготовления пилюль
- •Прописывание пилюль
- •Частная технология пилюль
- •Контроль качества, хранение и отпуск пилюль
- •Раздел 4 стерильные и асептически приготовляемые лекарственные формы
- •Глава 25 лекарственные формы для инъекций характеристика лекарственных форм для инъекций
- •Растворители
- •Организация работы в асептических условиях
- •Перечень лекарственных веществ, к которым предъявляются дополнительные требования
- •Стерилизация
- •Характеристика термоиндикаторов
- •Технология растворов для инъекций и контроль их качества
- •Журнал регистрации отдельных стадий изготовления инъекционных растворов1
- •Стабилизация растворов для инъекций
- •Частная технология растворов для инъекций
- •Изотонические растворы
- •Плазмозаменяющие (физиологические) растворы
- •Растворы для инъекций на неводных растворителях
- •Хранение и отпуск инъекционных лекарственных форм
- •Совершенствование технологии инъекционных лекарственных форм
- •Глава 26
- •Глазные лекарственные формы
- •Характеристика глазных
- •Лекарственных форм
- •Глазные капли (guttae ophtalmicae)
- •Глазные мази (unguenta ophtalmica seu oculenta)
- •Контроль качества, хранение и отпуск глазных лекарственных форм
- •Совершенствование технологии глазных лекарственных форм
- •Глава 27 лекарственные формы с антибиотиками характеристика антибиотиков
- •Технология лекарственных форм с антибиотиками
- •Оценка качества, хранение и отпуск лекарственных форм с антибиотиками
- •Совершенствование технологии лекарственных форм с антибиотиками
- •Глава 28
- •Особенности применения и назначения лекарственных препаратов для детей
- •Особенности технологии, контроля, хранения и отпуска лекарственных препаратов для детей
- •Особенности применения некоторых препаратов при лечении детей и беременных женщин
- •Совершенствование лекарственных форм для детей
- •Раздел 5 затруднительные и несовместимые сочетания лекарственных средств
- •Глава 29
- •Затруднительные случаи приготовления лекарств
- •Характеристика кажущихся несовместимостей
- •Глава 30 несовместимые сочетания лекарственных средств
- •Классификация несовместимостей
- •Взаиморастворимость (смешиваемость) отдельных растворителей1
- •Влияние относительной влажности воздуха на отсыревание порошков
- •Перечень лекарственных веществ, которые в виде порошков отпускаются в вощеных капсулах
- •Химические несовместимости
- •Осаждение алкалоидов-оснований и синтетических азотистых оснований из водных растворов их солей
- •Совместимость солей алкалоидов и азотистых оснований с щелочными веществами в микстурах
- •Совместимость солей алкалоидов и азотистых оснований с бензоатами, салицилатами, бромидами и йодидами (а. А. Фелсберг, в. А. Шидловска)
- •Несовместимость витаминов с некоторыми лекарственными веществами
- •Фармакологические несовместимости
- •Раздел 6
- •Глава 31 гомеопатические лекарственные препараты определение и история развития гомеопатии
- •Принципы гомеопатии. Механизм действия гомеопатических лекарств
- •Технология гомеопатических лекарственных форм
- •Частная технология гомеопатических лекарственных форм
- •Гомеопатических препаратов
- •Совершенствование гомеопатических лекарственных препаратов
- •Глава 32 ветеринарные лекарственные препараты характеристика ветеринарных лекарственных форм
- •Технология ветеринарных лекарственных форм
- •Совершенствование ветеринарных лекарственных форм
- •Глава 33 косметические препараты
- •Классификация косметических препаратов
- •Жировые (неэмульсионные) кремы
- •Эмульсионные кремы
- •Густые эмульсионные кремы
- •Крем ланолиновый
- •Состав ланолиновых кремов на восковом мыле и на стеаратах калия и натрия, %
- •Жидкие эмульсионные кремы Кремы на аммиаке и буре (примерная рецептура)
- •Эмульсионные кремы типа м/в (жидкие)
- •Жидкие кремы на холестерине и триэтаноламиностеарате
- •Оценка качества и совершенствование косметических препаратов
- •Часть первая общие вопросы технологии лекарств
- •Часть вторая
- •Р а з д е л 1 твердые лекарственные формы
- •Р а з д е л 2 жидкие лекарственные формы
- •Р а з д е л 3 мягкие лекарственные формы
- •Лекарственные формы
- •Затруднительные и несовместимые сочетания лекарственных средств
- •Тихонов Олександр 1ванович ярних Тетяна Григор1вна
Теоретические основы образования эмульсий
Эмульсии — термодинамически неустойчивые системы. Задача приготовления агрегативно устойчивых эмульсий сводится, в основном, к подысканию наиболее эффективного эмульгатора для данного сочетания компонентов.
Эмульгаторы — это дифильные ПАВ, ориентированно распределяющиеся на границе раздела двух жидкостей. Их условно классифицируют по структуре и свойствам молекул, механизму действия, медицинскому назначению (схема 8).
Эмульгаторы всегда должны являться достаточно высокими представителями гомологических рядов и иметь в составе молекул как гидрофильные, так и гидрофобные части, различные по объемам (площадям) занимаемой поверхности и должны быть сбалансированы в том смысле, что полярная часть должна обладать сильным сродством к воде, чтобы обусловливать достаточную растворимость вещества и сильную гидратацию, а углеводородная часть должна быть достаточно развита, например, углеводородная цепь должна обладать достаточной длиной, чтобы обеспечивать образование мицелл сцеплением углеводородных групп, а при больших концентрациях раствора и в адсорбционном слое приводить к развитию гелеобразных структур. Этим требованиям удовлетворяют жировые мыла, а также в различной степени другие мылообразные эмульгаторы — щелочные соли соответствующих органических кислот: нафтеновые мыла, смоляные (канифольные) мыла, а также алкил- и алилсульфаты и соответствующие сульфоновые кислоты как в кислом виде, так и в виде щелочных солей. Кроме таких поверхностно-активных коллоидных электролитов, являющихся анионоактивными, хорошо известны и катионоактивные мыла, типичными представителями которых являются неорганические, например солянокислые, соли соответствующих азотосодержащих органических оснований как жирного, так
Ионогенные
ПАВ
Катионные
Анионные
Соли
аммониевых, сульфо-ниевых, фосфо-ниевых
кисл от
Мыла
и ароматического ряда. Все подобные мылообразные вещества являются обычно эффективными смачивателями, пенообразователями, эмульгаторами и пептизаторами и имеют большое значение в фармации для технологии лекарств (см. с. 284 «Классификация ВМС»).
При выборе эмульгаторов для стабилизации эмульсий необходимо учитывать механизм их стабилизации, токсичность, величину рН, химическую совместимость с лекарственными веществами. Эмульгатор добавляют в количестве от 0,1 до 25 %.
О поверхностно-активных свойствах эмульгаторов можно судить по величине гидрофилъно-липофилъного баланса (ГЛБ). ГЛБ — это соотношение гидрофилъных и гидрофобных групп в молекуле, значение которого выражается определенным числом. Так, ПАВ с ГЛБ 1,5—3 — пеногасители, 3—6 — эмульгаторы типа В/М, 7—9 — смачиватели, 8—18 — эмульгаторы типа М/В, 13—15 — пенообразователи, 15—18 — солюбилизаторы. По величине ГЛБ эмульгаторов можно характеризовать тип образующейся эмульсии.
Относительно теории образования эмульсий и механизма стабилизирующего действия эмульгаторов существовало несколько научных представлений этого процесса. Например, теория объема фаз (W. Ostwald), теория вязкости (H. N. Holmes, W. D. Child), гидрата-ционная теория (R. Fischer), теория снижения межфазного поверхностного натяжения (I. Langmuir, W. D.Harkins и др.). Логическим продолжением последней теории является теория образования адсорбционной оболочки на поверхности дисперсной фазы (G. Clowes, W. Bancroft и др.). Современные положения этой теории впоследствии были развиты отечественными учеными (П. А. Ребиндер и др.), согласно которой механизм стабилизирующего действия эмульгаторов заключается в том, что они, адсорбируясь на границе фаз, понижают поверхностное натяжение и накапливаются на поверхности раздела, а главное, обволакивая капельки диспергируемого вещества, образуют адсорбционную пленку, которая обладает механической прочностью, препятствует образованию крупных частиц, слиянию капелек в сплошной слой (коалесценции) и сообщает эмульсии устойчивость (она как бы бронирует капли дисперсной фазы). Школой академика Ребиндера экспериментально доказано, что образовавшаяся пленка — основной фактор стабилизации эмульсий. Защитные пленки могут состоять из одного или нескольких молекулярных слоев эмульгатора (моно- или полимолекулярные пленки).
При приготовлении эмульсии в процессе смешивания компонентов эмульгатор концентрируется на поверхности раздела двух не-смешивающихся жидкостей. В процессе дальнейшего технологического процесса происходит образование соответствующего типа эмульсии, который зависит от типа эмульгатора, определяющего значения величин поверхностных натяжений по обе стороны образовавшейся оболочки, создаваемых соответствующим количеством (площадями) гидрофильной и гидрофобной частями данного поверхностно-активного вещества (рис. 116, 2).
 Так,
например, мыла с одновалентными катионами
коллоидно растворимы в воде, но не в
масле, что позволяет образовывать
оболочку, лучше смачиваемую водой,
чем маслом, поэтому поверхностное
натяжение ниже со стороны воды, чем со
стороны масла. Так как внутренняя
поверхность оболочки, окружающей шарик,
меньше внешней, оболочка стремится
выгнуться так, чтобы обволакивать
каплю масла, находящуюся в воде (рис.
116, 1). Вследствие этого поверхность с
более высоким поверхностным натяжением
уменьшается до минимума по сравнению
с поверхностью, обладающей менее высоким
поверхностным натяжением. С другой
стороны, оболочка мыла с двух- и
трехвалентными катионами (такие мыла
коллоидно растворимы в масле, но не в
воде) лучше смачивается маслом, чем
водой. В этом случае поверхностное
натяжение со стороны масла ниже, чем
со стороны воды, и оболочка стремится
выгнуться так, чтобы обволакивать капли
воды, находящиеся в объеме масляной
фазы. Эти представления схематически
изображены Ж. Клоусом и А. И. Тихоновым
(рис. 116, 3).
Так,
например, мыла с одновалентными катионами
коллоидно растворимы в воде, но не в
масле, что позволяет образовывать
оболочку, лучше смачиваемую водой,
чем маслом, поэтому поверхностное
натяжение ниже со стороны воды, чем со
стороны масла. Так как внутренняя
поверхность оболочки, окружающей шарик,
меньше внешней, оболочка стремится
выгнуться так, чтобы обволакивать
каплю масла, находящуюся в воде (рис.
116, 1). Вследствие этого поверхность с
более высоким поверхностным натяжением
уменьшается до минимума по сравнению
с поверхностью, обладающей менее высоким
поверхностным натяжением. С другой
стороны, оболочка мыла с двух- и
трехвалентными катионами (такие мыла
коллоидно растворимы в масле, но не в
воде) лучше смачивается маслом, чем
водой. В этом случае поверхностное
натяжение со стороны масла ниже, чем
со стороны воды, и оболочка стремится
выгнуться так, чтобы обволакивать капли
воды, находящиеся в объеме масляной
фазы. Эти представления схематически
изображены Ж. Клоусом и А. И. Тихоновым
(рис. 116, 3).
Межфазный слой состоит из одного ряда молекул, обращенных своей полярной частью к воде, а неполярной — к маслу. Полярные группы и углеводородные радикалы сольватируются одновременно водной и масляной фазами, и такой адсорбционно-сольватный слой обладает известной механической прочностью.
Тип образующейся эмулъсии зависит от растворимости эмульгатора в той или иной фазе. Дисперсионной средой становится та фаза, в которой эмульгатор преимущественно растворяется. Отсюда следует, что для получения устойчивых эмульсий типа М/В необходимо применять гидрофильные эмульгаторы (с ГЛБ 8—18) — камеди, белки, щелочные мыла, слизи, пектины, сапонины, некоторые растительные экстракты, полиоксиэтиленгликолевые эфиры высших жирных спиртов, кислот, спенов (твин-80, препарат ОС-20) и др.
Для получения устойчивых эмульсий типа В/М необходимо применять олеофильные эмульгаторы (с ГЛБ 3—6) — ланолин, производные холестерина, фитостерин, природные соли, цетиловый и ми-рициловый спирты, магниевое и алюминиевое мыла, окисленные растительные масла, пентол, эмульгатор Т-2, моноглицериды дистили-рованные (МГД), многие синтетические вещества. Эти эмульгаторы находят применение в аптечной практике только при приготовлении лекарств для наружного применения.
Доказано, что наиболее устойчивые эмульсии образуются эмульгаторами, которые обладают способностью образовывать студенистые или вязкие пленки.
Синергизм и антагонизм эмульгаторов. Обращение фаз. При получении эмульсий иногда применяются комбинированные эмульгаторы. Например, смесь аравийской камеди и трагаканта. В этом случае удается достигнуть повышения степени дисперсности и стойкости эмульсий, то есть наблюдается синергизм эмульгаторов (одно вещество усиливает действие другого). Однако, следует учитывать, что в зависимости от свойств эмульгатора эмульсии могут разрушаться, тогда эмульгаторы действуют как антагонисты.
Если к эмульсии типа М/В добавить эмульгатор противоположного типа, то один тип эмульсии может перейти в другой, то есть эмульсия типа М/В может превратиться в эмульсию типа В/М. То же может произойти и при значительном избытке эмульгированной фазы. Такое явление называют обращением фаз эмульсий. При этом вначале образуются оба типа эмульсий, но затем остается или преобладает одна наиболее устойчивая система. Для повышения устойчивости (стабильности) эмульсий иногда совмещают эмульгаторы противоположного типа. Например, в эмульсию типа М/В, стабилизированную олеатом натрия, прибавляют до 1 % хлорида кальция или алюминия. При этом в результате реакции обмена часть ионов натрия в олеате натрия замещается на ионы кальция или алюминия с образованием эмульгатора противоположного типа и поэтому наряду с эмульсией прямого типа М/В образуется эмульсия противоположного типа В/М, то есть в эмульсии типа М/В частицы масла будут представлять не чистое масло, а эмульсию типа В/М, которая равномерно распределена в водной фазе. Из-за малого количества эмульгатора противоположного типа обращения фаз здесь не наблюдается, однако значительно повышается стабильность таких эмульсий и их устойчивость к высыханию. Классическим примером устойчивости эмульсий за счет присутствия эмульгатора прямого и противоположного типов является молоко и сливочное масло.
Применяемые для приготовления аптечных эмульсий коллоидные эмульгаторы, как правило, дают прочные пленки гелеобразной структуры, механические свойства которой способны препятствовать ее прорыву, необходимому для коалесценции.
Факторы, влияющие на стабильность эмульсий. Эмульсии должны обладать физической, химической и микробиологической стабильностью.
Для физической стабилъности эмульсии весьма важно, чтобы вводилось достаточное количество эмульгатора. Необходимо иметь в виду, что определенное количество эмульгатора может насытить лишь определенную поверхность. Это означает, что при недостаточном количестве эмульгатора будет невелика и степень дисперсности. Шарики масла в этом случае получаются настолько крупными, что пленка не в состоянии выдержать тяжести шарика и прорывается. Поэтому необходимо, чтобы для каждого эмульгатора и масла были известны оптимальные соотношения, которые обеспечили бы необходимую степень дисперсности и стабильность эмульсии. Устойчивость эмульсии зависит не только от свойств применяемого эмульгатора, но и от степени дисперсности фазы. Чем ближе плотность дисперсной фазы к плотности дисперсионной среды, тем меньше межфазное поверхностное натяжение, тем выше вязкость дисперсионной среды, тем устойчивее эмульсия.
Размер капелек дисперсной фазы зависит от величины снижения поверхностного натяжения на границе раздела фаз и от величины
энергии, которая затрачена на измельчение частиц дисперсной фазы. Особенно большую устойчивость эмульсии получают в результате гомогенизации, то есть при дополнительно энергичном механическом воздействии на готовую эмульсию. При гомогенизации не только повышается дисперсность эмульсии, но она становится монодисперсной, что значительно повышает ее устойчивость.
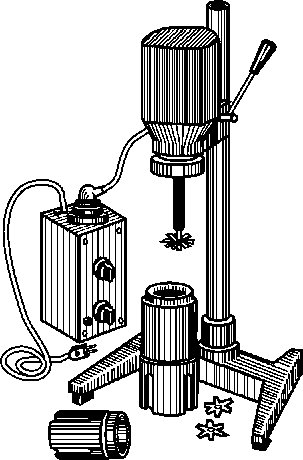
Гомогенизация эмульсии производит- ся с помощью специального прибора — гомогенизатора (рис. 117). Для этого гру- бодисперсную эмульсию пропускают под большим давлением сквозь имеющиеся в гомогенизаторе узкие каналы. В этом рис. П7. ГоМогеНизатор типа случае крупные капли дисперсной фазы МР-302 разрушаются и получается тонкодиспер- сная эмульсия. При этом диаметр капель может уменьшиться в десятки раз по сравнению с начальным.
Химическая стабилъностъ эмульсий определяется стабильностью лекарственных веществ, отсутствием химических реакций между ингредиентами эмульсий.
Химическая неустойчивость может отражаться на физической стабильности эмульсий (разрушение вследствие омыления, окисления, гидролиза, составных компонентов, их взаимодействия между собой и материалом упаковки).
С целью химической стабилизации эмульсий их сохраняют в упаковке из инертных материалов в прохладном месте, защищенном от воздействия света и воздуха, вводят антиоксиданты (бутилокситолу-ол, бутилоксианузол, пропилгаллат и др.).
Микробиологическая стабилъностъ эмульсий является важным требованием, определяющим их качество. При приготовлении эмульсий (как и других лекарственных форм) необходимо соблюдать все меры по обеспечению микробной чистоты лекарственных и вспомогательных веществ.
