
- •Введение
- •Термодинамические параметры состояния
- •2. Основные понятия и определения
- •Идеальный газ. Законы идеального газа
- •Закон Бойля – Мариотта
- •Закон Гей – Люссака
- •Закон Шарля
- •3. Уравнение состояния идеального газа
- •Закон Авогадро
- •Молярная масса
- •4. Уравнение менделеева – клапейрона
- •Уравнение состояния реальных газов
- •5. Газовые смеси
- •6. Первое начало термодинамики Теплота и работа
- •Принцип эквивалентности
- •7. Внутренняя энергия
- •Закон сохранения и превращения энергии
- •Формулировки первого начала термодинамики
- •Виды работ
- •Развернутое уравнение первого закона термодинамики и его частные выражения
- •Энтальпия
- •8. Теплоемкость газов
- •9. Анализ термодинамических процессов на основании I начала термодинамики Понятие об энтропии
- •Схемы распределения энергии
- •Изотермический процесс
- •Адиабатный процесс
- •10. Политропные процессы
- •Группы политропных процессов
- •Способы определения n
- •Связь между n и с
- •11. Второе начало термодинамики Односторонность протекания самопроизвольных процессов
- •Формулировки второго начала термодинамики
- •Выражение первого закона термодинамики для циклов
- •Термический коэффициент полезного действия прямого цикла
- •12. Цикл карно
- •Термодинамическая шкала температур
- •Математическое выражение второго закона термодинамики
- •Критика учения о «тепловой смерти вселенной»
- •13. Термодинамика потока газа. Основные понятия и уравнения гидрогазодинамики
- •Уравнение неразрывности
- •Уравнение энергии – уравнение первого закона термодинамики
- •Уравнение состояния идеального газа
- •Уравнение импульса
- •Располагаемая работа газа в потоке
- •Скорость звука и критические параметры
- •14. Скорость и расход газа при течении. Истечение из сужающихся сопел
- •Переход через скорость звука. Сопло Лаваля
- •После подстановки значения скорости потока в последнее уравнение получим .
- •Истечение при наличии трения
- •Дросселирование газа
- •15. Термодинамика химических процессов
- •Термохимические процессы
- •Первый закон термодинамики применительно к химическим процессам
- •Закон Гесса
- •Второй закон термодинамики
- •Тепловой закон Нернста
- •16. Циклы поршневых двигателей внутреннего сгорания
- •Цикл со смешанным подводом тепла
- •Цикл с подводом тепла при постоянном объеме
- •Цикл с подводом тепла при постоянном давлении
- •Сравнение циклов поршневых двс
- •Сравнение по условию .
- •Сравнение по условию
- •17. Циклы компрессоров
- •Многоступенчатые компрессоры
- •Центробежный компрессор
- •Осевой компрессор
- •18. Циклы газотурбинных установок
- •Регенеративные циклы
- •19. Циклы паросиловых установок
- •Цикл Карно для водяного пара
- •Цикл Ренкина
- •Цикл с промежуточным перегревом пара
- •Регенеративный цикл
- •Бинарные циклы
- •Цикл парогазовой установки
- •Теплофикационный цикл
- •20. Циклы холодильных установок
- •Цикл воздушной холодильной машины
- •Цикл парокомпрессорной холодильной машины
- •Цикл теплового насоса
- •Детандеры
- •21. Реактивные двигатели
- •Цикл ПуВрд
- •Цикл трд
- •22. Ракетные двигатели
- •Цикл рдтт
- •Цикл жрд
- •Цикл ярд
- •Заключение
- •Библиографический список
- •Оглавление
- •394026 Воронеж, Московский просп., 14
Группы политропных процессов
Несмотря на большое разнообразие политропных процессов, они по характеру преобразования энергии могут быть разбиты на три группы.

Рис. 10.2. Группа № 1

Рис. 10.3. Группа № 2

Рис. 10.4. Группа № 3
Коэффициент распределения тепла:![]() ,
т.к.
,
т.к.
![]() ,
то
,
то ![]() - в политропных процессах постоянен.
- в политропных процессах постоянен.
Доля теплоты, расходуемой на совершение
работы,
 .
Доля внутренней энергии, расходуемой
на совершение работы
.
Доля внутренней энергии, расходуемой
на совершение работы
![]() .
.
Схема распределения энергии для каждой из трех групп одинаковы.
Сплошные стрелки соответствуют процессам расширения, а пунктирные – процессам сжатия.
Области расположения в – и TS – координатах заштриховали области процессов расширения.
Каждой
из групп соответствуют следующие
диапазоны изменения показателя политропы
n:
для группы 1:![]() ,
для группы 2:
,
для группы 2:
![]() ,
для группы 3:
,
для группы 3:
![]() .
.

Рис. 10.5. Диапазоны изменения показателя политропы № 1

Рис. 10.6. Диапазоны изменения показателя политропы № 2

Рис. 10.7. pv-диаграмма
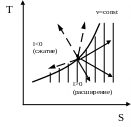
Рис. 10.8. TS-диаграмма
При составлении схемы любого политропного процесса, расположение которого в спектре политроп и направление известны, необходимо установить, какие знаки (положительные или отрицательные) имеют составляющие энергии q, u, l.
При этом следует иметь в виду, что области процессов сжатия и расширения разграничивает изохора, проведенная через начальную точку процесса.

Рис. 10.9. pv-диаграмма

Рис. 10.10. TS-диаграмма
Здесь заштрихованы области расширения где работа положительна. Области процессов с подводом и отводом тепла разграничивает адиабата
Н а
графиках заштрихованы области, где
тепло подводится (q
>0).
а
графиках заштрихованы области, где
тепло подводится (q
>0).
Рис. 10.11. pv-диаграмма

Рис. 10.12. TS-диаграмма
Области процессов с увеличением и уменьшением внутренней энергии разграничивает изотерма.
Заштрихованы
области процессов с увеличением
внутренней энергии (![]() ).
).

Рис. 10.13. Политропный процессы различных степеней

Рис. 10.14. Политропный процесс сжатия
Пример: Составить схему распределения энергии для политропного процесса сжатия с n=10. Для решения необходимо определить расположение процесса на графике в системе - или TS- координат. Политропа сжатия с n=10 расположена между адиабатой (n=k) и изохорой и направлена влево (по стрелке на рис. 10.13).
Процесс расположен выше изотермы и выше
адиабаты, т.е. в области процессов с
подводом тепла (q>о)
и в области процессов c
увеличением внутренней энергии (
).
По условию l<0 .
Полученному сочетанию знаков q,
![]() и l соответствует
схема, представленная на рис. 10.14.
и l соответствует
схема, представленная на рис. 10.14.
