
- •Глава I
- •§ 1. Предмет термодинамики и основные черты
- •§ 2. Виды энергии и формы обмена энергией
- •§ 3. Термодинамическая система, окружающая среда и взаимодействие между нмми
- •§ 4. Состояние термодинамической системы, параметры!
- •§ 5. Внутренняя енергия термодинамической системы
- •§ 6. Термодинамические процессы .
- •Глава III
- •§ 13. Понятие о разновесных и обратимых
- •IpOTbl.
- •§ 14. Термодинамический анализ круговых'' процессов (циклов)
- •§ 15. Цикл Карно
- •§ Is. Термический кпд цикла Карно.
- •§ 13. Изменение энтропии в произвольных
- •§ 19. Статистический смысл второго закона термодинамики
- •§ 29. Общая математическая формулировка второго закона
- •§ 23. Свойства характеристических функций
- •§ 31. Фазовая Тр-диаграмма
- •§ 32. Фазовые переходы 2-го рода
- •§ 33. Термодинамические характеристики идеального газа
- •Глава VIII
- •§ 44. Задачи изучения термодинамических процессов
- •§ 45. Изохорный процесс
- •§ 46'. Изобарный процесс
- •Рис, 23, Изобарный процесс:
- •§ 47. Изотермный процесс
- •Глава IX
- •§ 50. Качественные особенности реальных газов
- •§ 51. Уравнение состояния реальных газов
- •§ 52. Уравнение Ван-дер-Ваальса
- •§ 53. Получение пара
- •§ 54. Термодинамические свойства поверхности раздела фаз
- •§ 58. Термодинамические процессы изменения состояния пара
- •§ 60. Температура мокрого термометра
- •§ 62. Смешение потоков влажного воздуха
- •§ 63. Определение влажности воздуха по температурам мокрого и сухого термометров
- •§ 64. Кондиционирование воздуха
- •Глава XII
- •§ 65. Задание состава сложной системы
- •§ 84. Определение параметров состояния и состава рабочих тел и продуктов сгорания
- •Глава XV
- •§ 85. Состав и парциальные молярные свойства растворов
- •§ 86. Уравнение Ван-дер-Ваальса для бинарных систем
- •§ 89. Первый и второй законы Коновалова
- •§ 90. Реальные и многокомпонентные растворы
- •Глава XVI
- •§ 91. Установившееся одномерное течение газов
- •§ 92. Основные уравнения истечения
- •§ 95. Влияние трения на процессы истечения' из. Сопл и диффузоров
- •§ 97. Нерасчетный режим истечения через соппо Лаааля
- •1| § 98. Скачки уплотнения
- •§ 99. Процессы в эжекторах -
- •Глава XVII
- •§ 101. Основные уравнения истечения газа из сосуда
- •§ 120. Паровой цикл Карно
- •§ 121. Теоретический паросиловой цикл (цикл Ренкина)
- •§ 122. Расширение пределов рабочего процесса
- •§ 124. Бинарные циклы 1
- •§ 125. Регенеративный цикл паротурбинной установки
- •§ 126. Циклы атомных энергетических установок
- •§ 127. Циклы парогазовых установок
- •Глава XXII
- •§ 129. Понятие об обратных термодинамических циклах.1
- •§ 130. Разновидности обратных термодинамических циклов и
- •§ 131. Газовые холодильные машины
- •§ 132. Парокомпрессионные холодильные машины
- •§ 133. Абсорбционные холодильные машины
- •§ 134. Тепловой насос и термохимический j
- •§ 135. Получение сжиженных газов
- •§ 142. Эксергетический анализ работы тепловых машин
- •§ 148. Термодинамические параметры плазмы
§ 3. Термодинамическая система, окружающая среда и взаимодействие между нмми
Объектом изучения в термодинамике является термодинамическая система, представляющая собой совокупность взаимодействующих макроскопических тел. ■
В метеоро-логи-и«такой системой, например, является земная атмосфера, в энергетике — весь комплекс машин и устройств электрической станции или отдельный узел теплового двигателя и т. д.
Объектам научения в технической термодинамике весьма часто является какое-либо вещество, выполняющее главную функцию в тепловой машине: пар, продукты сгорания топлива, сжатый газ и т. п. Такое вещество также является термодинамической системой и называется рабочим телом машины или термодинамической системы.
Все тела, ие входящие в состав изучаемой термодинамической системы, объединяются общим понятием «окружающая среда». Границу между термодинамической системой и окружающей средой часто называют контрольной поверхностью. Это условное поня- Рис. 1. Термодинамические системы:
тие, которое в ряде случаев мо ^Хр^ческоГТ ЖДГиоГойГ Т-
жет геометрически совпадать С открытая проточная (газ в канале между ло-
„„«. „„,», j,„„„„ латками турбины); в — сложная с четырьмя
некоторой реальной физическои степенями свободы (термической, деформаци- поверхностыо. Например, КОНТ- 011 иой- электрической И магиитиой)
рольная поверхность для газа
совпадает с внутренними поверхностями поршня и цилиндра (рис. 1, а). Контрольная поверхность системы 5 на рис, I, б частично проходит через сечения А—А и Б—Бг и на этих участках она является условной, воображаемой.
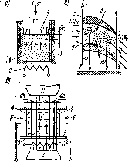
ре 3 с подвижным поршнем 4 (рис. 1, а). Энергию газа можно увеличить, передавая ему некоторое количество механической работы, используя механическую или деформационную степень свободы (перемещение вниз поршня 4 внешней силой). Вторая степень свободы (тепловая или термическая) проявляется при изменении энергии за счет подвода некоторого количества теплоты от нагревателя 2 через стенку цилиидра 3. Системы, обладающие двумя степенями свободы (термической и деформационной), называют простыми или термодеформа- цивнными. На рис. 1, в представлена схема сложной термодинамической системы с четырьмя степенями свободы: деформационной, термической, электрической и магнитной. Рабочим телом этой системы служит газ с диэлектрическими и парамагнитными свойствами (например, кислород). Его энергию можно изменить сжатием, подводом теплоты, изменением электрического заряда на поршнях 4, являющихся одновременно обкладками конденсатора, и намагничиванием во внешнем магнитном поле.
В технической термодинамике обычно рассматриваются простые системы.
Характер взаимодействия между термодинамической системой и окружающей средой зависит также от свойств контрольной поверхности. Система называется закрытой (замкнутой), если контрольная поверхность непроницаема для вещества, т. е. между системой- и средой отсутствует обмен массой (рис. 1, а, в). Открытой система называется в том случае, когда при взаимодействии через контрольную поверхность переходит вещество. Частным случаем открытой системы является так называемая проточная система, когда на одних участках контрольной поверхности вещество входит в систему, а на других — выходит из нее (рис. 1,6).
Термодинамическая система называется изолированной, если контрольную поверхность не могут пересекать ни потоки вещества, ни потоки энергии. Понятие изоляции является научной абстракцией, т. е. изоляция считается идеальной. Практически идеальной является только деформационная изоляция газа от обмен а. механической работой (при заключении его в жесткий сосуд или в цилиндр с закрепленным поршнем). Существуют также способы создания весьма совершенной тепловой изоляции. Иногда, говорят о частично изолированных системах. Прй этом имеется в виду наличие обмена энергией лишь по некоторым из присущих системе степеней свободы. Системы, находящиеся в тепловой изоляции и не-обменивающиеся с окружающей средой теплотой, называются адиабатными.
