
- •Билет № 1
- •Принципы классификации дисперсных систем
- •Потенциал и ток течения
- •Поверхностно-активные вещества и их классификация
- •Билет № 2
- •Молекулярно-кинетические свойства дисперсных систем
- •Электрофорез
- •Адсорбционный потенциал
- •Билет № 3
- •Билет 3. Седиментация суспензий и седиментационно-диффузионное равновесие
- •Электроосмос
- •Теория быстрой коагуляции Смолуховского
- •1. Оптические свойства дисперсных систем
- •2. Зависимость ψ1-потенциала от концентрации электролита
- •3. Правило уравнивания полярностей Ребиндера
- •Билет № 5
- •Билет № 6
- •Строение двойного электрического слоя (дэс) на границе раздела твердое тело – жидкость. Потенциалы дэс.
- •Защитное действие растворов высокомолекулярных соединений
- •Билет № 7
- •Билет 7. Химический потенциал и давление пара у искривленных поверхностей
- •Механизмы образования двойного электрического слоя на поверхности твердых тел
- •Влияние многозарядных ионов на устойчивость гидрофобных коллоидов
- •Билет № 8
- •Уравнение адсорбции Гиббса
- •Числа переноса ионов в капиллярных системах
- •Электрокинетический потенциал и его роль в устойчивости гидрофобных коллоидов
- •Билет 9. Изотерма адсорбции Ленгмюра (адсорбция на границе раздела раствор - газ)
- •Основные положения теории двойного электрического слоя Гуи-Чепмена, модифицированной теории Гуи, теории Штерна.
- •Лиофильные коллоидные системы
- •Билет № 10
- •Поверхностные пленки нерастворимых веществ
- •Индифферентные и специфически сорбирующиеся электролиты. Влияние на устойчивость гидрофобных коллоидов
- •3. Поверхностная проводимость
- •Билет № 11
- •Адсорбция на поверхности твердых тел. Теплоты адсорбции и смачивания
- •Методы определения размеров частиц
- •Приведенная толщина диффузного слоя; зависимость от вида электролита
- •Билет № 12
- •Теория адсорбции Ленгмюра (граница раздела твердое тело – газ или пар)
- •Электрокинетический потенциал; влияние концентрации электролита и заряда противоиона
- •Поверхностное натяжение и способы его определения
- •Билет № 13
- •Теория адсорбции Поляни
- •Коллоидно-химические основы охраны окружающей среды
- •Электрокинетический потенциал
- •Билет № 14
- •Теория адсорбции Брунауэра – Эммета – Теллера
- •Высокомолекулярные электролиты
- •Правило уравнивания полярностей Ребиндера
- •Билет № 15
- •Адсорбция неэлектролитов на границе раздела твердое тело – жидкость (молекулярная адсорбция)
- •Мицеллообразование в водных и неводных средах.
- •Изоэлектрическая точка и точка нулевого заряда
- •Билет № 16
- •Адсорбция электролитов на границе раздела твердое тело – жидкость и возникновение двойного электрического слоя
- •Структурно-механические свойства дисперсных систем
- •Защитное действие растворов высокомолекулярных соединений
- •Билет № 17
- •Электрокапиллярные явления
- •Влияние электролитов на устойчивость гидрофобных коллоидов. Роль -потенциала
- •Поверхностная активность
- •Билет № 18
- •Теория двойного электрического слоя Гуи – Чепмена
- •Электродиализ
- •Флотация
- •Билет № 19
- •Теория двойного электрического слоя Штерна
- •Работа адсорбции. Правило Траубе
- •Основные факторы устойчивости гидрофобных коллоидов
- •Билет № 20
- •Параметры дэс и их зависимость от концентрации электролита
- •Электроосмос
- •Устойчивость лиофильных и лиофобных коллоидных систем
- •Билет № 21
- •Билет 21. Электрокинетические явления
- •Капиллярная конденсация
- •Адсорбционный потенциал
- •Билет № 22
- •Потенциал и ток течения
- •Теплоты физической адсорбции и смачивания
- •Поверхностное и пограничное натяжение
- •Билет № 23
- •Электрокинетический потенциал. Влияние концентрации электролита и вида противоиона
- •Уравнение состояния поверхностного слоя разбавленных растворов
- •Критическая концентрация мицеллообразования (ккм)
- •Билет № 24
- •Потенциалы двойного электрического слоя. Зависимость от концентрации электролита
- •Работа адсорбции. Правило Траубе
- •Пептизация
- •Билет № 25
- •Электрокинетические свойства капиллярных систем
- •Поверхностно-активные и поверхностно-инактивные вещества
- •Изоэлектрическая точка и точка нулевого заряда
- •Билет № 26
- •Билет 26. Методы получение и очистки дисперсных систем
- •Изменение уровня жидкости в капиллярах
- •Правило Шульце - Гарди
- •Билет № 27
- •Теория быстрой коагуляции Смолуховского
- •Критическое сопоставление теорий адсорбции газов и паров твердыми телами
- •Числа переноса ионов в капиллярных системах
- •Билет № 28
- •Поверхностное натяжение жидкостей
- •Теория устойчивости гидрофобных коллоидов Дерягина – Ландау – Фервея – Овербека
- •3. Правило уравнивания полярностей Ребиндера
- •Билет № 29
- •Специфика коллоидного состояния вещества
- •Коагулирующее действие электролитов
- •Капиллярное давление
Изменение уровня жидкости в капиллярах
Если
две фазы разделены искривленной
поверхностью, то давление в фазах будет
различным. Эта разность давлений
называется капиллярным
давлением.
Выражение для капиллярного давления
можно получить, рассматривая процесс
выдувания пузырька, например, в жидкость.
Если под действием избыточного
давления Р происходит
увеличение радиуса Rпузырька
на dR,
то совершается работа dW=PdV (dV=4π R2dR –
увеличение объема пузырька). Затраченная
работа расходуется на увеличение
поверхностной энергии пузырька
на σdS (σ –
поверхностное натяжение, dS=8πRdR –
увеличение площади поверхности
сферического пузырька). При равновесии
работа равна увеличению поверхностной
энергии P4πR2dR =σ8πRdR и
получаем закон
Лапласа для сферических поверхностей:
![]() (1)
(1)
Поверхности
произвольной кривизны, которые можно
охарактеризовать двумя главными
радиусами кривизны R1 и R2 ,
закон Лапласа имеет вид:
![]() (2)
(2)
Следует отметить, что капиллярное давление для выпуклой поверхности, радиус кривизны которой больше нуля, положительно, а для вогнутой поверхности (с отрицательным радиусом кривизны) отрицательно. На законе Лапласа основано несколько методов измерения поверхностного натяжения (метод максимального давления в пузырьке воздуха, капиллярного поднятия, методы сидящей, висящей и вращающейся капли), а также капиллярные явления (капиллярного поднятия, пропитки пористых тел, стягивания частиц менисками).
Рассмотрим процесс капиллярного поднятия. Если в жидкость поместить узкую трубку – капилляр, то в результате смачивания стенок капилляра, поверхность жидкости внутри трубки становится искривленной. Если жидкость смачивает стенки капилляра, то возникает вогнутая поверхность с радиусом кривизны R=r/cosθ (r - радиус капилляра, θ – уголсмачивания, рис.1).
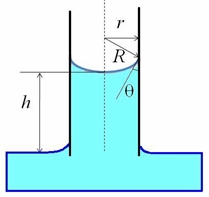
Рис.1. (капиллярное поднятие)
Давление под поверхностью мениска будет меньше, чем давление под плоской границей жидкости в сосуде на величину капиллярного давления Р=2σ/R=2σcosθ/r, поэтому жидкость в капилляре будет подниматься до тех пор, пока гидростатический вес столбика жидкости (ρgh )не уравновесит капиллярное давление:
ρgh=(2σcosθ)r
где ρ – плотность жидкости. Отсюда высота капиллярного поднятия
![]() (3)
Выражение (3) называют законом
Жюрена который
показывает, что жидкость тем выше
поднимается по капилляру, чем у нее
больше ее поверхностное натяжение,
меньше плотность, чем уже капилляр и
чем лучше данная жидкость смачивает
стенки капилляра. При несмачивании
наблюдается капиллярная депрессия –
уровень жидкости в капилляре будет ниже
уровня жидкости в широком сосуде.
(3)
Выражение (3) называют законом
Жюрена который
показывает, что жидкость тем выше
поднимается по капилляру, чем у нее
больше ее поверхностное натяжение,
меньше плотность, чем уже капилляр и
чем лучше данная жидкость смачивает
стенки капилляра. При несмачивании
наблюдается капиллярная депрессия –
уровень жидкости в капилляре будет ниже
уровня жидкости в широком сосуде.
Из формулы (3) очевидно, что произведение, (hr)= a2 = (2σ/ρg) является постоянной для данной жидкости величиной - капиллярной постоянной. Величину а называют капиллярной длиной и все капиллярные эффекты будут наблюдаться, если характерный размер (например, радиус капилляра) будет меньше капиллярной длины. Для обычных жидкостей капиллярная длина имеет порядок миллиметра.
Поскольку
давление жидкости в капле повышено на
величину капиллярного давления, давление
насыщенных паров будет также увеличено
по сравнению с давлением над плоской
поверхностью. Зависимость давления
насыщенных паров от радиуса кривизны
поверхности R определяется законом
Томсона (Кельвина):
![]()
где Vm – молярный объем жидкости, R – универсальная газовая постоянная, Т – абсолютная температура. Знак ± означает, что давление паров повышено над выпуклой поверхностью и понижено над вогнутой.
Закон Томсона (Кельвина) имеет несколько важных следствий. В полидисперсной системе давление над мелкими каплями выше, чем над крупными, и в дисперсионной среде возникает диффузионный поток вещества от мелких капель к крупным. В результате происходит испарение малых и увеличение размера более крупных капель. Это явление называютизотермической перегонкой. Другое следствие закона – капиллярная конденсация – конденсация жидкости из пара над вогнутым (смачивающим) мениском в капиллярах при давлениях, более низких, чем давление насыщенных паров над плоской поверхностью.
