
- •Билет № 1
- •Принципы классификации дисперсных систем
- •Потенциал и ток течения
- •Поверхностно-активные вещества и их классификация
- •Билет № 2
- •Молекулярно-кинетические свойства дисперсных систем
- •Электрофорез
- •Адсорбционный потенциал
- •Билет № 3
- •Билет 3. Седиментация суспензий и седиментационно-диффузионное равновесие
- •Электроосмос
- •Теория быстрой коагуляции Смолуховского
- •1. Оптические свойства дисперсных систем
- •2. Зависимость ψ1-потенциала от концентрации электролита
- •3. Правило уравнивания полярностей Ребиндера
- •Билет № 5
- •Билет № 6
- •Строение двойного электрического слоя (дэс) на границе раздела твердое тело – жидкость. Потенциалы дэс.
- •Защитное действие растворов высокомолекулярных соединений
- •Билет № 7
- •Билет 7. Химический потенциал и давление пара у искривленных поверхностей
- •Механизмы образования двойного электрического слоя на поверхности твердых тел
- •Влияние многозарядных ионов на устойчивость гидрофобных коллоидов
- •Билет № 8
- •Уравнение адсорбции Гиббса
- •Числа переноса ионов в капиллярных системах
- •Электрокинетический потенциал и его роль в устойчивости гидрофобных коллоидов
- •Билет 9. Изотерма адсорбции Ленгмюра (адсорбция на границе раздела раствор - газ)
- •Основные положения теории двойного электрического слоя Гуи-Чепмена, модифицированной теории Гуи, теории Штерна.
- •Лиофильные коллоидные системы
- •Билет № 10
- •Поверхностные пленки нерастворимых веществ
- •Индифферентные и специфически сорбирующиеся электролиты. Влияние на устойчивость гидрофобных коллоидов
- •3. Поверхностная проводимость
- •Билет № 11
- •Адсорбция на поверхности твердых тел. Теплоты адсорбции и смачивания
- •Методы определения размеров частиц
- •Приведенная толщина диффузного слоя; зависимость от вида электролита
- •Билет № 12
- •Теория адсорбции Ленгмюра (граница раздела твердое тело – газ или пар)
- •Электрокинетический потенциал; влияние концентрации электролита и заряда противоиона
- •Поверхностное натяжение и способы его определения
- •Билет № 13
- •Теория адсорбции Поляни
- •Коллоидно-химические основы охраны окружающей среды
- •Электрокинетический потенциал
- •Билет № 14
- •Теория адсорбции Брунауэра – Эммета – Теллера
- •Высокомолекулярные электролиты
- •Правило уравнивания полярностей Ребиндера
- •Билет № 15
- •Адсорбция неэлектролитов на границе раздела твердое тело – жидкость (молекулярная адсорбция)
- •Мицеллообразование в водных и неводных средах.
- •Изоэлектрическая точка и точка нулевого заряда
- •Билет № 16
- •Адсорбция электролитов на границе раздела твердое тело – жидкость и возникновение двойного электрического слоя
- •Структурно-механические свойства дисперсных систем
- •Защитное действие растворов высокомолекулярных соединений
- •Билет № 17
- •Электрокапиллярные явления
- •Влияние электролитов на устойчивость гидрофобных коллоидов. Роль -потенциала
- •Поверхностная активность
- •Билет № 18
- •Теория двойного электрического слоя Гуи – Чепмена
- •Электродиализ
- •Флотация
- •Билет № 19
- •Теория двойного электрического слоя Штерна
- •Работа адсорбции. Правило Траубе
- •Основные факторы устойчивости гидрофобных коллоидов
- •Билет № 20
- •Параметры дэс и их зависимость от концентрации электролита
- •Электроосмос
- •Устойчивость лиофильных и лиофобных коллоидных систем
- •Билет № 21
- •Билет 21. Электрокинетические явления
- •Капиллярная конденсация
- •Адсорбционный потенциал
- •Билет № 22
- •Потенциал и ток течения
- •Теплоты физической адсорбции и смачивания
- •Поверхностное и пограничное натяжение
- •Билет № 23
- •Электрокинетический потенциал. Влияние концентрации электролита и вида противоиона
- •Уравнение состояния поверхностного слоя разбавленных растворов
- •Критическая концентрация мицеллообразования (ккм)
- •Билет № 24
- •Потенциалы двойного электрического слоя. Зависимость от концентрации электролита
- •Работа адсорбции. Правило Траубе
- •Пептизация
- •Билет № 25
- •Электрокинетические свойства капиллярных систем
- •Поверхностно-активные и поверхностно-инактивные вещества
- •Изоэлектрическая точка и точка нулевого заряда
- •Билет № 26
- •Билет 26. Методы получение и очистки дисперсных систем
- •Изменение уровня жидкости в капиллярах
- •Правило Шульце - Гарди
- •Билет № 27
- •Теория быстрой коагуляции Смолуховского
- •Критическое сопоставление теорий адсорбции газов и паров твердыми телами
- •Числа переноса ионов в капиллярных системах
- •Билет № 28
- •Поверхностное натяжение жидкостей
- •Теория устойчивости гидрофобных коллоидов Дерягина – Ландау – Фервея – Овербека
- •3. Правило уравнивания полярностей Ребиндера
- •Билет № 29
- •Специфика коллоидного состояния вещества
- •Коагулирующее действие электролитов
- •Капиллярное давление
Билет № 2
Молекулярно-кинетические свойства дисперсных систем

![]()






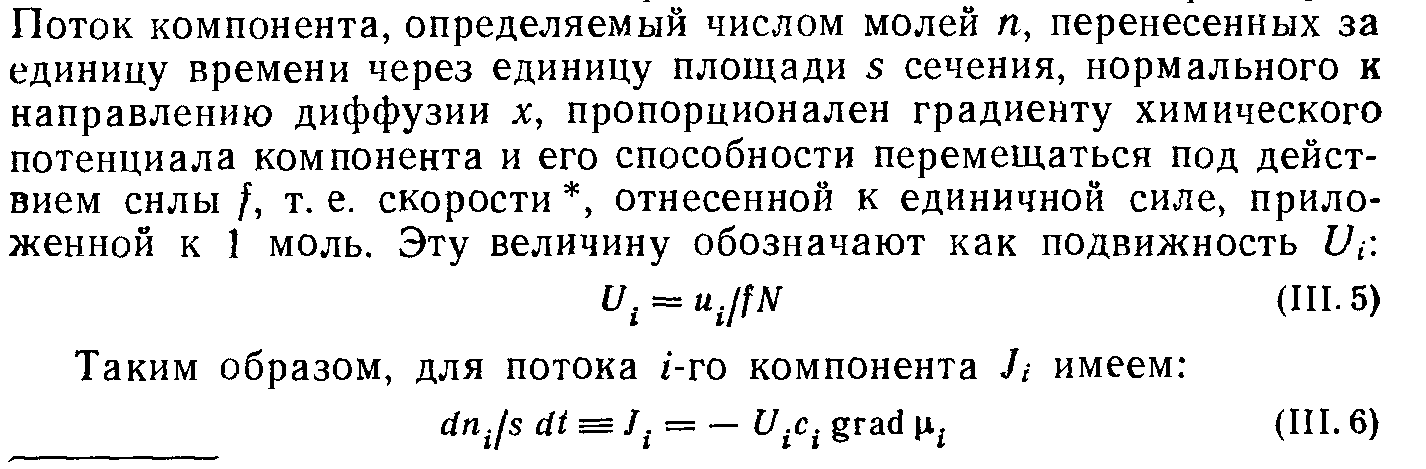






Электрофорез
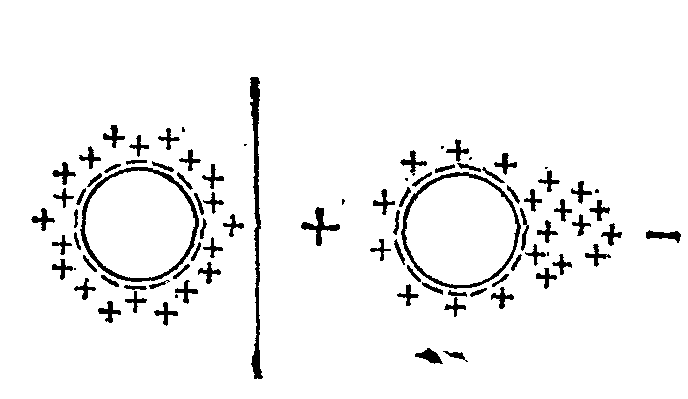




Адсорбционный потенциал
Поляни
предложил рассматривать
процесс адсорбции аналогично
сжатию молекул адсорбтива
в некотором поле адсорбционных сил
вблизи поверхности адсорбента.
Этот процесс протекает таким образом,
что на поверхности адсорбента в
результате сжатия адсорбтива в поле
адсорбционных сил формируется жидкая
пленка, т.е. происходит конденсация адсорбтива.
Для упрощения Поляни допускал, что в
поле адсорбционных сил газ подчиняется
закону Менделеева-Клапейрона. Это
означает, что адсорбент химически
инертный и адсорбция протекает
только в результате физического
взаимодействия между молекулами адсорбента и
адсорбтива. В этом случае можно было
ввести количественную характеристику
поля адсорбционных сил, а именно,
адсорбционный потенциал e, равный работе
сжатия одного моля газа или пара от
равновесного давления Р
в объеме до давления насыщения
Ps. Этот потенциал можно также рассматривать
как работу перемещения одного моля газа с
бесконечно большого расстояния на
поверхность адсорбента.
Из химической
термодинамики известно,
что работа сжатия идеального
газа вплоть
до его конденсации может
быть описана уравнением
![]() .
Потенциал адсорбционных сил в трактовке
Поляни является не чем иным, как
дифференциальной свободной
энергией адсорбции,
т.е. e = - DGа.
.
Потенциал адсорбционных сил в трактовке
Поляни является не чем иным, как
дифференциальной свободной
энергией адсорбции,
т.е. e = - DGа.
Адсорбционный потенциал имеет постоянное значение вдоль сечения очень узких микропор, но в более широких микропорах его значение проходит через минимум; минимальное значение потенциала наблюдается вблизи центра поры. В случае малых пор минимальное значение потенциала соответствует точке кривой, удаленной от центра поры на расстояние, меньшее радиуса поры. В случае больших пор результирующая кривая не достигает минимума, прежде чем адсорбция не вступит в стадию, в которой относительное давление приближается к единице. Следовательно, будет или не будет в поре данного диаметра происходить капиллярная конденсация, зависит от профиля кривой потенциальной энергии. Самопроизвольное заполнение поры большого диаметра, приводящее к капиллярной конденсации, происходило бы в том случае, если адсорбционный потенциал был бы высок, а силы отталкивания - слабы. Такое положение соответствует сильному сродству адсорбент - адсорбат и слабому взаимодействию между слоями адсорбата. Адсорбционный потенциал отличается от теплоты адсорбции теплотой сжатия, которой часто можно пренебречь.
Билет № 3
Билет 3. Седиментация суспензий и седиментационно-диффузионное равновесие
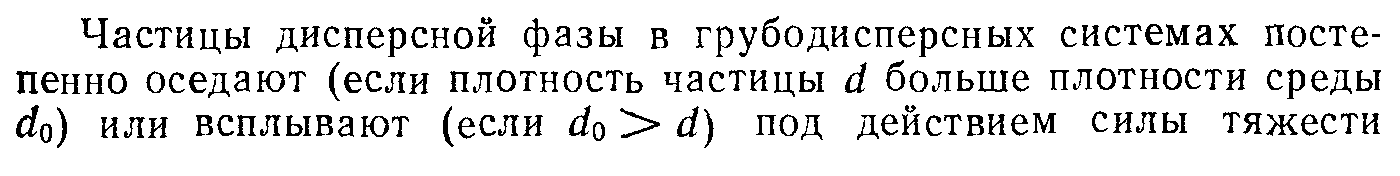


Электроосмос


Теория быстрой коагуляции Смолуховского


1) частицы дисперсной фазы сферические, а сами дисперсные системы являются монодисперсными, т.е. содержат частички одного размера; 2) скорость коагуляции определяется тремя факторами:
– радиусом сферы сил притяжения частиц;
– интенсивностью броуновского движения, которая определяет число столкновений в единицу времени и характеризуется коэффициентомдиффузии D;
– начальной концентрацией частиц n0; 3) между частицами существуют только силы притяжения.
Последняя предпосылка означает, что в какой-то момент времени, который можно обозначить как t0, внезапно и полностью исчезают силы, приводившие к отталкиванию частиц при их сближении. После этого времени любое столкновение частиц обязательно приведет к их агрегированию.
Смолуховский предложил рассматривать процесс коагуляции как попарное слипание частиц, чем формально уподобил процесс коагуляциихимической реакции второго порядка. Считается, что вероятность одновременного столкновения трех частиц столь мала, что такие столкновения можно не учитывать.
Очевидно,
что вначале будут образовываться
агрегаты частиц, состоящие из двух
первичных, затем первичная частица
может объединяться с агрегатом из двух
первичных частиц и образуется новый
агрегат, состоящий из трех первичных
частиц. Затем к нему присоединится еще
одна частица и будет сформирован агрегат
из четырех частиц и т.д. Назовем число
частиц в агрегате порядком агрегата и
будем считать, что прикоагуляции последовательно
будут сформированы агрегаты второго
n2,
третьего n3,
четвертого n4,
пятого n5 и
т.д. порядков. В любой момент времени
после начала коагуляции в дисперсной
системе будет
присутствовать набор агрегатов частиц,
так что частичная концентрация будет
определяться суммой всех агрегатов:
![]() .
(2.3.137)
.
(2.3.137)
Выражая
скорость коагуляции через
уменьшение числа частиц в единице объема
за единицу времени и учитывая, что общее
число частиц может только уменьшаться,
записываем v = – dn/dt = kn2,
(2.3.138) где v – скорость коагуляции,
k – постоянная скорости коагуляции,
n – частичная концентрация (частиц/м3).
Выяснение физического смысла постоянной
скорости коагуляции проводится
при рассмотрении диффузионного механизма
сближения частиц. Вначале решают задачу
диффузионного сближения произвольной
частицы с некоторой закрепленной в
пространстве центральной частицей.
Столкновение этой неподвижной частицы
с другой происходит каждый раз, когда
частицы сближаются на расстояние, равное
их двойному радиусу(R = 2r). Таким образом,
рассматривается диффузия точечных
частиц к сфере радиуса R. При
этом концентрация единичных
(первичных) частиц на поверхности такой
сферы равна нулю, поскольку на этой
поверхности частицы образуют агрегаты.
Распределение частичной концентрации в дисперсной
системе находят
решением дифференциального
уравнения диффузии (второго
закона Фика)
![]() ,
(2.3.139) где
,
(2.3.139) где ![]() – оператор Лапласа,
– оператор Лапласа,
![]() .
(2.3.140)
.
(2.3.140)
Поскольку частицы перемещаются независимо друг от друга, то постоянная диффузии будет складываться из постоянных диффузии различных частиц, т.е. D12 = D1 + D2. (2.3.148) Если частицы имеют одинаковый размер, то
D12 =2
D1 .
(2.3.149) Доказательство справедливости
уравнений (2.3.148) и (2.3.149) проводят при
рассмотрении относительного среднего
сдвига частиц. Из теорииброуновского
движения известно,
что
![]() ,
(2.3.150) где
,
(2.3.150) где ![]() -
средний квадратичный сдвиг частицы.
Относительное смещение частиц будет
-
средний квадратичный сдвиг частицы.
Относительное смещение частиц будет
![]() .
(2.3.151) Поэтому
.
(2.3.151) Поэтому
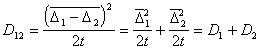 .
(2.3.152) Для одинаковых частиц
.
(2.3.152) Для одинаковых частиц
![]() .
(2.3.153) Для потока j частиц через сферу
радиуса R, движущуюся вместе с одной из
них, подставляя вместо D12 =2
D, получаем j = 8πRDn0.
(10.154) Поток j выражает скорость агрегирования
по отношению к одной частице, для всех
n0 частиц
в 1 м3 она
будет в n0 раз
больше, следовательно,
.
(2.3.153) Для потока j частиц через сферу
радиуса R, движущуюся вместе с одной из
них, подставляя вместо D12 =2
D, получаем j = 8πRDn0.
(10.154) Поток j выражает скорость агрегирования
по отношению к одной частице, для всех
n0 частиц
в 1 м3 она
будет в n0 раз
больше, следовательно,
![]() (2.3.155)
или
(2.3.155)
или
![]() ,
(2.3.156) так как уравнение (2.3.155) справедливо
для любой концентрации частиц
в любой момент времени от начала коагуляции.
Таким образом, постоянная
скорости коагуляции имеет
физический смысл к = 8πRD . (2.3.157) Интегрирование
уравнения (2.3.156) проводим в пределах от
0 до t и, соответственно, от n0 до
n. В результате интегрирования получаем
,
(2.3.156) так как уравнение (2.3.155) справедливо
для любой концентрации частиц
в любой момент времени от начала коагуляции.
Таким образом, постоянная
скорости коагуляции имеет
физический смысл к = 8πRD . (2.3.157) Интегрирование
уравнения (2.3.156) проводим в пределах от
0 до t и, соответственно, от n0 до
n. В результате интегрирования получаем
![]() .
(2.3.158) Это уравнение может быть использовано
для расчета кинетической
кривой коагуляции,
однако экспериментальное определение
постоянной скорости коагуляции встречает
определенные трудности. В процессе коагуляции в
результате слипания частиц происходит
изменение их размера и, следовательно,
коэффициента диффузии и
радиуса сферы сил притяжения. При этом
постоянная скорости коагуляции оказывается
связанной с двумя неопределенными
величинами. Поэтому кинетическое
уравнение приводят
к виду, не содержащему постоянной
скорости коагуляции.
Прием, который применил Смолуховский,
заключается в определении времени
половинной коагуляции,
когда nt =n0/2.
(2.3.159) Поэтому
.
(2.3.158) Это уравнение может быть использовано
для расчета кинетической
кривой коагуляции,
однако экспериментальное определение
постоянной скорости коагуляции встречает
определенные трудности. В процессе коагуляции в
результате слипания частиц происходит
изменение их размера и, следовательно,
коэффициента диффузии и
радиуса сферы сил притяжения. При этом
постоянная скорости коагуляции оказывается
связанной с двумя неопределенными
величинами. Поэтому кинетическое
уравнение приводят
к виду, не содержащему постоянной
скорости коагуляции.
Прием, который применил Смолуховский,
заключается в определении времени
половинной коагуляции,
когда nt =n0/2.
(2.3.159) Поэтому
![]() ,
(2.3.160) где Q – время половинной коагуляции,
определяемое по времени, в течение
которого начальная частичная концентрация изменится
в два раза. Следовательно
,
(2.3.160) где Q – время половинной коагуляции,
определяемое по времени, в течение
которого начальная частичная концентрация изменится
в два раза. Следовательно
![]() (2.3.161)
Подставляя значение постоянной
скорости коагуляции из
уравнения (2.3.161) в уравнение (2.3.158),
получаем
(2.3.161)
Подставляя значение постоянной
скорости коагуляции из
уравнения (2.3.161) в уравнение (2.3.158),
получаем
![]() .
(2.3.162) Определение постоянной
скорости коагуляции можно
проводить графическим методом после
построения графика в координатах
линейной формы уравнения Смолуховского
.
(2.3.162) Определение постоянной
скорости коагуляции можно
проводить графическим методом после
построения графика в координатах
линейной формы уравнения Смолуховского
![]() .
(2.3.163) В соответствии с этим уравнением
постоянную скорости коагуляции можно
определить по тангенсу угла наклона,
если известна величина начальной
частичной концентрации n0.
В процессе коагуляции в
результате слипания частиц происходит
изменение их размера и, следовательно,
коэффициент диффузии и
радиуса сферы сил притяжения. При этом
постоянная скорости коагуляции оказывается
связанной с двумя неопределенными
величинами. Поэтому кинетическое
уравнение приводят
к виду, не содержащему постоянной
скорости коагуляции.
Для расчета концентрации агрегатов
частиц любого порядка была получена
формула
.
(2.3.163) В соответствии с этим уравнением
постоянную скорости коагуляции можно
определить по тангенсу угла наклона,
если известна величина начальной
частичной концентрации n0.
В процессе коагуляции в
результате слипания частиц происходит
изменение их размера и, следовательно,
коэффициент диффузии и
радиуса сферы сил притяжения. При этом
постоянная скорости коагуляции оказывается
связанной с двумя неопределенными
величинами. Поэтому кинетическое
уравнение приводят
к виду, не содержащему постоянной
скорости коагуляции.
Для расчета концентрации агрегатов
частиц любого порядка была получена
формула
![]() ,
(2.3.164) где i – порядок, т.е. число
соединившихся в агрегат частиц.
Расчет кинетических
кривых по
уравнениям (2.3.162) и (2.3.164) приводит к
зависимостям, показанным на рис.2.25, а.
Иногда расчеты постоянной скорости
проводят теоретически, для чего используют
уравнение Эйнштейна, связывающее
коэффициент диффузии и
размер частиц
,
(2.3.164) где i – порядок, т.е. число
соединившихся в агрегат частиц.
Расчет кинетических
кривых по
уравнениям (2.3.162) и (2.3.164) приводит к
зависимостям, показанным на рис.2.25, а.
Иногда расчеты постоянной скорости
проводят теоретически, для чего используют
уравнение Эйнштейна, связывающее
коэффициент диффузии и
размер частиц
![]() ,
(2.3.165) где D – коэффициент диффузии,
k- постоянная
Больцмана,
h – вязкость дисперсионной
среды,
r – радиус частиц.
,
(2.3.165) где D – коэффициент диффузии,
k- постоянная
Больцмана,
h – вязкость дисперсионной
среды,
r – радиус частиц.
Билет № 4
