
- •Билет № 1
- •Принципы классификации дисперсных систем
- •Потенциал и ток течения
- •Поверхностно-активные вещества и их классификация
- •Билет № 2
- •Молекулярно-кинетические свойства дисперсных систем
- •Электрофорез
- •Адсорбционный потенциал
- •Билет № 3
- •Билет 3. Седиментация суспензий и седиментационно-диффузионное равновесие
- •Электроосмос
- •Теория быстрой коагуляции Смолуховского
- •1. Оптические свойства дисперсных систем
- •2. Зависимость ψ1-потенциала от концентрации электролита
- •3. Правило уравнивания полярностей Ребиндера
- •Билет № 5
- •Билет № 6
- •Строение двойного электрического слоя (дэс) на границе раздела твердое тело – жидкость. Потенциалы дэс.
- •Защитное действие растворов высокомолекулярных соединений
- •Билет № 7
- •Билет 7. Химический потенциал и давление пара у искривленных поверхностей
- •Механизмы образования двойного электрического слоя на поверхности твердых тел
- •Влияние многозарядных ионов на устойчивость гидрофобных коллоидов
- •Билет № 8
- •Уравнение адсорбции Гиббса
- •Числа переноса ионов в капиллярных системах
- •Электрокинетический потенциал и его роль в устойчивости гидрофобных коллоидов
- •Билет 9. Изотерма адсорбции Ленгмюра (адсорбция на границе раздела раствор - газ)
- •Основные положения теории двойного электрического слоя Гуи-Чепмена, модифицированной теории Гуи, теории Штерна.
- •Лиофильные коллоидные системы
- •Билет № 10
- •Поверхностные пленки нерастворимых веществ
- •Индифферентные и специфически сорбирующиеся электролиты. Влияние на устойчивость гидрофобных коллоидов
- •3. Поверхностная проводимость
- •Билет № 11
- •Адсорбция на поверхности твердых тел. Теплоты адсорбции и смачивания
- •Методы определения размеров частиц
- •Приведенная толщина диффузного слоя; зависимость от вида электролита
- •Билет № 12
- •Теория адсорбции Ленгмюра (граница раздела твердое тело – газ или пар)
- •Электрокинетический потенциал; влияние концентрации электролита и заряда противоиона
- •Поверхностное натяжение и способы его определения
- •Билет № 13
- •Теория адсорбции Поляни
- •Коллоидно-химические основы охраны окружающей среды
- •Электрокинетический потенциал
- •Билет № 14
- •Теория адсорбции Брунауэра – Эммета – Теллера
- •Высокомолекулярные электролиты
- •Правило уравнивания полярностей Ребиндера
- •Билет № 15
- •Адсорбция неэлектролитов на границе раздела твердое тело – жидкость (молекулярная адсорбция)
- •Мицеллообразование в водных и неводных средах.
- •Изоэлектрическая точка и точка нулевого заряда
- •Билет № 16
- •Адсорбция электролитов на границе раздела твердое тело – жидкость и возникновение двойного электрического слоя
- •Структурно-механические свойства дисперсных систем
- •Защитное действие растворов высокомолекулярных соединений
- •Билет № 17
- •Электрокапиллярные явления
- •Влияние электролитов на устойчивость гидрофобных коллоидов. Роль -потенциала
- •Поверхностная активность
- •Билет № 18
- •Теория двойного электрического слоя Гуи – Чепмена
- •Электродиализ
- •Флотация
- •Билет № 19
- •Теория двойного электрического слоя Штерна
- •Работа адсорбции. Правило Траубе
- •Основные факторы устойчивости гидрофобных коллоидов
- •Билет № 20
- •Параметры дэс и их зависимость от концентрации электролита
- •Электроосмос
- •Устойчивость лиофильных и лиофобных коллоидных систем
- •Билет № 21
- •Билет 21. Электрокинетические явления
- •Капиллярная конденсация
- •Адсорбционный потенциал
- •Билет № 22
- •Потенциал и ток течения
- •Теплоты физической адсорбции и смачивания
- •Поверхностное и пограничное натяжение
- •Билет № 23
- •Электрокинетический потенциал. Влияние концентрации электролита и вида противоиона
- •Уравнение состояния поверхностного слоя разбавленных растворов
- •Критическая концентрация мицеллообразования (ккм)
- •Билет № 24
- •Потенциалы двойного электрического слоя. Зависимость от концентрации электролита
- •Работа адсорбции. Правило Траубе
- •Пептизация
- •Билет № 25
- •Электрокинетические свойства капиллярных систем
- •Поверхностно-активные и поверхностно-инактивные вещества
- •Изоэлектрическая точка и точка нулевого заряда
- •Билет № 26
- •Билет 26. Методы получение и очистки дисперсных систем
- •Изменение уровня жидкости в капиллярах
- •Правило Шульце - Гарди
- •Билет № 27
- •Теория быстрой коагуляции Смолуховского
- •Критическое сопоставление теорий адсорбции газов и паров твердыми телами
- •Числа переноса ионов в капиллярных системах
- •Билет № 28
- •Поверхностное натяжение жидкостей
- •Теория устойчивости гидрофобных коллоидов Дерягина – Ландау – Фервея – Овербека
- •3. Правило уравнивания полярностей Ребиндера
- •Билет № 29
- •Специфика коллоидного состояния вещества
- •Коагулирующее действие электролитов
- •Капиллярное давление
Билет № 23
Электрокинетический потенциал. Влияние концентрации электролита и вида противоиона
Величина λ определяется при математическом описании ДЭС выражением
 (1.1)
(1.1)
где λ — эффективная толщина диффузного слоя - расстояние, где потенциал на границе плотного и диффузного слоя падает в е (основание натурального логарифма) раз;
![]() — диэлектрическая
постоянная;
R — газовая
постоянная; 8,3 Дж\(моль*Кл) Т — температура;
— диэлектрическая
постоянная;
R — газовая
постоянная; 8,3 Дж\(моль*Кл) Т — температура;
Z — заряд иона; F — число Фарадея; 96400 Кл\моль С — концентрация ионов, моль-ион\литр
ε0— электрическая константа. 8,85*10-12 Ф/м
Влияние
различных факторов на ![]() -
потенциал:
-
потенциал:
Рассмотрим
свойства параметра λ. Как
следует из уравнения (1.1) он является
функцией заряда ионов,
концентрации, температуры, диэлектрической
постоянно среды. Например, с введением
в систему электролитов диффузный слой
будет сжиматься (?.
линейно уменьшается с ростом ![]() ),
распределение потенциала идет на меньшем
расстоянии, то есть более круто. Величина
потенциала при этом на границе скольжения
(
)
уменьшается
),
распределение потенциала идет на меньшем
расстоянии, то есть более круто. Величина
потенциала при этом на границе скольжения
(
)
уменьшается
Рассматривая влияние электролита на -потенциал необходимо различал природу электролита. Электролит может быть индифферентным или чужеродным, то есть не содержащим ионов, подобных ионам твердой фазы, а также неиндифферентным или родственным, способным достраивать кристаллическую решетку твердой фазы.
При введении индифферентных электролитов возможно не только сжатие диффузной части ДЭС, но и изменение знака -потенциала на противоположный. Полный потенциал при этом остается неизменным Перезарядка наблюдается при введении в систему индифферентного электролита с многовалентным ионом, способным повлияй, только на внешнюю обкладку ДЭС
Добавление неиндифферентного электролита может привести к дополнительной адсорбции ионов на поверхности (?0 при этом возрастает), либо к их полной замене другими родственными ионами. Если последние имеют противоположный знак, то возможна перезарядка поверхности, при которой изменятся как полный, так и электрокинетический потенциалы. С ростом заряда ионов также возрастает способность электролита снижать ?-потенциал Диффузный слой будет тем тоньше и тем ниже ?-потенциал, чем больше заряд ионов. Аналогично влияет на толщину диффузного слоя понижение температуры и диэлектрической постоянной среды.
С возрастанием радиусов ионов увеличивается их поляризуемость, уменьшается гидратация, а адсорбционная способность возрастает. Следовательно, соотношение между силами диффузии и электростатическими силами сдвигается в сторону электростатических. Это означает, что толщина диффузного слоя уменьшается, а ?-потенциал падает.
Радиусы анионов обычно больше радиусов катионов, следовательно они обладают большей способностью снижать ?-потенциал или положительный заряд поверхности. Катионам, в силу их меньшей адсорбционной способности, снизить отрицательный заряд поверхности труднее. Поэтому в природе чаще всего встречаются отрицательно заряженные поверхности.
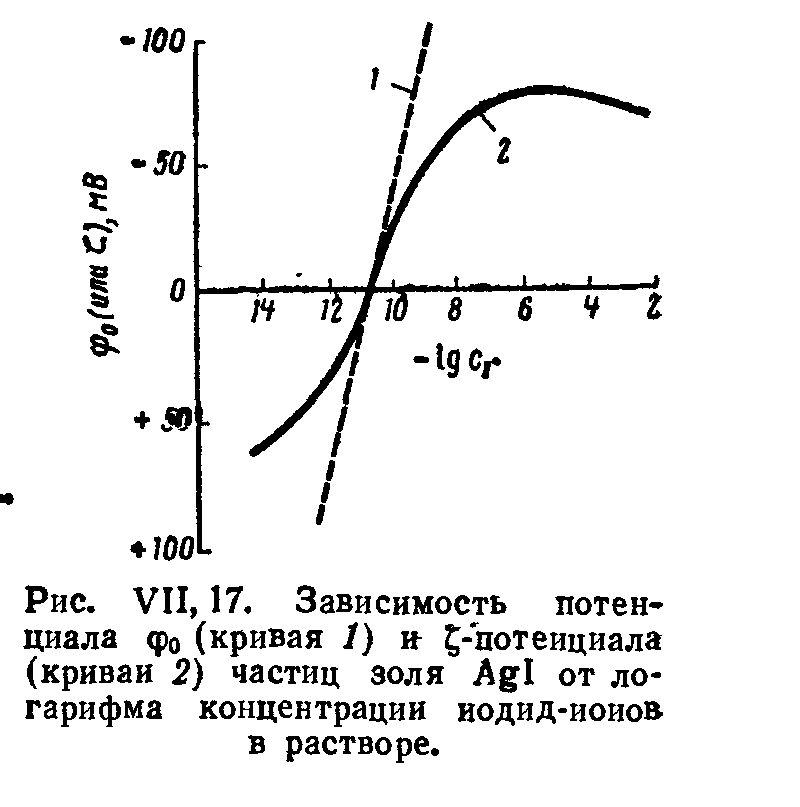



Уравнение состояния поверхностного слоя разбавленных растворов



