- •Билет № 1
- •Принципы классификации дисперсных систем
- •Потенциал и ток течения
- •Поверхностно-активные вещества и их классификация
- •Билет № 2
- •Молекулярно-кинетические свойства дисперсных систем
- •Электрофорез
- •Адсорбционный потенциал
- •Билет № 3
- •Билет 3. Седиментация суспензий и седиментационно-диффузионное равновесие
- •Электроосмос
- •Теория быстрой коагуляции Смолуховского
- •1. Оптические свойства дисперсных систем
- •2. Зависимость ψ1-потенциала от концентрации электролита
- •3. Правило уравнивания полярностей Ребиндера
- •Билет № 5
- •Билет № 6
- •Строение двойного электрического слоя (дэс) на границе раздела твердое тело – жидкость. Потенциалы дэс.
- •Защитное действие растворов высокомолекулярных соединений
- •Билет № 7
- •Билет 7. Химический потенциал и давление пара у искривленных поверхностей
- •Механизмы образования двойного электрического слоя на поверхности твердых тел
- •Влияние многозарядных ионов на устойчивость гидрофобных коллоидов
- •Билет № 8
- •Уравнение адсорбции Гиббса
- •Числа переноса ионов в капиллярных системах
- •Электрокинетический потенциал и его роль в устойчивости гидрофобных коллоидов
- •Билет 9. Изотерма адсорбции Ленгмюра (адсорбция на границе раздела раствор - газ)
- •Основные положения теории двойного электрического слоя Гуи-Чепмена, модифицированной теории Гуи, теории Штерна.
- •Лиофильные коллоидные системы
- •Билет № 10
- •Поверхностные пленки нерастворимых веществ
- •Индифферентные и специфически сорбирующиеся электролиты. Влияние на устойчивость гидрофобных коллоидов
- •3. Поверхностная проводимость
- •Билет № 11
- •Адсорбция на поверхности твердых тел. Теплоты адсорбции и смачивания
- •Методы определения размеров частиц
- •Приведенная толщина диффузного слоя; зависимость от вида электролита
- •Билет № 12
- •Теория адсорбции Ленгмюра (граница раздела твердое тело – газ или пар)
- •Электрокинетический потенциал; влияние концентрации электролита и заряда противоиона
- •Поверхностное натяжение и способы его определения
- •Билет № 13
- •Теория адсорбции Поляни
- •Коллоидно-химические основы охраны окружающей среды
- •Электрокинетический потенциал
- •Билет № 14
- •Теория адсорбции Брунауэра – Эммета – Теллера
- •Высокомолекулярные электролиты
- •Правило уравнивания полярностей Ребиндера
- •Билет № 15
- •Адсорбция неэлектролитов на границе раздела твердое тело – жидкость (молекулярная адсорбция)
- •Мицеллообразование в водных и неводных средах.
- •Изоэлектрическая точка и точка нулевого заряда
- •Билет № 16
- •Адсорбция электролитов на границе раздела твердое тело – жидкость и возникновение двойного электрического слоя
- •Структурно-механические свойства дисперсных систем
- •Защитное действие растворов высокомолекулярных соединений
- •Билет № 17
- •Электрокапиллярные явления
- •Влияние электролитов на устойчивость гидрофобных коллоидов. Роль -потенциала
- •Поверхностная активность
- •Билет № 18
- •Теория двойного электрического слоя Гуи – Чепмена
- •Электродиализ
- •Флотация
- •Билет № 19
- •Теория двойного электрического слоя Штерна
- •Работа адсорбции. Правило Траубе
- •Основные факторы устойчивости гидрофобных коллоидов
- •Билет № 20
- •Параметры дэс и их зависимость от концентрации электролита
- •Электроосмос
- •Устойчивость лиофильных и лиофобных коллоидных систем
- •Билет № 21
- •Билет 21. Электрокинетические явления
- •Капиллярная конденсация
- •Адсорбционный потенциал
- •Билет № 22
- •Потенциал и ток течения
- •Теплоты физической адсорбции и смачивания
- •Поверхностное и пограничное натяжение
- •Билет № 23
- •Электрокинетический потенциал. Влияние концентрации электролита и вида противоиона
- •Уравнение состояния поверхностного слоя разбавленных растворов
- •Критическая концентрация мицеллообразования (ккм)
- •Билет № 24
- •Потенциалы двойного электрического слоя. Зависимость от концентрации электролита
- •Работа адсорбции. Правило Траубе
- •Пептизация
- •Билет № 25
- •Электрокинетические свойства капиллярных систем
- •Поверхностно-активные и поверхностно-инактивные вещества
- •Изоэлектрическая точка и точка нулевого заряда
- •Билет № 26
- •Билет 26. Методы получение и очистки дисперсных систем
- •Изменение уровня жидкости в капиллярах
- •Правило Шульце - Гарди
- •Билет № 27
- •Теория быстрой коагуляции Смолуховского
- •Критическое сопоставление теорий адсорбции газов и паров твердыми телами
- •Числа переноса ионов в капиллярных системах
- •Билет № 28
- •Поверхностное натяжение жидкостей
- •Теория устойчивости гидрофобных коллоидов Дерягина – Ландау – Фервея – Овербека
- •3. Правило уравнивания полярностей Ребиндера
- •Билет № 29
- •Специфика коллоидного состояния вещества
- •Коагулирующее действие электролитов
- •Капиллярное давление
Приведенная толщина диффузного слоя; зависимость от вида электролита
Диффузный слой или слой Гуи, в котором находятся противоионы. Диффузный слой имеет толщину λ, которая зависит от свойств системы и может достигать больших значений. Толщина диффузного слоя рассчитывается по формуле:
![]()



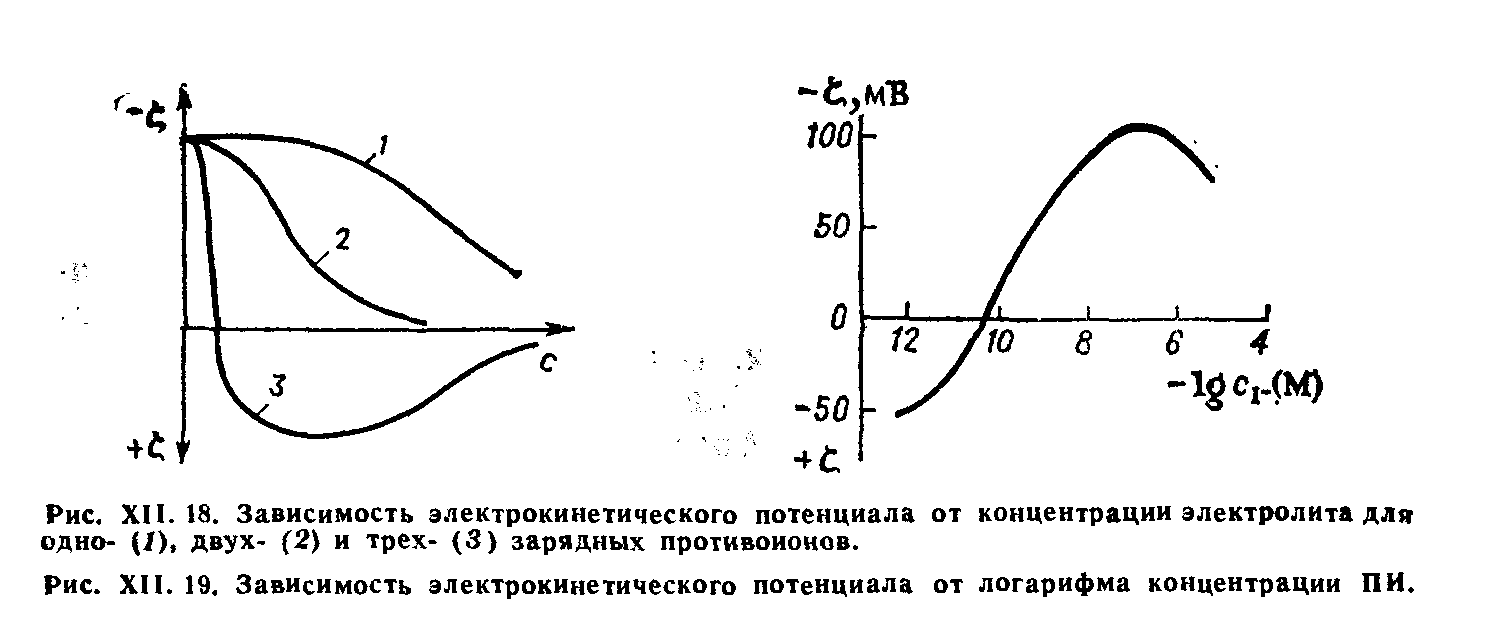
Билет № 12
Теория адсорбции Ленгмюра (граница раздела твердое тело – газ или пар)

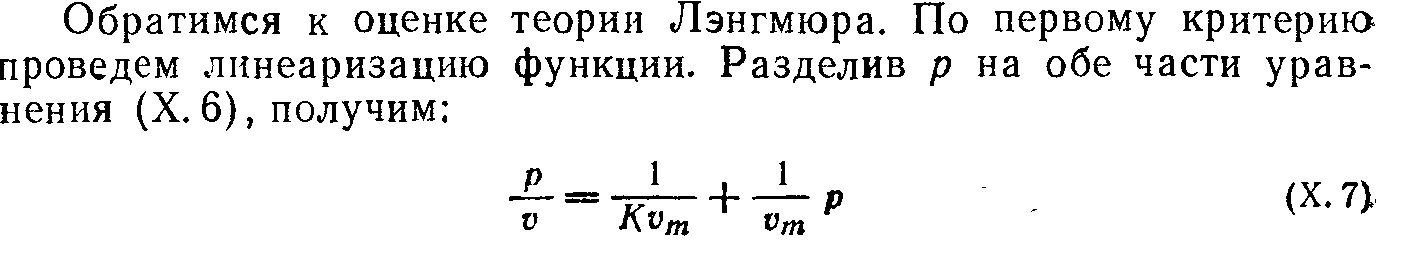

Электрокинетический потенциал; влияние концентрации электролита и заряда противоиона

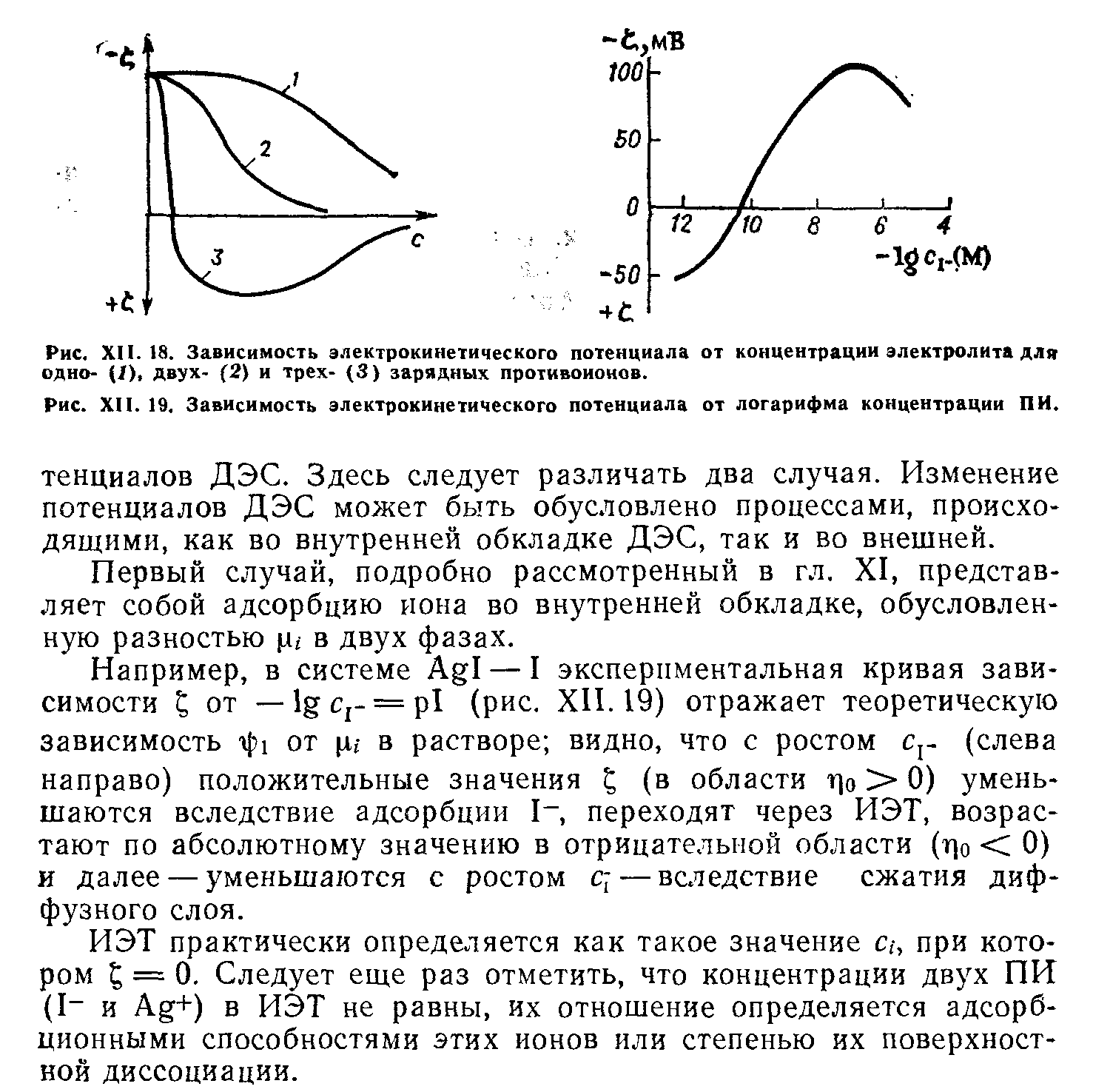
В соответствии с приведенным ранее уравнением теории строения двойного ионного слоя Гуи-Чепмена, электрокинетический потенциал должен уменьшаться линейно при повышении концентрации электролита, пропорционально C1/2. Такая зависимость может проявляться только в случае, если наблюдается лишь электростатическое взаимодействие, т.е. происходит неспецифическая адсорбция введенных в систему ионов. Поскольку именно такие представления положены в основу теории Гуи-Чепмена, хотелось бы напомнить, что неспецифическая адсорбция является лишь идеализацией, хотя в целом и полезной, реальной ситуации.
На
практике зависимость электрокинетического
потенциала от концентрации электролитов определяется
прежде всего именно специфическойадсорбцией ионов,
что приводит к тому,
что ионы одинаковой валентности будут
тем сильнее снижать электрокинетический
потенциал,
чем меньше их гидратная оболочка, что
способствует адсорбции.
Например, на одинаково заряженной
отрицательной поверхности можно
наблюдать такой ряд адсорбции: ![]() .
.
Лиотропный
ряд снижения электрокинетического
потенциала будет
противоположен ряду адсорбции (чем
выше адсорбция,
тем ниже z-потенциал). Поскольку противоионы
тем больше будут способны накапливаться
в слое Штерна и экранировать потенциал
определяющие ионы,
чем меньше их размер в гидратированном
состоянии, то именно в такой
последовательности будет уменьшаться
число ионов в
диффузионной части двойного слоя,
снижаться электрокинетический
потенциал и устойчивость
дисперсных систем.
Естественно, что двухзарядные ионы будут
более эффективны, чем однозарядные, так
как у них не только выше электростатическое
взаимодействие с
потенциалопределяющими ионами,
но и значительно сильнее проявляется
специфическая адсорбция,
приводящая к повышению степени заполнения
слоя Штерна. При низких концентрацияхэлектролитов это
способно вызывать рост поверхностной
проводимости, неучет которой приводит
к появлению кажущейся экстремальной
зависимости электрокинетического
потенциала от концентрации электролитов,
найденной из измерений электрофоретической
подвижности частиц или электроосмотической
скорости дисперсионной
среды.
Критерием, который показывает необходимость
учета поверхностной
проводимостиэлектрокинетического
потенциала по
данным электрофореза,
служит отношение поверхностной и
объемной проводимостей:
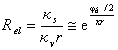 ,
(1.4.39)
,
(1.4.39)
где ks, kv – удельная поверхностная и объемная проводимость; k- параметр Дебая; r – радиус капилляра или частицы. Если Rel<<1, то электрофорез(и электроосмос) не осложнен поверхностной проводимостью и нечувствителен к форме частиц (или капилляров). Максимум на зависимостях z-потенциала от концентрации электролита свидетельствует об изменении режима электрофоретической подвижности (электроосмотической скорости) от Rel.
|
Пример зависимости электрокинетического потенциала капрона от концентрации некоторых ПАВ по данным [7] приведен на рис. 1.43. Влияние поливалентных электролитов на электрокинетический потенциал золя красителя было показано на рис. 1.37. На рис. 1.44 приведена зависимостьэлектрокинетического потенциала волокна капрон от концентрации некоторых электролитов.
Риc. 1.44. Зависимоcть z-потенциала волокна капрон от концентрацииэлектролитов. Электролиты: 1 – AlCl3; 2 –Na2SO4; 3 – NaCl |
Зависимость z-потенциала волокна от концентрации поливалентного электролита, например, от AlCl3 (см. рис. 1.44.), характеризуетсяизоэлектрической точкой и последующей перезарядкой. Это связано с тем, что ион имеет высокий специфический адсорбционный потенциал, вследствие чего способен адсорбироваться на поверхности волокна в сверхэквивалентном количестве. Катионактивные ПАВ проявляют свою адсорбционную активность в том, что изоэлектрическая точка зависит не только от величины заряда поверхности, но и от гидрофобности волокна. Чем более гидрофобно волокно, тем ниже концентрация ПАВ, при которой достигается изоэлектрическая точка, хотя z-потенциал волокна в водной среде у этих волокон выше.