- •Билет № 1
- •Принципы классификации дисперсных систем
- •Потенциал и ток течения
- •Поверхностно-активные вещества и их классификация
- •Билет № 2
- •Молекулярно-кинетические свойства дисперсных систем
- •Электрофорез
- •Адсорбционный потенциал
- •Билет № 3
- •Билет 3. Седиментация суспензий и седиментационно-диффузионное равновесие
- •Электроосмос
- •Теория быстрой коагуляции Смолуховского
- •1. Оптические свойства дисперсных систем
- •2. Зависимость ψ1-потенциала от концентрации электролита
- •3. Правило уравнивания полярностей Ребиндера
- •Билет № 5
- •Билет № 6
- •Строение двойного электрического слоя (дэс) на границе раздела твердое тело – жидкость. Потенциалы дэс.
- •Защитное действие растворов высокомолекулярных соединений
- •Билет № 7
- •Билет 7. Химический потенциал и давление пара у искривленных поверхностей
- •Механизмы образования двойного электрического слоя на поверхности твердых тел
- •Влияние многозарядных ионов на устойчивость гидрофобных коллоидов
- •Билет № 8
- •Уравнение адсорбции Гиббса
- •Числа переноса ионов в капиллярных системах
- •Электрокинетический потенциал и его роль в устойчивости гидрофобных коллоидов
- •Билет 9. Изотерма адсорбции Ленгмюра (адсорбция на границе раздела раствор - газ)
- •Основные положения теории двойного электрического слоя Гуи-Чепмена, модифицированной теории Гуи, теории Штерна.
- •Лиофильные коллоидные системы
- •Билет № 10
- •Поверхностные пленки нерастворимых веществ
- •Индифферентные и специфически сорбирующиеся электролиты. Влияние на устойчивость гидрофобных коллоидов
- •3. Поверхностная проводимость
- •Билет № 11
- •Адсорбция на поверхности твердых тел. Теплоты адсорбции и смачивания
- •Методы определения размеров частиц
- •Приведенная толщина диффузного слоя; зависимость от вида электролита
- •Билет № 12
- •Теория адсорбции Ленгмюра (граница раздела твердое тело – газ или пар)
- •Электрокинетический потенциал; влияние концентрации электролита и заряда противоиона
- •Поверхностное натяжение и способы его определения
- •Билет № 13
- •Теория адсорбции Поляни
- •Коллоидно-химические основы охраны окружающей среды
- •Электрокинетический потенциал
- •Билет № 14
- •Теория адсорбции Брунауэра – Эммета – Теллера
- •Высокомолекулярные электролиты
- •Правило уравнивания полярностей Ребиндера
- •Билет № 15
- •Адсорбция неэлектролитов на границе раздела твердое тело – жидкость (молекулярная адсорбция)
- •Мицеллообразование в водных и неводных средах.
- •Изоэлектрическая точка и точка нулевого заряда
- •Билет № 16
- •Адсорбция электролитов на границе раздела твердое тело – жидкость и возникновение двойного электрического слоя
- •Структурно-механические свойства дисперсных систем
- •Защитное действие растворов высокомолекулярных соединений
- •Билет № 17
- •Электрокапиллярные явления
- •Влияние электролитов на устойчивость гидрофобных коллоидов. Роль -потенциала
- •Поверхностная активность
- •Билет № 18
- •Теория двойного электрического слоя Гуи – Чепмена
- •Электродиализ
- •Флотация
- •Билет № 19
- •Теория двойного электрического слоя Штерна
- •Работа адсорбции. Правило Траубе
- •Основные факторы устойчивости гидрофобных коллоидов
- •Билет № 20
- •Параметры дэс и их зависимость от концентрации электролита
- •Электроосмос
- •Устойчивость лиофильных и лиофобных коллоидных систем
- •Билет № 21
- •Билет 21. Электрокинетические явления
- •Капиллярная конденсация
- •Адсорбционный потенциал
- •Билет № 22
- •Потенциал и ток течения
- •Теплоты физической адсорбции и смачивания
- •Поверхностное и пограничное натяжение
- •Билет № 23
- •Электрокинетический потенциал. Влияние концентрации электролита и вида противоиона
- •Уравнение состояния поверхностного слоя разбавленных растворов
- •Критическая концентрация мицеллообразования (ккм)
- •Билет № 24
- •Потенциалы двойного электрического слоя. Зависимость от концентрации электролита
- •Работа адсорбции. Правило Траубе
- •Пептизация
- •Билет № 25
- •Электрокинетические свойства капиллярных систем
- •Поверхностно-активные и поверхностно-инактивные вещества
- •Изоэлектрическая точка и точка нулевого заряда
- •Билет № 26
- •Билет 26. Методы получение и очистки дисперсных систем
- •Изменение уровня жидкости в капиллярах
- •Правило Шульце - Гарди
- •Билет № 27
- •Теория быстрой коагуляции Смолуховского
- •Критическое сопоставление теорий адсорбции газов и паров твердыми телами
- •Числа переноса ионов в капиллярных системах
- •Билет № 28
- •Поверхностное натяжение жидкостей
- •Теория устойчивости гидрофобных коллоидов Дерягина – Ландау – Фервея – Овербека
- •3. Правило уравнивания полярностей Ребиндера
- •Билет № 29
- •Специфика коллоидного состояния вещества
- •Коагулирующее действие электролитов
- •Капиллярное давление
Электрокинетический потенциал
Электрокинетический потенциал, -потенциал, дзета-потенциал, часть общего скачка потенциала на границе двух фаз, определяющая относительное перемещение этих фаз при электрокинетических явлениях. Общий скачок потенциала при пересечении межфазной границы вдисперсных системах обусловлен существованием двойного электрического слоя. Электрокинетический потенциал — перепад потенциала по той части диффузного слоя, в пределах которой жидкость может быть вовлечена в тангенциальное движение относительно межфазной поверхности при внешнем воздействии на систему. Под влиянием сильно адсорбирующихся на поверхности ионов или изменения pH жидкости может произойти перемена знака на противоположный («перезарядка» поверхности). Электрокинетический потенциал в изоэлектрической точке равен нулю.
ζ-потенциал есть мера интенсивности элетрокинетических явлений.
Измеряя параметры таких электрокинетических явлений, как электроосмос
 где
uэо
– электроосмотическая скорость; знак
минус означает, что жидкость движется
против поля, если ζ > 0.
где
uэо
– электроосмотическая скорость; знак
минус означает, что жидкость движется
против поля, если ζ > 0.
![]()
и электрофорез, можно вычислить ζ-потенциал на основе теории, связывающей его с этими параметрами.
Экспериментальное определение Q и I позволяет вычислить ζ-потенциал.
Билет № 14
Теория адсорбции Брунауэра – Эммета – Теллера
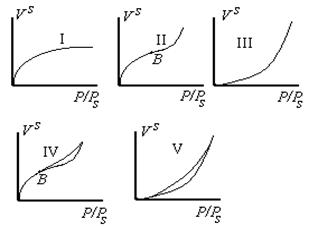
Анализ изотерм адсорбции указывает, что процесс адсорбции во многих случаях не ограничивается образованием монослоя и уже при сравнительно низких значениях относительного давления Р/Рs > 0,1 образуются, как правило, полимолекулярные слои. Брунауэр, Демминг, Демминг и Теллер выделили пять основных типов изотерм адсорбции газов на твердых адсорбентах, приведенных на рис. 1.28.
Тип I. Изотерма описывается теорией монослоя и уравнением Ленгмюра при асимптотическом приближении количества адсорбированного газа к емкости монослоя.
Тип II. Наиболее общий тип изотермы, соответствующий формированию полислоя на поверхности с высоким адсорбционным потенциалом.
Тип III. Сравнительно редко встречающийся тип изотерм образования полислоя из газовой среды на твердом адсорбенте, для тел, потенциалмонослоя которых мал и имеет тот же порядок, что и теплота конденсации адсорбтива.
Типы IV и V аналогичны типам II и III и характерны для пористых сорбентов, где адсорбция ограничивается объемом мезопор (2-50 нм), а предельнаяадсорбция достигается при давлениях Р/Рs<< 1. Часто такие изотермы имеют петлю гистерезиса, что указывает на дополнительное поглощениепара в результате капиллярной конденсации.
|
Следует отметить, что существует ряд изотерм адсорбции, которые трудно отнести к какому-либо из типов выделенных в классификации БДДТ.
Теория полимолекулярной адсорбции была развита в работах Брунауэра, Эммета и Теллера (БЭТ). В основе этой теории лежит распространение обобщенных представлений локализованного монослоя на полислойную адсорбцию. В теории БЭТ используется предпосылка, что молекулыкаждого предыдущего адсорбционного слоя служат активными центрами при образовании последующих слоев. Это предполагает, что емкость каждого слоя одинакова. Считается, что силами взаимодействия между молекулами в каждом адсорбционном слое можно пренебречь (отсутствие латеральных взаимодействий), а молекулы каждого адсорбционного слоя локализованы. Полагается, что адсорбционный потенциал в первом адсорбционном слое значительно выше, чем в других слоях, а начиная со второго адсорбционного слоя он сопоставим с энергией конденсации(изотермы типа II, IV) или для всех слоев одинаков (изотермы III, IV).