
- •Г. И. Сидоренко
- •5Уботехническое материаловедение
- •Предисловие
- •Введение
- •Свойства материалов
- •Технологические Свойства
- •Биологические свойства
- •Основные материалы металлы, применяемые в ортопедической стоматологии
- •Благородные металлы Золото
- •Металлы платиновой группы
- •Серебро
- •Неблагородные металлы—cм, с. 144.
- •Изменение структуры и свойств стали в зависимости от способа ее плавления
- •Хромоникелевая нержавеющая сталь
- •Характеристика элементов сплава
- •Хромокобальтовая сталь
- •Паяльные материалы
- •Изготовление мостовидных протезов, не содержащих припоя
- •Материалы, применяемые для изготовления базисов протезов
- •Целлулоид
- •Пластмассы
- •Акриловые пластмассы
- •Эластичные пластмассы
- •Материалы, применяемые для изготовления искусственных зубов
- •Фарфоровые стоматологические массы
- •Ситаллы
- •Искусственные зубы
- •Фарфоровые зубы
- •Пластмассовые зубы
- •Металлические зубы
- •Вспомогательные материалы
- •Слепочные материалы
- •Твердые слепочн.Ые материалы
- •Кристаллизующиеся слепочные материалы
- •Цинкоксидэвгенольные слепочные материалы
- •Термопластические слепочные массы
- •Эластичные слепочные материалы
- •Альгинатные слепочные массы
- •Тиоколовые слепочные массы
- •Силиконовые слепочные массы
- •Моделировочные материалы
- •Синтетические воски
- •Вспомогательные металлы и их сплавы
- •V легкоплавкие сплавы
- •Формовочные материалы
- •Материалы, применяемые для изготовления огнеупорных моделей
- •Разделительные и покровные материалы
- •Абразивные материалы и инструменты материалы
- •Естественные абразивные материалы
- •Фиксирующие материалы
- •Оглавление
Биологические свойства
Под биологическими свойствами
материалов понимают их влияние на
окружающие живые ткани и организм в
целом.
Все материалы основной (конструкционной) группы не должны оказывать вредного воздействия на ткани и среды, с которыми они соприкасаются, изменять состав слюны и микрофлору полости рта, вызывать воспалительные явления на слизистой оболочке и др.
Поэтому все материалы перед внедрением их в практику проходят тщательное исследование на стойкость и биологическую индифферентность, определяют как местнораздражающее, так и общетоксическое воздействие на организм. Изучают также реакцию тканей на материал методом имплантации, определяют сенсибилизирующее действие материала.
После тщательных исследований специалисты дают заключение о возможности применения материалов в качестве конструкционных для стоматологических и других целей.
Основные материалы металлы, применяемые в ортопедической стоматологии
Общие сведения Металлами называются простые вещества, обладающие характерными для них
физико-химическими свойствами (электро- и теплопроводностью, пластичностью) и имеющие в твердом состоянии кристаллическое строение.
В технике под металлами понимают вещества, обладающие металлическим блеском, пластичностью, тепло- и электропроводностью. По определению М. В. Ломоносова, «металлы суть светлые тела, которые ковать можно».
Основными химическими свойствами металлов являются способность их атомов легко отдавать валентные электроны и переходить в положительно заряженные ионы Ионы типичных металлов всегда заряжены положительно Однако способность к отдаче электронов у различных металлов проявляется по-разному: у одних более легко, у других с некоторыми затруднениями Чем легче металл отдает свои электроны, тем он активнее вступает во взаимодействие с другими элементами
Например, если кусочек цинка опустить в раствор свинцовой соли, то цинк, отдавая свои валентные электроны ионам двухвалентного свинца, начинает быстро растворяться, а ионы свинца разряжаются и выделяются в виде металлического свинца
2п + РЬ(Ж)з)2 = РЬ + 2п(Ж)з)2.
Если же в раствор цинковой соли погрузить кусочек свинца, то реакции не произойдет, так как свинец менее активен, чем цинк Все металлы можно расположить последовательно в ряд по убывающей химической активности. Этот ряд получил название «Бекетова ряда» в честь ученого, изучившего явления вытеснения одних металлов другими, «вытеснительного ряда» или «ряда напряжений». Этот ряд выглядит следующим образом: калий (К), кальций (Са), натрий (Nа), магний (М§), алюминий (А1), марганец (Мп), цинк (2п), железо (Ре), никель (М1), олово (5п), свинец (РЬ), медь (Си), ртуть (Н^), серебро (А§), золото (Аи).
При изготовлении протезов и аппаратов различных конструкций с применением неоднородных металлов необходимо учитывать химическую активность этих металлов, а также металлов, уже находя-
23
щихся в полости рта в составе пломб, вкладок, коронок и др. В противном случае могут возникнуть окислительно-восстановительные реакции, способствующие понижению прочности изготовляемых конструкций протезов.
Почти все металлы, реагируя с кислородом, образуют основные окислы, реже кислотные. Непосредственно не реагируют с кислородом в обычных условиях лишь некоторые металлы: золото, металлы платиновой группы (платина, палладий, иридий, рутений, родий, осмий), серебро, получившие название благородных металлов (см. с. 30). Большинство из этих металлов имеет высокую температуру плавления, большую плотность и не имеет ал-лотропных форм, т. е. в свободном виде не образует несколько простых веществ, различных по строению и свойствам (например, элемент углерод встречается в форме алмаза, графита и углерода).
Металлы обладают высокой способностью отражать своей поверхностью световые излучения, что является причиной своеобразного, металлического, блеска. Металлы, по сравнению с другими веществами, хорошо проводят электричество и теплоту. Под влиянием внешней силы легко изменяют свою форму, т. е. обладают хорошей пластичностью, легко куются и, не разрушаясь, прокатываются в листы или вытягиваются в проволоку. Это позволяет при сравнительно несложной технологии изготовлять из металлов изделия различной формы и величины, в том числе и зубные протезы различных конструкций. Однако каждый из металлов имеет свое, характерное только для него, внутреннее строение, что определяет его плотность, твердость, температуру плавления, кипения и др. Все металлы, за исключением ртути, в обычных условиях находятся в твердом состоянии.
Важными показателями, характеризующими свойства металлов, являются твердость, прочность и упругость.
Внешне изделие из металла напоминает однородное вещество, но на изломе обнаруживается сложное его строение. Зерна металлов разнообразны как по величине, так и по форме; располагаются в строгой последовательности или беспорядочно. Все металлы в твердом состоянии имеют кристаллическое характерное строение.
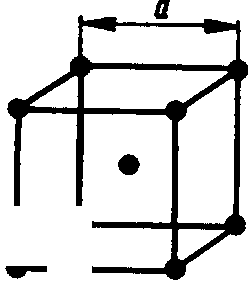
Для металлов наиболее характерны следующие типы кристаллических решеток (рис. 1).
1. Решетка куба с центрированными гранями наблюдается у алюминия, золота, меди, свинца, железа, находящегося в 'у-фазе, т. е. в пределах температуры 910...1390 °С (рис. 1,а).
2. Решетка объемно-центрированного куба, свойственна для хрома и а-железа (при температуре ниже 910 или свыше 1390 °С) (рис. 1,б).
24
|
|
|
^ |
• |
^ |
• ^ |
• • |
• |
|
• |
^ |
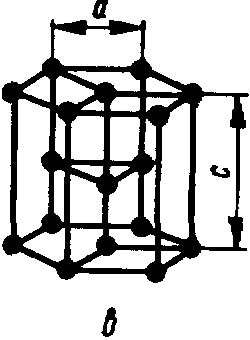
а 5 Рис.
1. Элементарные кристаллические
решетки:
о — кубическая
объемно-центрированная; С — кубическая
гранецентрированная; в — гекса-
гональная.
Свойства металлов зави-]^— сят как от типа кристалли-— ческой решетки, так и от направлений, в которых расположены кристаллы.
Кристаллическая решетка некоторых металлов меняется в зависимости от температуры его нагрева и давления. Свойство металлов изменять кристаллическую решетку при различных температурных режимах называется аллотропным превращением металлов.
Несмотря на то что металлы отличают-
Классификация металлов ся друг от друга строением и свойства-
ми, все они по ряду признаков могут быть объединены в определенные группы. Металлы принято классифицировать по их положению в периодической системе элементов. Однако такая классификация мало удовлетворяет интересы промышленности, так как в ней не указаны многие физико-химические и механические свойства. В промышленности металлы чаще всего разделяют на черные, цветные и редкие.
По плотности металлы могут быть разделены на две большие группы — легкие и тяжелые. К легким относят такие металлы, плотность которых не превышает 5 г/см3, к тяжелым — все остальные.
По взаимодействию металлов с кислородом их разделяют на благородные и неблагородные.
В стоматологической практике все материалы, в том числе и металлы, принято разделять на основные и вспомогательные. „ . Металлы могут быть одно- и многокрис-йТа^ч^^^^^^^^ таллическими. Расположение кристаллов зависит от факторов, воздействующих на металл. В отливаемых деталях кристаллы находятся в определенной направленности к поверхности охлаждения. Эта ориентация зерен может резко изменяться в зависимости от характера воздействия различных механических факторов. Например при волочении все кристаллы располагаются вдоль направления вытяжки, а при прокатке кристаллографическая плоскость становится в плоскости прокатки. На характер ориентации зерен влияют не только условия и степень деформации, но и температура, длительность и характер последующего нагрева (отжига). Имеет значение
25
и то, был ли это суммарный отжиг клу отжиг с промежутками в процессе деформации. Чем сильнее деформация после последнего нагрева, тем резче выражена ориентационная направленность кристаллов. Даже при слабых напряжениях (механических деформациях) у поликристаллических металлов появляются сдвиги в отдельных зернах, одновременно повороты и смещение их, в связи с чем возникают параллельные линии кристаллов При резком увеличении степени деформации коренным образом меняется структура металла. Зерна вытягиваются в направлении деформирующей силы, а затем происходит их дробление. Все это приводит к искажению кристаллической решетки металла Характерно, что часть этих изменений остается и после снятия нагрузки.
Неоднородность строения, а также возникающая вследствие этой неоднородности местная концентрация напряжений является причиной усталости металлов. Усталостью металлов называют постепенное, медленное распространение сдвигов по отдельным кристаллам, ведущее сначала к местному разрушению — появлению микротрещин, а затем к общему разрушению металла.
Пределом усталости является то максимальное напряжение, которое выдерживает материал, не разрушаясь при достаточно большом количестве циклов смены нагрузки. Каждый металл имеет свое предельное количество циклов. Для железа и его сплавов количество циклов достигает 10 000 000.
Рекристаллизация — снятие упругих на-Рекристаллизация пряжений и искажений в кристаллической решетке металла. Этот процесс может идти различными путями: 1) за счет перемещения атомов в пределах одного монокристалла, не подвергающегося пластической деформации, т. е. отдыха металла (при этом происходит только частичное восстановление кристаллической решетки и свойств металла); 2) за счет образования и роста новых кристаллов.
Различают рекристаллизацию обработки и рекристаллизацию собирательную. Рекристаллизация обработки характеризуется ростом новых кристаллов за счет ранее деформированных. Образовавшиеся новые кристаллы имеют менее искаженную решетку.
Собирательная рекристаллизация происходит при воздействии на металл высоких температур. Для каждого металла существует своя минимальная температура, ниже которой процесс рекристаллизации практически невозможен.
Для определения температуры рекристаллизации необходимо знать температуру плавления металла. Температура рекристаллизации любого металла находится в пределах 0,3 ..0,4 °С от его точки плавления,т.е
Трекристал == 0,4 • Тплавл >
где Тплавл—температура плавления металла, °С 26
Рекристаллизация значительно изменяет строение и механические свойства металла и поэтому широко применяется в технике. Рекристаллизация делает возможным продолжать механическую обработку уже наклепанных и ставших хрупкими металлов. Ее широко используют в промежуточных нагревах, а также при окончательном отжиге наклепанных металлов, если необходимо возвратить им пластичность. При рекристаллизации предел прочности, упругости и твердости металла уменьшается, удлинение и сопротивление удару увеличиваются.
Рекристаллизацией широко пользуются при изготовлении многих стоматологических изделий. При неправильном выборе режима обработки рекристаллизация может принести большой вред.
Разрушение металлов под воздействием Коррозия окружающей среды называется коррозией. Почти все металлы под воздействием газообразной или жидкой среды подвергаются более или менее быстрому разрушению
Соприкосновение металла с газообразной средой или воздухом сопровождается образованием на его поверхности соединений (окислов или основных соединений), покрывающих поверхность металла тонким слоем и тем самым предохраняющих его от дальнейшего взаимодействия с окружающей средой, а следовательно, от дальнейшего разрушения.
Более сложные коррозийные процессы происходят при взаимодействии металла с растворами кислот, солей и щелочей, т. е при взаимодействии определенных веществ в жидкой среде. Растворенные в воде вещества не только не способствуют образованию защитной пленки вокруг металла, но могут под воздействием электрических процессов проникать в глубь металла, способствуя дальнейшему развитию коррозии.
Металлы в чистом виде почти не подвергаются коррозии. Железо 99,999 % чистоты почти не ржавеет. Значительно труднее поддается коррозии чистый цинк, чем цинк, содержащий хотя бы минимальное количество примесей.
Технические металлы всегда содержат различные примеси, а это создает благоприятные условия для коррозии. Неоднородный металл рассматривается как сложный комплекс анодных и катодных участков, обусловливающих совокупность процессов, проходящих на границе металла с электролитом.
Анодными и катодными участками могут служить как кристаллы разных фаз двухфазных или многофазных металлов, так и различно ориентированные участки кристаллов однофазных металлов, даже участки одного и того же кристалла, если он находится в различном энергетическом состоянии (напряжении). Степень выраженности напряжения в двух последних случаях значительно сла-
27
Рис. 2. Избирательная
коррозия:
7 — интеркристаллическая;
2 —
транскристаллическая.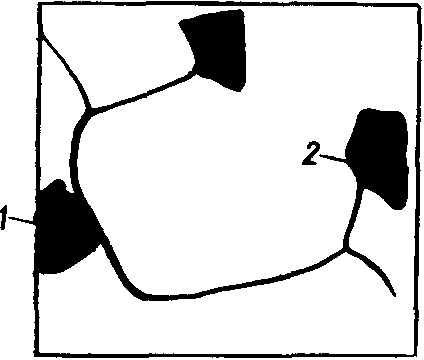
По характеру распространения различают равномерную (общую), местную и избирательную (интеркристаллическую и транскристаллическую коррозию).
Равномерной, или общей, называется коррозия, при которой металлические изделия подвергаются разрушению по всей поверхности. Чаще она встречается при мелкодисперсной структуре сплава. Это менее опасный и медленно протекающий процесс коррозийного разрушения.
Местной называется коррозия, при которой участки поражения располагаются очагами, пятнами, точками. Обычно очаги коррозии появляются в участках грубой структуры металла или участках, имеющих оставшееся напряжение, механическое повреждение, трещины и др. В зависимости от расположения местная коррозия может значительно снизить или привести в полную непригодность металлическую деталь.
Избирательной называется коррозия, при которой разрушение происходит в глубине металла. Это один из наиболее сложных и опасных видов разрушения металла. Различают избирательную интеркристаллическую коррозию, когда процесс разрушения распространяется по границам кристаллов (рис. 2, /), и избирательную транскристаллическую коррозию, когда процесс разрушения распространяется по определенным кристаллографическим направлениям или через отдельные кристаллы (рис.2, 2).
Избирательная коррозия наблюдается при крупнозернистой структуре металла, имеющего различные включения других металлов или карбиды.
Основой коррозии является реакция между ионами металла и полярными молекулами раствора. Скорость реакции зависит как от характера металла (сплава), его примесей, структуры, способа термической и механической обработки, так и от свойств окружающей среды (раствора, сплава). Реакцию эту можно замедлить или даже полностью предотвратить.
28
Защита металлов
от коррозии
веществами (красками), изолирующими металл от окружающей среды. Этот способ может быть применен только для тех изделий или их частей, которые не находятся в соприкосновении и трении с другими деталями, так как при этом защитный слой краски быстро стирается и его действие прекращается.
Более эффективным способом защиты металла от разрушения является покрытие поверхности изделия другими металлами. С электролитической точки зрения защитное действие оказывает металл, который в паре с защищаемым металлом является анодом, например, цинк защищает от коррозии железо (оцинкованное железо), а олово усиливает его разрушение.
Важное место в борьбе с коррозией металлов занимает хромирование — покрытие поверхности металлических изделий хромом. Известны два способа хромирования: электролитическое и диффузное. Электролитическое хромирование — покрытие изделия хромом путем его осаждения. Этот способ широко распространен в технике. Были попытки применения его и в стоматологической практике, однако на хромированной поверхности протезов появляются трещины, внутри и вокруг которых со временем образуются темные точки и зеленоватые пятна коррозии. Больные нередко жалуются на неприятный вкус во рту и эстетическую неполноценность таких протезов.
Более эффективно диффузное хромирование — диффузия хрома в поверхность металла путем пропускания хлористого водорода через кусочки хрома или феррохрома при температуре 800...850 °С и направления полученного СгС\г на поверхность изделия при температуре 950...1050 °С. Полученный хромированный слой отличается высокой твердостью, стойкостью против стирания и антикоррозийной стойкостью в различных средах. Однако этот способ не получил достаточного распространения из-за технической сложности.
В настоящее время для предохранения металлических зубных протезов от коррозии и снижения их электрической активности поверхность протезов покрывают нитридами титана и нитридами циркония. На гладко отполированную поверхность протеза (полировка не ниже 10 класса чистоты) наносят слой из нитрида титана или нитрида циркония или поочередно.
Существует два способа покрытия: осаждением и ионно-плаз-менным распылением. В стоматологической практике нашел применение способ ионно-плазменного распыления. Сущность его заключается в бомбардировании в вакууме поверхности металлической детали или протеза ионами титана или циркония. Изделие, подлежащее покрытию, располагают на катоде аппарата «Булат».
29
Под воздействием тока высокого напряжения в вакуумной камере аппарата происходит оседание нитрида тонким слоем на поверхности изделия. Температура в области изделия не должна превышать 300 °С. Толщина покрытия зависит от режима и продолжительности воздействия, а прочность — от толщины слоя. Однако с увеличением толщины слоя покрытия адгезия его с основой протеза несколько уменьшается.
Так как нитридное покрытие, наряду с высокой твердостью, обладает и большой хрупкостью, то для увеличения прочности чередуют слои покрытия (нитрид титана, нитрид циркония, основа изделия). При этом возникшие трещины в одном слое покрытия ку-пируются соседними слоями и полного разрушения покрытия изделия не наступает. Толщина общего слоя покрытия — многослойного защитного нитридного покрытия (МЗНП) — не должна превышать 10 мкм. Многочисленными исследованиями не выявлено отрицательного влияния нитридных покрытий на организм. Электрохимический потенциал зубных протезов, изготовленных с применением МЗНП, близок по величине • и знаку электрохимическому потенциалу зубных протезов, изготовленных из сплавов золота.
Применение МЗНП является одним из мероприятий, направленных на профилактику и устранение патологических состояний, возникающих вследствие неоднородности структуры применяемых сплавов металлов и электрической активности протезов.
