
- •В.М. Васюков
- •Курс лекций
- •Часть I. Теоретическая химия
- •Глава 1. Основные понятия и законы химии
- •Основные понятия химии
- •Основные положения атомно-молекулярной теории
- •Газовые законы
- •Глава 2. Строение атома и периодический закон Модели строения атома
- •Квантовые числа электронов
- •Электронные конфигурации атомов
- •Ядро атома и радиоактивные превращения
- •Периодический закон
- •Глава 3. Химическая связь Валентность и степень окисления
- •Ковалентная связь
- •Ионная связь
- •Металлическая связь
- •Межмолекулярные взаимодействия
- •Глава 4. Комплексные соединения
- •Глава 5. Состояние вещества
- •Глава 6. Физико-химические закономерности протекания химических реакций Химическая термодинамика
- •Химическая кинетика и катализ
- •Обратимые и необратимые реакции. Состояние химического равновесия
- •Глава 7. Физико-химическая теория растворов электролитов и неэлектролитов Механизм образования растворов и их классификация
- •Идеальные и реальные растворы. Растворение как физико-химический процесс
- •Зависимость растворимости различных веществ от природы растворителя, температуры и давления
- •Законы разбавленных растворов
- •Способы выражения концентрации (состава) растворов
- •Электролиты и электролитическая диссоциация
- •Гидролиз солей
- •Глава 8. Дисперсные системы
- •Классификации дисперсных систем
- •Оптические и молекулярно-кинетические свойства дисперсных систем
- •Поверхностные и адсорбционные явления
- •Коллоидные (коллоидно-дисперсные) системы
- •Глава 9. Теория окислительно-восстановительных процессов Окислительно-восстановительные реакции
- •Химические источники электрической энергии. Электродные потенциалы
- •1) Металлы, обладающие более электроотрицательным потенциалом, способны вытеснить менее активные металлы (с более положительным потенциалом) из водных растворов их солей;
- •Коррозия металлов
- •Электролиз
- •Восстанавливается вода Восстанавливается вода и катионы металла Восстанавливается катионы металла
- •Глава 10. Качественный и количественный анализ веществ
- •Качественный анализ
- •Классификация катионов на аналитические группы
- •Классификация анионов на аналитические группы
- •Количественный анализ
- •Химические методы анализа
- •Физические и физико-химические методы анализа
- •Часть II. Неорганическая химия
- •Глава 11. Важнейшие классы неорганических соединений
- •Основания (гидроксиды металлов)
- •Кислоты
- •Глава 12. Элементы I группы
- •Водород
- •Глава 13. Элементы II группы
- •Бериллий
- •Глава 14. Элементы III группы
- •Алюминий
- •Лантаноиды
- •Актиноиды
- •Глава 15. Элементы IV группы
- •Углерод
- •Кремний
- •Глава 16. Элементы V группы
- •Глава 17. Элементы VI группы
- •Кислород
- •Глава 18. Элементы VII группы
- •Глава 19. Элементы VIII группы
- •Часть III. Органическая химия Глава 20. Общая характеристика органических соединений
- •Теория строения органических соединений
- •Атомы в молекулах соединены между собой в определенном порядке химическими связями согласно их валентности; углерод во всех органических соединениях четырехвалентен.
- •Свойства вещества определяются не только качественным составом, но и его строением, взаимным влиянием атомов, как связанных между собой химическими связями, так и непосредственно не связанных.
- •Строение молекул может быть установлено на основе изучения их химических свойств.
- •Формулы органических соединений
- •Классификация органических соединений
- •Номенклатура органических соединений
- •Изомерия органических соединений
- •Взаимное влияние атомов в молекуле и реакционная способность органических соединений
- •Общая характеристика органических реакций
- •Промышленное производство органических соединений
- •Глава 21. Алканы Номенклатура и изомерия
- •Физические свойства
- •Способы получения
- •Химические свойства
- •Применение
- •Глава 22. Циклоалканы Номенклатура и изомерия
- •Физические свойства
- •Получение
- •Химические свойства
- •Глава 23. Алкены (олефины) Номенклатура и изомерия
- •Физические свойства
- •Получение
- •Химические свойства
- •Применение
- •Глава 24. Алкадиены (диеновые углеводороды) Номенклатура и изомерия
- •Физические свойства
- •Получение
- •Химические свойства
- •Применение
- •Глава 25. Алкины (ацетилены) Номенклатура и изомерия
- •Физические свойства
- •Получение
- •Химические свойства
- •Применение
- •Глава 26. Ароматические углеводороды (арены) Номенклатура и изомерия
- •Физические свойства
- •Способы получения
- •Химические свойства
- •Правила ориентации (замещения) в бензольном кольце
- •Применение
- •Глава 27. Гидроксильные соединения (спирты)
- •Одноатомные спирты (алкоголи) Номенклатура и изомерия
- •Физические свойства
- •Получение
- •Химические свойства
- •Применение
- •Многоатомные спирты
- •Получение
- •Химические свойства
- •Применение
- •Физические свойства
- •Способы получения
- •Химические свойства
- •Применение
- •Глава 28. Карбонильные соединения (оксосоединения) Номенклатура и изомерия
- •Метаналь этаналь
- •Физические свойства
- •Получение
- •Химические свойства
- •Применение
- •Глава 29. Карбоновые кислоты Номенклатура и изомерия
- •Физические свойства
- •Получение
- •Химические свойства
- •Применение
- •Глава 30. Сложные эфиры. Жиры Номенклатура и изомерия
- •Физические свойства
- •Химические свойства
- •Жиры и масла
- •Глава 31. Углеводы (сахара)
- •Моносахариды Номенклатура и изомерия
- •Физические и химические свойства глюкозы
- •Дисахариды
- •Полисахариды
- •Глава 32. Амины
- •Предельные алифатические амины Номенклатура и изомерия
- •Физические свойства
- •Получение
- •Химические свойства
- •Применение
- •Ароматические амины
- •Физические свойства
- •Химические свойства
- •Применение
- •Глава 33. Аминокислоты, пептиды и белки
- •Аминокислоты Номенклатура и изомерия
- •Физические свойства
- •Получение
- •Химические свойства
- •Пептиды
- •Физические свойства
- •Химические свойства
- •Биологическое значение белков
- •Глава 34. Гетероциклические соединения
- •Шестичленные гетероциклы
- •Пятичленные гетероциклы
- •Нуклеиновые кислоты Строение нуклеиновых кислот
- •Биологическая роль нуклеиновых кислот
- •Глава 35.Синтетические высокомолекулярные соединения
- •Общая характеристика полимеров
- •Пластмассы
- •Волокна
- •Каучуки
- •Литература
- •Приложения Растворимость неорганических веществ в воде при 25°c
Глава 31. Углеводы (сахара)
Углеводы – это природные органические соединения, имеющие общую формулу Сm(Н2О)n (т, п > 3). Углеводы подразделяют на три большие группы: моносахариды, олигосахариды и полисахариды.
Моносахаридами называют такие углеводы, которые не могут гидролизоваться с образованием более простых углеводов.
Олигосахариды – это продукты конденсации небольшого числа моносахаридов, например сахароза – С12Н22О11. Полисахариды (крахмал, целлюлоза) образованы большим числом молекул моносахаридов.
Моносахариды Номенклатура и изомерия
Простейший моносахарид – глицериновый альдегид, С3Н6О3:
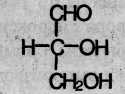
Остальные моносахариды по числу атомов углерода подразделяют на тетрозы (С4Н8О4), пентозы (С5Н10O5) и гексозы (С6Н12О6). Важнейшие гексозы – глюкоза и фруктоза.Все моносахариды представляют собой бифункциональные соединения, в состав которых входят неразветвленный углеродный скелет, несколько гидроксильных групп и одна карбонильная группа. Моносахариды с альдегидной группой называют альдозами а с кетогруппой – кетозами. Ниже приведены структурные формулы важнейших моносахаридов:
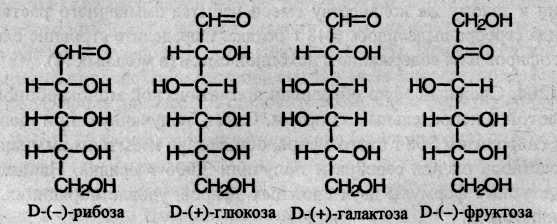
Все эти вещества содержат три или четыре асимметрических атома углерода, поэтому они проявляют оптическую активность и могут существовать в виде оптических изомеров. Знак в скобках в названии углевода обозначает направление вращения плоскости поляризации света: (–) обозначает левое вращение, (+) – правое вращение. Буква D перед знаком вращения означает, что во всех этих веществах асимметрический атом углерода, наиболее удаленный от карбонильной группы, имеет такую же конфигурацию (т.е. направление связей с заместителями), что и глицериновый альдегид, структура которого приведена выше. Углеводы с противоположной конфигурацией относятся к L-ряду:
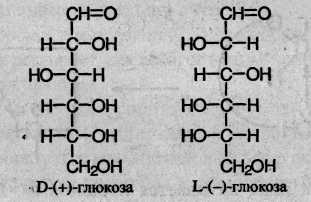
Обратите внимание на то, что углеводы D- и L-ряда являются зеркальными отражениями друг друга. Большинство природных углеводов относится к D-ряду.
Установлено, что в кристаллическом состоянии моносахариды существуют исключительно в циклических формах. Например, глюкоза в твердом виде обычно находится в α-пиранозной форме. При растворении в воде α-глюкопираноза медленно превращается в другие таутомерные формы вплоть до установления равновесия. Это является своеобразной кольчатоцепной таутомерной системой.
Физические и химические свойства глюкозы
Глюкоза С6Н12О6 представляет собой белые кристаллы, сладкие на вкус, хорошо растворимые в воде. В линейной форме молекулы глюкозы содержат одну альдегидную группу, и пять гидроксильных групп. В кристаллах молекулы глюкозы находятся в одной из двух циклических форм (α- или β-глюкоза), которые образуются из линейной формы за счет взаимодействия гидроксильной группы при 5-м атоме углерода с карбонильной группой:
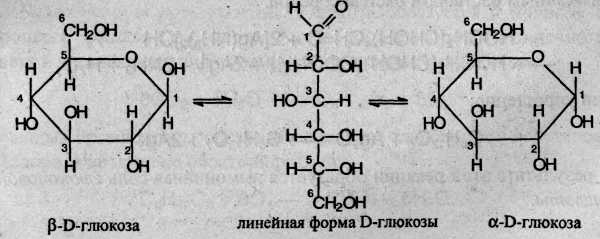
Данное равновесие существует в водном растворе. Буква α в названии циклических форм моносахаридов означает, что группа –ОН при первом углеродном атоме и группа –СН2ОН при шестом углеродном атоме находятся по разные стороны от плоскости кольца; в β-моносахаридах эти группы находятся по одну сторону от плоскости кольца.
Процесс образования циклических форм (кольчато-цепная таутомерия) глюкозы из линейной можно представить следующим образом. Атом водорода группы ОН при 5-м атоме углерода перемещается к атому кислорода альдегидной группы СH=O, а между атомами С-1 и С-5 устанавливается связь через атом кислорода с образованием шестичленного цикла (циклического полуацеталя):

Шестичленный цикл называется пиранозным. Если во взаимодействие с альдегидной группой вступит группа ОН при 4-м атоме углерода, то образуется пятичленный цикл, называемый фуранозиым.
Группу ОН при первом углеродном атоме в циклических формах называют гликозидным гидроксилом. Эта группа резко отличается по свойствам от остальных групп ОН. В частности, при реакциях со спиртами в присутствии кислот гликозидный гидроксил легко замещается на группу OR с образованием простого эфира.
Химические свойства глюкозы обусловлены наличием в ее молекуле альдегидной (в линейной форме) и гидроксильных групп.
1. Реакции альдегидной группы. Глюкоза вступает в реакцию с аммиачным раствором оксида серебра:
![]()
или упрощенно:
![]()
В результате этой реакции образуется аммонийная соль глюконовой кислоты.
Глюкоза при нагревании окисляется гидроксидом меди (II) в глюконовую кислоту:
![]()
При восстановлении альдегидной группы глюкозы образуется шестиатомный спирт сорбит:
![]()
Поскольку циклическая форма глюкозы не содержит альдегидной группы, глюкоза не вступает в некоторые реакции, характерные для альдегидов, например в реакцию с NаНSО3.
2. Реакции гидроксильных групп. С гидроксидом меди (II) без нагревания глюкоза реагирует как многоатомный спирт и дает характерное синее окрашивание.
При действии метилового спирта в присутствии каталитических количеств соляной кислоты гликозидный гидроксил замещается на группу ОСН3, и образуется монометиловый эфир глюкозы.
3. Брожение гексоз (пентозам брожение не свойственно) представляет собой многостадийный биохимический процесс, протекающий под действием ферментов, выделяемых дрожжевыми грибами, бактериями или плесневыми грибами. На этих процессах основана биотехнология многих ценных химических продуктов, таких, как этанол (спиртовое брожение), молочная и лимонная кислота (соответственно, молочнокислое и лимоннокислое брожение) и др. Основные виды брожения:
а) спиртовое брожение:
![]()
б) молочнокислое брожение:
![]()
4. Эпимеризация моносахаридов в слабощелочных растворах. Эпимерными моносахаридами являются глюкоза, манноза, фруктоза, которые имеют одинаковую конфигурацию у третьего, четвертого и пятого атомов углерода. В присутствии щелочи происходят превращения эпимеров через промежуточное образование ендиола:
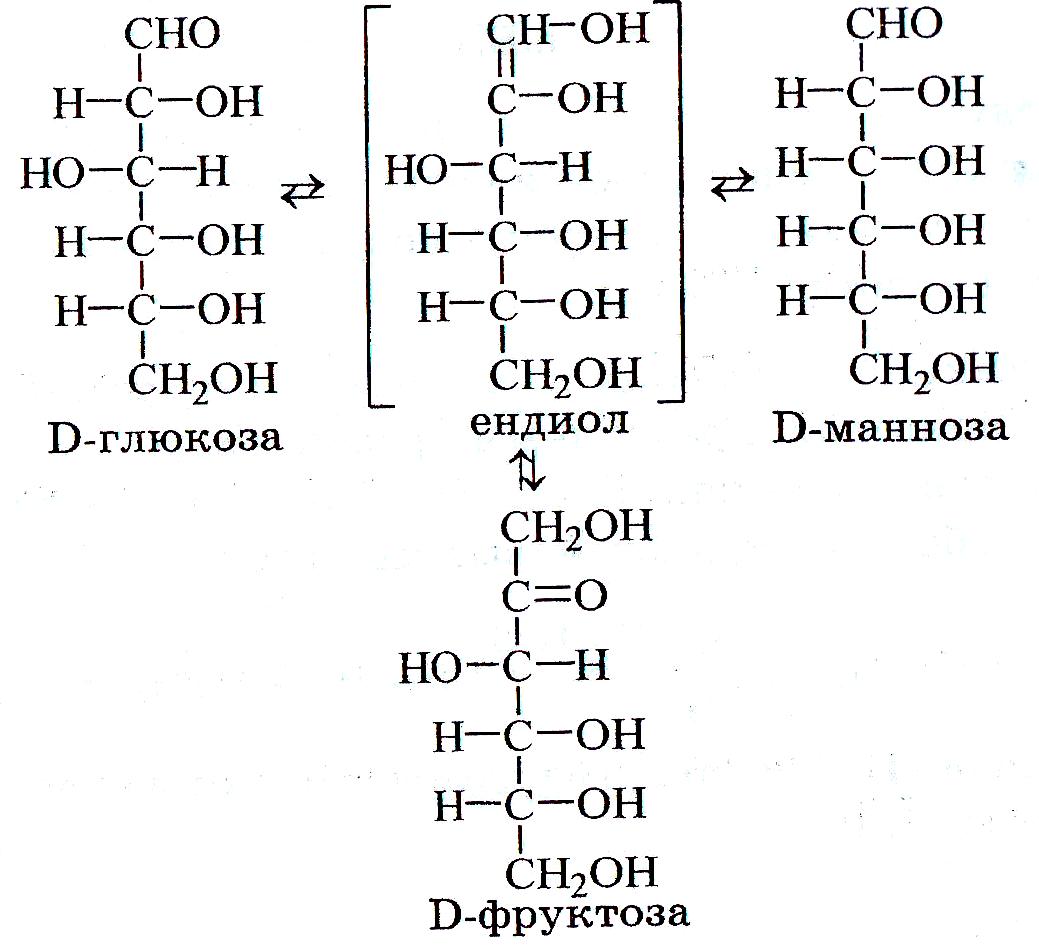
Глюкоза с известковой водой через 5 суток дает смесь глюкозы (63%), фруктозы (31%) и маннозы (6%). Эпимеризация встречается в биохимических процессах и происходит при действии ферментов эпимераз.
Биологическая роль глюкозы. Глюкоза образуется в природе в процессе фотосинтеза, протекающего под действием солнечного света в листьях растений. Суммарное уравнение фотосинтеза:
![]()
В живых организмах происходит окисление глюкозы под действием кислорода воздуха по обратной реакции:
![]()
При этом выделяется энергия, которая используется организмом. Таким образом, глюкоза играет роль аккумулятора солнечной энергии.
Фруктоза С6Н12О6 – изомер глюкозы. Как и глюкоза, она может существовать в линейной и циклических формах. В линейной форме фруктоза представляет собой кетоноспирт с пятью гидроксильными группами, а в циклической – преимущественно кетофуранозу, т.е. пятичленный цикл с атомом кислорода:
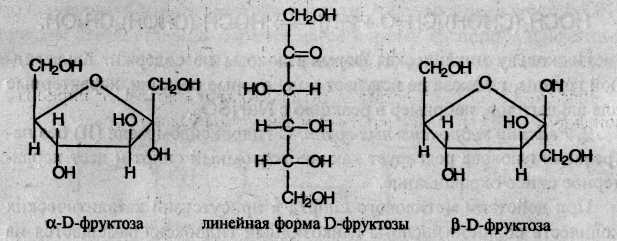
Фруктоза вступает во все реакции многоатомных спиртов, но, в отличие от глюкозы, не реагирует с аммиачным раствором оксида серебра.
