- •1. Назначение и функции, выполняемые ао.
- •2. Классификация ао по видам оборудования.
- •10) Авиационные тренажеры:
- •3. Особенности работы авиационного оборудования.
- •4. Требования, предъявляемые к авиационному оборудованию.
- •5. Дать определение сэс вс и её составляющих.
- •6. Как классифицируется сэс вс.
- •7. Структура сэс вс переменного тока.
- •8. Структура сэс вс постоянного тока.
- •9. Структура первичной сэс вс.
- •10. Структура вторичной сэс вс.
- •11. Что входит в состав срэ вс?
- •12. Перечислить наименования электрических проводов используемых в системах распределения электрической энергии. В чём их отличия.
- •13. Перечислить виды разъёмных устройств используемых в системах распределения электрической энергии.
- •14. Перечислить виды элементов регулирования, защиты и управления сэс ла.
- •15. Назначение элементов регулирования, защиты и управления сэс ла.
- •16. Назначение металлизации и экранирования в срэ ла.
- •17. Назначение и принцип действия статических разрядников.
- •18. Общие сведения, назначение и классификация химических источников тока.
- •19. Основные положения теории электролитической диссоциации. Электролиты.
- •20. Электрические характеристики химических источников тока.
- •23. Общие характеристики для всех типов электрохимических систем.
- •21. Принцип действия кислотных аккумуляторов.
- •22.Пояснить процесс двойной сульфатации.
- •24. Основные технические и электрические характеристики свинцово-кислотных аб.
- •25.Конструкция авиационных кислотных аккумуляторных батарей.
- •26. Пояснить сущность вредной сульфатации электродов.
- •27. Принцип действия серебряно-цинковых аккумуляторов.
- •28.Пояснить процесс дендритообразования.
- •29. Общие характеристики для всех типов электрохимических систем.
- •30. Основные технические и электрические характеристики серебряно-цинковых аб.
- •31. Конструкция авиационных серебряно-цинковых аккумуляторных батарей.
- •32. Назначение, конструкция и принцип действия интегрирующего счётчика ампер-часов (иса).
- •33. Принцип действия авиационных никель-кадмиевых аккумуляторных батарей.
- •34. Конструкция и характеристики авиационных никель-кадмиевых аккумуляторных батарей.
- •35. Меры безопасности при работе с бортовыми аккумуляторными батареями.
- •36. Общие правила эксплуатации авиационных аккумуляторных батарей.
- •20Нкбн-25 (Ni-Cd)
- •37. Особенности эксплуатации авиационных аккумуляторных батарей.
- •38. Установка аккумуляторных батарей на летательный аппарат, основные правила содержания аккумуляторов.
- •39. Устойчивость работы системы регулирования напряжения и способы её повышения.
- •40. Способы уменьшения температурной погрешности регулятора напряжения типа урн.
- •41. Назначение параллельной работы генераторов.
- •42. Защита генераторов постоянного тока от обратного тока.
- •43. Защита генераторов и бортовой сети от перенапряжения.
- •44. Импульсные автоматы защиты питательной сети.
- •45. Требования, предъявляемые к точности стабилизации напряжения в системах электроснабжения летательных аппаратов.
- •46. Методы регулирования напряжения. Принципы построения регуляторов напряжения авиационных генераторов.
- •47. Параллельная работа источников электроэнергии постоянного и переменного токов в авиационных системах электроснабжения.
- •48. Назначение, принцип действия, устройство, работа и особенности эксплуатации урн типа рн - 180, рн - 600, рн - 120у.
- •49. Назначение, принцип действия, устройство и особенности эксплуатации дифференциально-минимального реле дмр-600т.
- •50. Назначение, классификация и основные электрические характеристики авиационных генераторов.
- •51. Принцип действия и конструктивные особенности авиационных генераторов.
- •52. Основные типы генераторов постоянного тока и их конструктивные особенности.
- •53. Электрические и эксплуатационные характеристики генераторов постоянного тока.
- •54. Основные типы генераторов переменного тока и их конструктивные особенности.
- •55. Электрические и эксплуатационные характеристики генераторов переменного тока.
- •57. Охлаждение авиационных генераторов.
- •58. Правила технической эксплуатации генераторов постоянного тока типа стг, гс.
- •60. Правила технической эксплуатации генераторов переменного тока типа го.
- •63. Назовите аварийные режимы при эксплуатации электроэнергетических систем вс.
- •64. Назначение питательной сети вс.
- •65. Что понимается под основной сетью?
- •66. Что понимается под аварийной сетью?
- •67. Поясните работу схемы питательной сети самолёта-истребителя.
- •68. Требования, предъявляемые к аппаратуре защиты энергосистем летательных аппаратов.
- •69. На какие группы делится коммутационная аппаратура в зависимости от способа управления?
- •70. Пояснить принцип действия реле и контакторов.
- •71. Пояснить принцип работы коробки переключающих реле кпр-9.
- •72. Типы плавких предохранителей применяемых на вс.
- •73. Принцип действия плавких предохранителей.
- •74. Типы автоматов защиты и их принцип действия.
- •75. Назначение и типы дмр.
- •76. Защита генераторов и их фидеров от коротких замыканий.
- •77. Типы биметаллических автоматов защиты.
- •78. Типы плавких предохранителей.
- •79. Работа коробки коч-62б 2 серии.
- •80. Работа автомата азп-8м 4 серии.
- •81. Работа автомата азп-8м 5 серии.
- •82. Принцип действия защиты при несимметрии нагрузки.
- •83. Принцип действия датчика направления тока днт-1.
- •84. Типы автоматов защиты и их принцип действия.
- •85. Характерные отказы аппаратуры защиты и управления и методы их предупреждения.
- •86. Требования предъявляемые к системам распределения электроэнергии вс.
- •87. Состав срэ и классификация по способу распределения электроэнергии.
- •88. Классификация по электрическим параметрам систем распределения электроэнергии и по конфигурации систем распределения электроэнергии.
- •89. Классификация по системе распределения электроэнергии.
- •90. Назначение и состав системы распределения эл. Энергии самолёта Ан-26.
- •91. Назначение и состав системы распределения эл. Энергии вертолёта Ми-8.
- •1.1. Система генерирования
- •92. Типы бортовых эл. Проводов. 93. Классификация электрических проводов.
- •94. Меры безопасности при работе с системами электроснабжения летательных аппаратов.
- •95. Характерные отказы электрических сетей ла и методы их предупреждения.
19. Основные положения теории электролитической диссоциации. Электролиты.
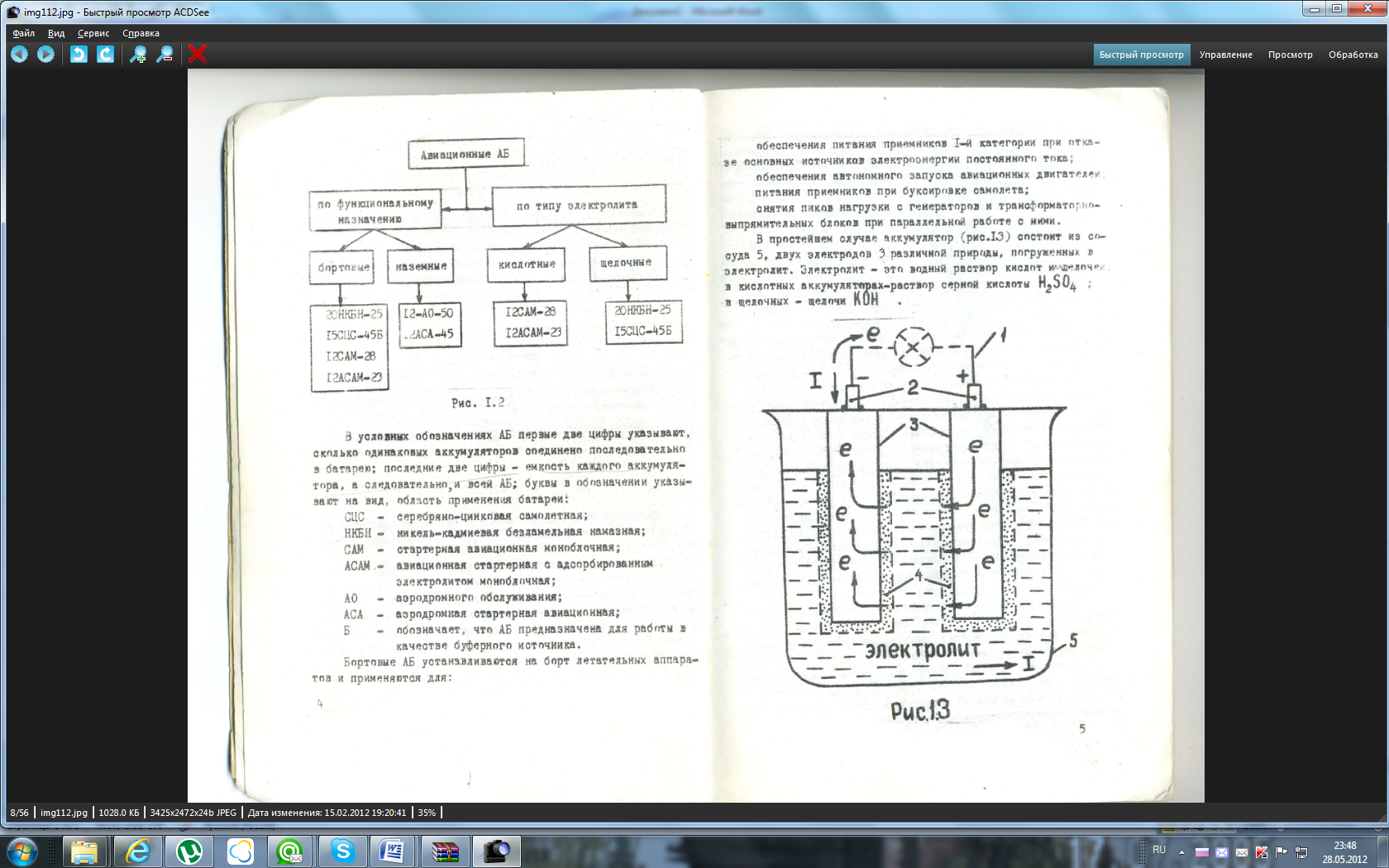
5 – сосуд; 3 – электроды различной природы; 2 – выводы; 1 – внешняя проводящая цепь; 4 – граница между электролитом и частицами активных масс электродов.
Электролит – водный раствор кислоты (серной) или щёлочи (гидроксид калия).
Электроды – проводники, одним концом соединённые с выводами, другим погружённые в электролит, металлические пластины или сетки, с нанесёнными на них реагирующими веществами.
Основа работы – взаимодействие окислителя и восстановителя, окислительно-восстановительная реакция. Восстановитель, окисляясь, отдаёт электроны, а окислитель, восстанавливаясь, принимает их. При погружении электродов электролит в них образуется разность потенциалов. Это происходит из=за того, что при погружении металлического электрода под действие сил электролитической упругости упругости металл растворяется. При переходе в электролит, каждый атом теряет некоторое количество электронов с внешней орбиты, образуя положительный ион. Положительные ионы располагаются вблизи электродов на границе «электрод-электролит». В связи с тем, что электроны атомов, вышедших из металла, остались на электроде, а электролит пополнился положительными ионами металла, электрод приобретает отрицательный заряд, а прилегающий слой электролита – положительный. Разность потенциалов между электродом и электролитом называют электродным потенциалом. Растворение металла в электролите прекратится тогда, когда силы взаимодействия электрического поля, образовавшегося в пограничном слое, уравновесят силы электролитической упругости растворения металла. При соединении электродов внешней проводящей цепью, по ней пойдёт поток электронов от «-« полюса к «+», что равносильно прохождению электрического тока в обратном направлении(по отношению к направлению движения электронов).
Электрохимическая система – совокупность активных веществ и электролита, на основе которых создан аккумулятор.

«+» «-» вещества электролитов; вертикальные линии – электролит.
Между электродами ставят сепараторы. Функции:механическое разделение электродов при узком зазоре; механически удерживают активную массу на электродах, предупреждают её выкрашивание и осыпание.
20. Электрические характеристики химических источников тока.
23. Общие характеристики для всех типов электрохимических систем.
Список: ЭДС, внутреннее сопротивление, напряжение, ёмкость, коэффициенты отдачи по ёмкости и энергии, удельные емкость и энергия, саморазряд.
ЭДС: разность электродных потенциалов при разомкнутой внешней цепи. Каждый тип материала электрода характеризуется потенциалом, появляющемся при попадании его в электролит. Активные вещества электродов – металлы, и проявляющие свойства металлов, опущенные в электролит , становятся заряженными отрицательно. Вещества электродов с окислительными свойствами заряжаются положительно.
Скачок потенциала возникает на границе электрод-электролит, что связано с появлением на этой границе двойного электрического слоя заряженных частиц. Одна группа частиц находится на электроде, а другая (ионная) группа частиц с противоположным зарядом образуется в приэлектродной зоне электролита. В результате, электрически нейтральные до помещения в электролит электроды, становятся заряженными. Процесс образования зарядов на электродах описывается (для кислотных АБ):


Процесс образования зарядов в бортовой свинцовой АБ.
Внутреннее сопротивление аккумулятора: сопротивление, оказываемое аккумулятором проходящему через него постоянному току:
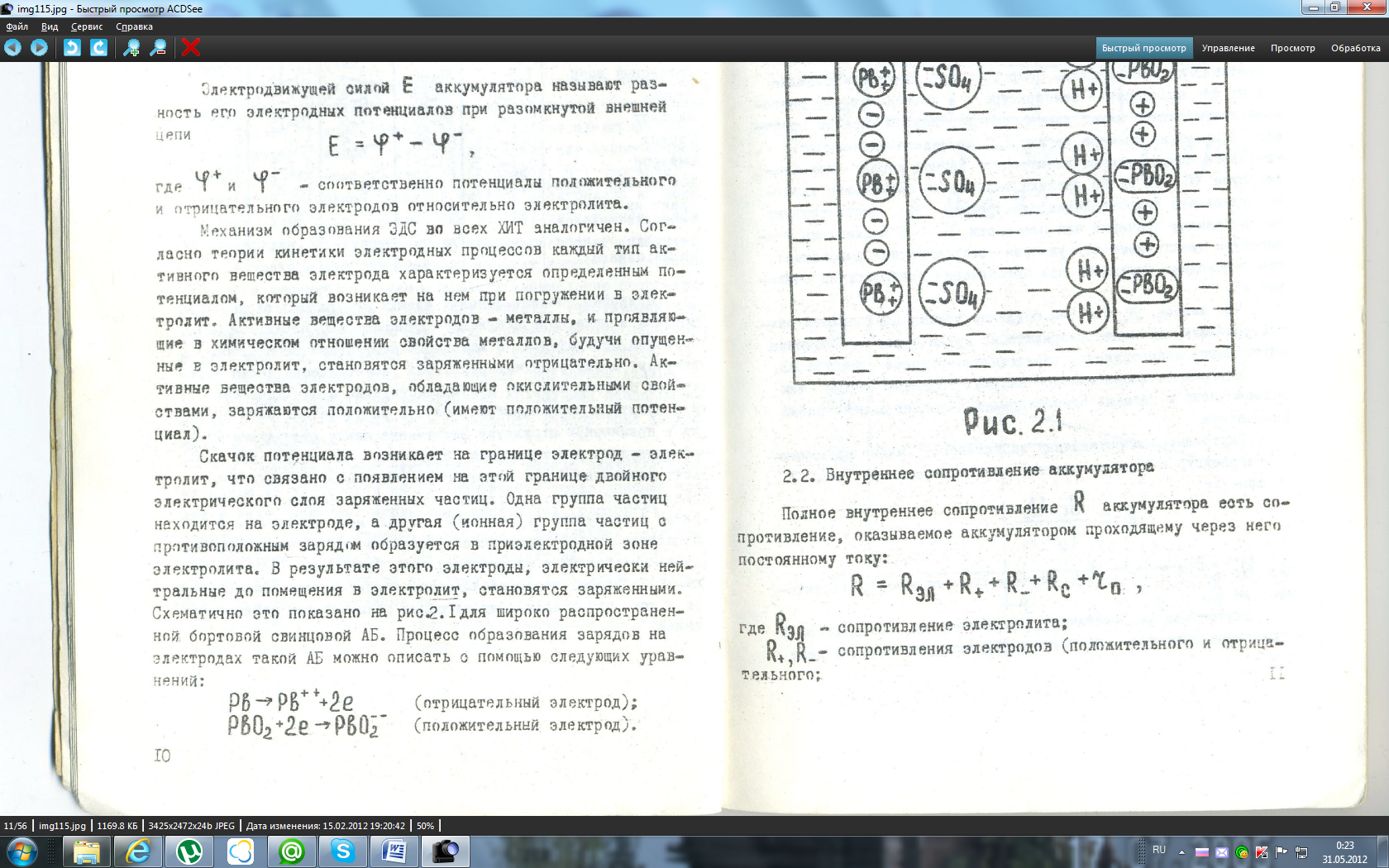
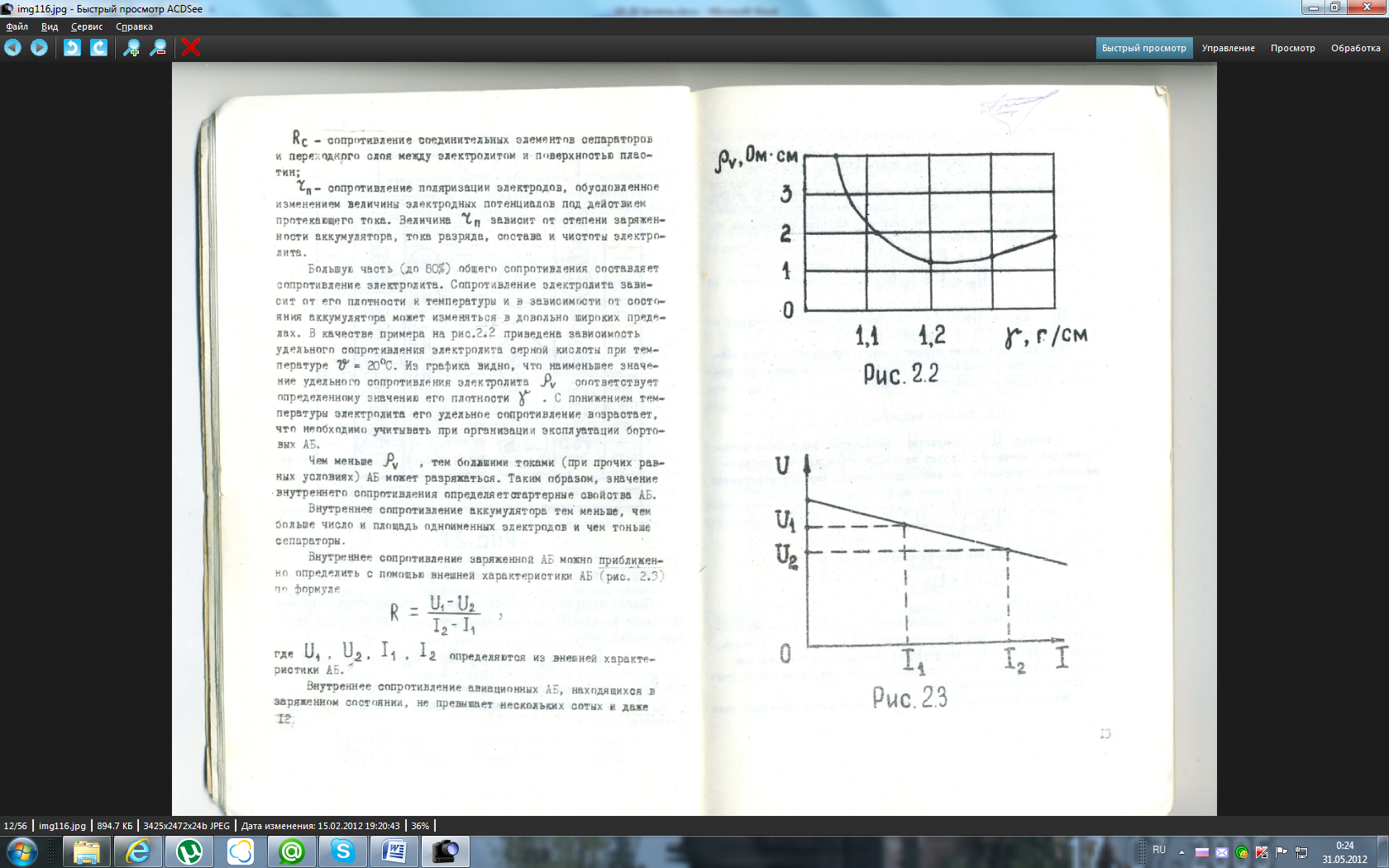
Большая часть общего сопротивления (до 80%) – сопротивление электролита. Сопротивление электролита зависит от его плотности, температуры, состояния аккумулятора. С понижением температуры электролита его удельное сопротивление возрастает. Чем меньше удельное сопротивление электролита, тем большими токами АБ может разряжаться. Значение внутреннего сопротивления определяет стартерные свойства АБ. Внутреннее сопротивление аккумулятора тем выше, чем больше число и площадь одноимённых электродов и чем тоньше сепараторы.
Внутреннее сопротивление зараженной авиационной АБ не превышает 10-х или сотых долей ома.
Напряжение аккумулятора.
Напряжение аккумулятора изменяется при замкнутой внешней цепи. В процессе заряда и разряда аккумулятора напряжение его отличается от ЭДС на величину падения напряжения на внутреннем сопротивлении аккумулятора.

Так как внутреннее сопротивление аккумулятора не является величиной постоянной, то и величина напряжения при заряде и разряде не постоянно.
Ёмкость аккумулятора.
Ёмкостью Q аккумулятора называется колличество электричества, которое он может отдать при разряде его до меньшего допустимого значения; измеряется в ампер-часах, определяется по формуле:
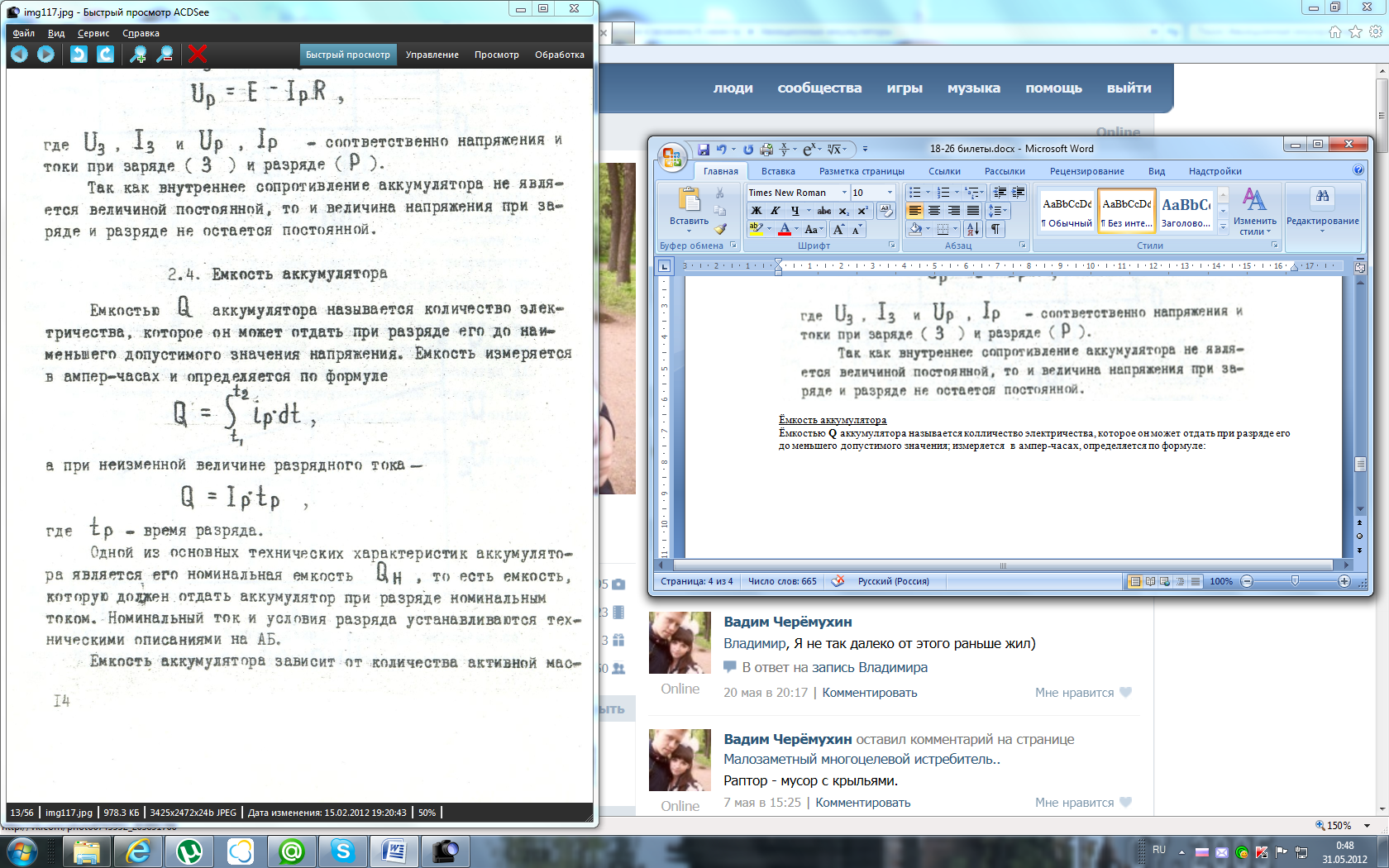
Одна из важных технических характеристик – номинальная ёмкость, ёмкость, которую должен отдать аккумулятор при разряде номинальным током. Номинальный ток и условия разряда устанавливаются техническими описаниями на АБ.
Емкость зависит от количества активной массы, ее пористости, толщины электродов, температуры и плотности электролита.
Чем тоньше электроды при одинаковом количестве активной массы, тем большая часть активного вещества участвует в реакции и тем больше ёмкость аккумулятора. С повышением плотности электролита ёмкость аккумулятора возрастает, но ускоряется саморазряд аккумулятора и нарушение его электродов. При увеличении разрядного тока и понижении температуры электролита разрядная ёмкость понижается.
Коэффициент отдачи аккумулятора по ёмкости и энергии.
Коэффициентом отдачи аккумулятора по ёмкости называется отношение количества электричества, отдаваемого при разряде, к количеству электричества, полученному при заряде.
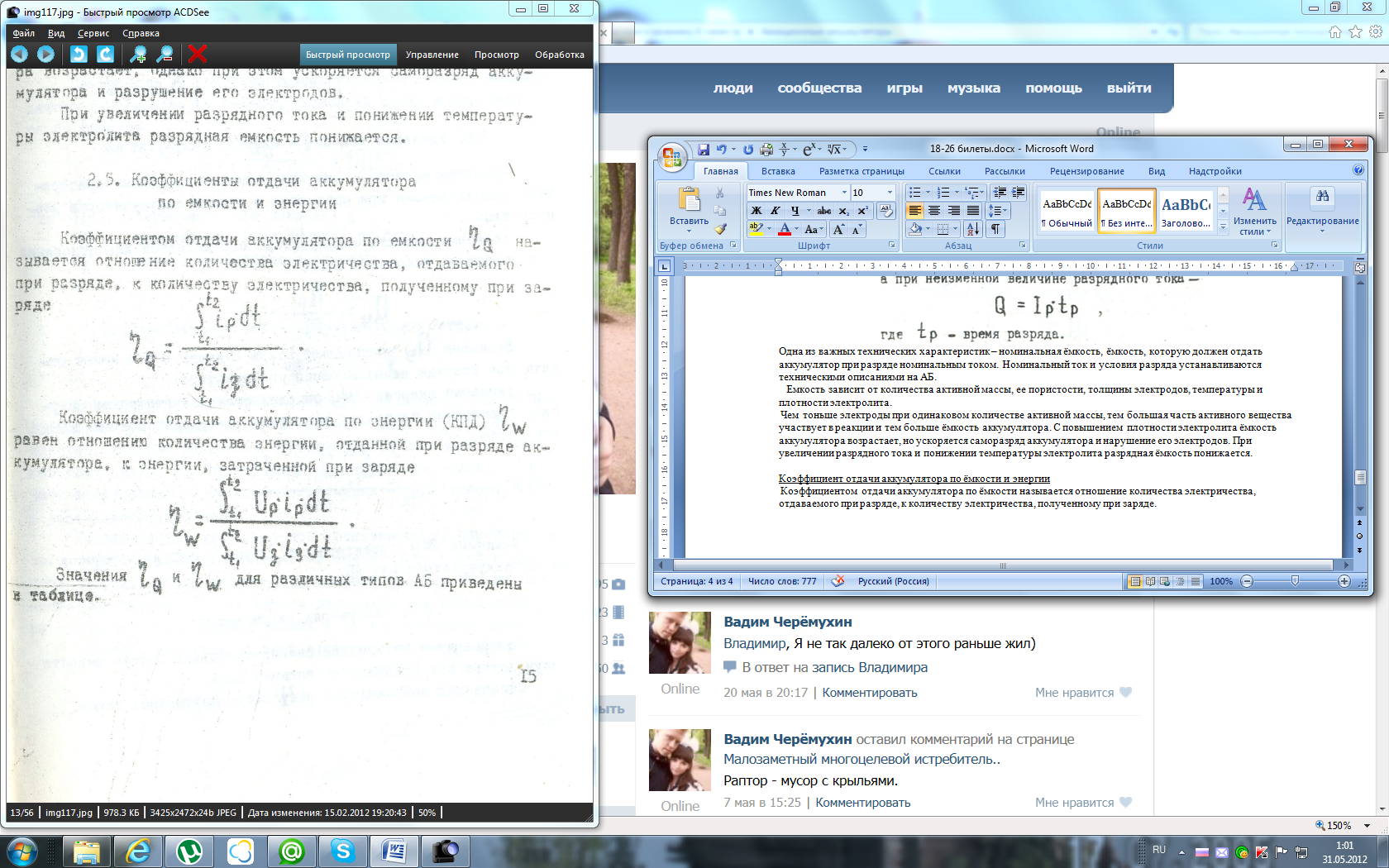
Коэффициент отдачи аккумулятора по энергии (КПД) равен отношению количества энергии , отданной при разряде аккумулятора, к энергии, затраченной при заряде
Удельные ёмкость и энергия аккумулятора
Удельные ёмкость и энергия – основные критерии используемые при сравнении и оценке аккумуляторов разного типа.
Удельная ёмкость определяется как его разрядной ёмкости к массе:
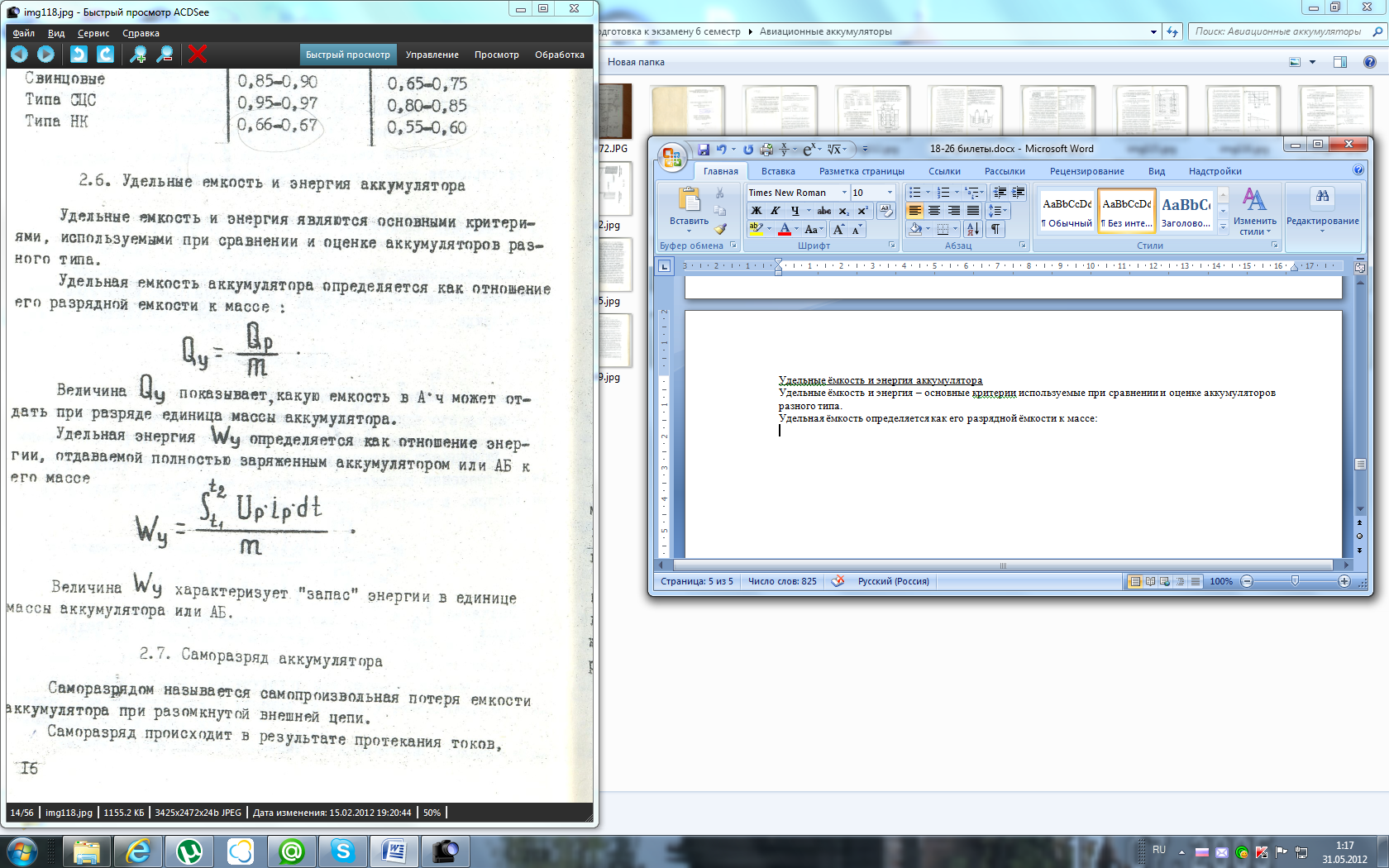
Удельная энергия определяется как отношение энергии, отдаваемой отдаваемой полностью заряженным аккумулятором или АБ его массе:
Саморазряд аккумулятора.
Саморазряд – самопроизвольная потеря ёмкости аккумулятора при разомкнутой внешней цепи. Происходит в результате протекания токов, вызванных разностью потенциалов между активной массой и основанием пластин электродов, между элементами активной массы и примесями в ней, а так же при протекании тока между выводами на поверхности аккумулятора при загрязнении её электролитом или другими веществами. Саморазряд увеличивается с увеличением температуры и особенно сильно при наличии внутренних коротких замыканий. Саморазряд S оценивается уменьшением ёмкости аккумулятора в % от первоначальной за сутки по формуле: