- •1. Назначение и функции, выполняемые ао.
- •2. Классификация ао по видам оборудования.
- •10) Авиационные тренажеры:
- •3. Особенности работы авиационного оборудования.
- •4. Требования, предъявляемые к авиационному оборудованию.
- •5. Дать определение сэс вс и её составляющих.
- •6. Как классифицируется сэс вс.
- •7. Структура сэс вс переменного тока.
- •8. Структура сэс вс постоянного тока.
- •9. Структура первичной сэс вс.
- •10. Структура вторичной сэс вс.
- •11. Что входит в состав срэ вс?
- •12. Перечислить наименования электрических проводов используемых в системах распределения электрической энергии. В чём их отличия.
- •13. Перечислить виды разъёмных устройств используемых в системах распределения электрической энергии.
- •14. Перечислить виды элементов регулирования, защиты и управления сэс ла.
- •15. Назначение элементов регулирования, защиты и управления сэс ла.
- •16. Назначение металлизации и экранирования в срэ ла.
- •17. Назначение и принцип действия статических разрядников.
- •18. Общие сведения, назначение и классификация химических источников тока.
- •19. Основные положения теории электролитической диссоциации. Электролиты.
- •20. Электрические характеристики химических источников тока.
- •23. Общие характеристики для всех типов электрохимических систем.
- •21. Принцип действия кислотных аккумуляторов.
- •22.Пояснить процесс двойной сульфатации.
- •24. Основные технические и электрические характеристики свинцово-кислотных аб.
- •25.Конструкция авиационных кислотных аккумуляторных батарей.
- •26. Пояснить сущность вредной сульфатации электродов.
- •27. Принцип действия серебряно-цинковых аккумуляторов.
- •28.Пояснить процесс дендритообразования.
- •29. Общие характеристики для всех типов электрохимических систем.
- •30. Основные технические и электрические характеристики серебряно-цинковых аб.
- •31. Конструкция авиационных серебряно-цинковых аккумуляторных батарей.
- •32. Назначение, конструкция и принцип действия интегрирующего счётчика ампер-часов (иса).
- •33. Принцип действия авиационных никель-кадмиевых аккумуляторных батарей.
- •34. Конструкция и характеристики авиационных никель-кадмиевых аккумуляторных батарей.
- •35. Меры безопасности при работе с бортовыми аккумуляторными батареями.
- •36. Общие правила эксплуатации авиационных аккумуляторных батарей.
- •20Нкбн-25 (Ni-Cd)
- •37. Особенности эксплуатации авиационных аккумуляторных батарей.
- •38. Установка аккумуляторных батарей на летательный аппарат, основные правила содержания аккумуляторов.
- •39. Устойчивость работы системы регулирования напряжения и способы её повышения.
- •40. Способы уменьшения температурной погрешности регулятора напряжения типа урн.
- •41. Назначение параллельной работы генераторов.
- •42. Защита генераторов постоянного тока от обратного тока.
- •43. Защита генераторов и бортовой сети от перенапряжения.
- •44. Импульсные автоматы защиты питательной сети.
- •45. Требования, предъявляемые к точности стабилизации напряжения в системах электроснабжения летательных аппаратов.
- •46. Методы регулирования напряжения. Принципы построения регуляторов напряжения авиационных генераторов.
- •47. Параллельная работа источников электроэнергии постоянного и переменного токов в авиационных системах электроснабжения.
- •48. Назначение, принцип действия, устройство, работа и особенности эксплуатации урн типа рн - 180, рн - 600, рн - 120у.
- •49. Назначение, принцип действия, устройство и особенности эксплуатации дифференциально-минимального реле дмр-600т.
- •50. Назначение, классификация и основные электрические характеристики авиационных генераторов.
- •51. Принцип действия и конструктивные особенности авиационных генераторов.
- •52. Основные типы генераторов постоянного тока и их конструктивные особенности.
- •53. Электрические и эксплуатационные характеристики генераторов постоянного тока.
- •54. Основные типы генераторов переменного тока и их конструктивные особенности.
- •55. Электрические и эксплуатационные характеристики генераторов переменного тока.
- •57. Охлаждение авиационных генераторов.
- •58. Правила технической эксплуатации генераторов постоянного тока типа стг, гс.
- •60. Правила технической эксплуатации генераторов переменного тока типа го.
- •63. Назовите аварийные режимы при эксплуатации электроэнергетических систем вс.
- •64. Назначение питательной сети вс.
- •65. Что понимается под основной сетью?
- •66. Что понимается под аварийной сетью?
- •67. Поясните работу схемы питательной сети самолёта-истребителя.
- •68. Требования, предъявляемые к аппаратуре защиты энергосистем летательных аппаратов.
- •69. На какие группы делится коммутационная аппаратура в зависимости от способа управления?
- •70. Пояснить принцип действия реле и контакторов.
- •71. Пояснить принцип работы коробки переключающих реле кпр-9.
- •72. Типы плавких предохранителей применяемых на вс.
- •73. Принцип действия плавких предохранителей.
- •74. Типы автоматов защиты и их принцип действия.
- •75. Назначение и типы дмр.
- •76. Защита генераторов и их фидеров от коротких замыканий.
- •77. Типы биметаллических автоматов защиты.
- •78. Типы плавких предохранителей.
- •79. Работа коробки коч-62б 2 серии.
- •80. Работа автомата азп-8м 4 серии.
- •81. Работа автомата азп-8м 5 серии.
- •82. Принцип действия защиты при несимметрии нагрузки.
- •83. Принцип действия датчика направления тока днт-1.
- •84. Типы автоматов защиты и их принцип действия.
- •85. Характерные отказы аппаратуры защиты и управления и методы их предупреждения.
- •86. Требования предъявляемые к системам распределения электроэнергии вс.
- •87. Состав срэ и классификация по способу распределения электроэнергии.
- •88. Классификация по электрическим параметрам систем распределения электроэнергии и по конфигурации систем распределения электроэнергии.
- •89. Классификация по системе распределения электроэнергии.
- •90. Назначение и состав системы распределения эл. Энергии самолёта Ан-26.
- •91. Назначение и состав системы распределения эл. Энергии вертолёта Ми-8.
- •1.1. Система генерирования
- •92. Типы бортовых эл. Проводов. 93. Классификация электрических проводов.
- •94. Меры безопасности при работе с системами электроснабжения летательных аппаратов.
- •95. Характерные отказы электрических сетей ла и методы их предупреждения.
26. Пояснить сущность вредной сульфатации электродов.
Вредная сульфатация пластин:
Возникает в результате перехода мелкокристаллического сульфата свинца, получавшегося при разряде в крупнокристаллический,который при последующих зарядах АБ растворяется крайне плохо, и поэтому активная масса пластин восстанавливается не полностью.
Причинами появления вредной сульфатации являются:
- хранение батарей в разряженном или полуразряженном состоянии;
- систематические недозаряды и глубокие разряды;
- несистематическое проведение глубоких зарядов и КТЦ;
- пониженный уровень и повышенная плотность электролита.
Признаки вредной сульфатации:
- повышенное напряжение в начале заряда и пониженное в конце заряда;
- медленное повышение плотности электролита при заряде;
- быстрое повышение температуры электролита при заряде;
- преждевременное начало газовыделения при заряде из-за гидролиза воды, вызванного повышенным напряжением на аккумуляторе;
- резкое падение напряжения, пониженная емкость при разряде;
Сульфатация акумулятора устраняется проведением процесса десульфатации:
- вылить электролит;
- залить дистиллированную воду;
- залить новый электролит;
- заряд током второй ступени.
Если плотность электролита будет повышаться, то данные меры достигли цели.
27. Принцип действия серебряно-цинковых аккумуляторов.
Конструктивно серебряно-цинковые аккумуляторы выполнены в виде набора положительных и отрицательных электродных пластин, которые разделены сепараторами, и помещены в пластмассовый сосуд. Для приведения в действие аккумуляторы заливают электролитом - раствором химически чистой щелочи КОН в дистиллированной воде.
Положительные электроды изготавливаются из порошкообразного серебра, а отрицательные—из смеси окиси цинка и цинкового порошка. В результате формирования (заряда АБ) на положительных электродах образуется двухвалентная окись серебра AgO, а на отрицательных - чистый рубчатый цинк Zn.
Электрохимическая система аккумулятора имеет вид:
AgO|KOH|Zn
Плотность электролита равна 1.47 г/см3. В ходе токообразующей реакций электролит выполняет роль переносчика ионов.
Процесс разряда и заряда серебряно-цинкового аккумулятора происходит в две ступени:
1) 2AgO + KOH +Zn Ag2 + KOH +ZnO
AgO = 0,62 В; Zn = -1,24 В; Eак = 0,62 + 1,24 = 1,86 В.
2) Ag2O + KOH +Zn 2Ag + KOH +ZnO
AgO = 0,31 В; Zn = -1,24 В; Eак = 0,31 + 1,24 = 1,55 В.
При разряде на положительном электроде протекает реакция восстановления серебра, а на отрицательном - окисления цинка.
При заряде токообразующие реакции идут в обратном ( по отношению к заряду ) порядке.
Суммарная токообразующая реакция имеет вид
2AgO + KOH +Zn Ag + KOH +ZnO
При разряде уровень электролита понижается зачет уменьшения объема активных веществ при их химических превращениях, при заряде - повышается.
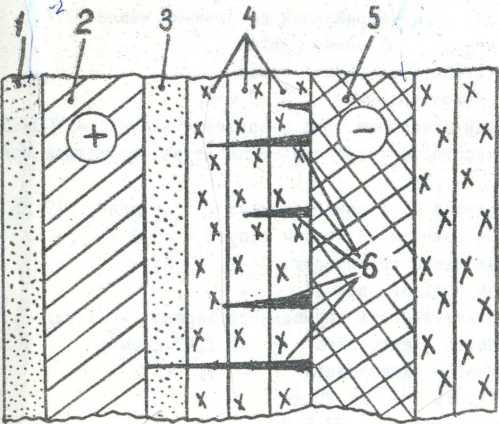
28.Пояснить процесс дендритообразования.
Серебряно-цинковые аккумуляторы особенно чувствительны к перезаряду, во время которого в пленке прорастают дендриты цинка (игольчатые кристаллы 6), способные протыкать пленку, капрон и вызывать короткие замыкания разноименных электродов. Объясняется это тем, что при перезаряде восстановление окиси цинка до металлического Zn в порах активной массы отрицательных электродов 5 уже закончилось (весь Zn там восстановлен). Поэтому начинается восстановление его из раствора электролита, а последний почти весь находится в порах пленки 4. Это сопровождается выделением цинка на электроде 5 в виде дендритов - игл 6, прокалывающих сепарацию. Рост дендритов цинка в пленке направлен в сторону положительного электрода 2 и в конце концов приводит к электрическому соединению электродов 2 и 5 через дендриты 6, то есть к их короткому замыканию. Цинковые дендриты не вступают в обратимые реакции.