
- •Билет №1
- •Вопрос 1: Показатель политропы в изотермическом, изобарном, изохорном, адиабатном и политропных процессах.
- •Показатель политропы:
- •Вопрос 2: Законы гидрогазодинамики. Физические свойства жидкостей (газов).
- •Билет №2
- •Вопрос 1: Дифференциальное уравнение равновесия Эйлера (вывод). Основное уравнение гидростатики. Дифференциальные уравнения равновесия Эйлера
- •После преобразования находим:
- •Таким образом, условия равновесия элементарного параллелепипеда выражаются системой уравнений:
- •Основное уравнение гидростатики
- •Вопрос 2: Уравнения теплоемкостей в изотермическом, изобарном, изохорном, адиабатном и политропных процессах.
- •43.Уравнения изменений энтальпии в изотермическом, изобарном, изохорном, адиабатном и политропных процессах.
- •3.Основные характеристики движения жидкости. Гидравлический радиус и эквивалентный диаметр.
- •4.Дифференциальное уравнение для установившегося и неустановившегося потока.
- •42.Уравнения изменений внутренней энергии в изотермическом, изобарном, изохорном, адиабатном и политропных процессах.
- •5.Режимы движения жидкостей и расход жидкости при ламинарном движении потока.
- •41.Уравнения количества теплоты, сообщаемое в адиабатном и политропном процессах.
- •6.Дифференциальное уравнение неразрывности потока. Практическое приложение.
- •Вопрос 2
- •Работа при адиабатическом процессе
- •Расчёт теплоты и работы политропных процессов сжатия газов
- •Вопрос 7
- •7. Дифференциальное уравнение движения идеальной жидкости (уравнение эйлера).
- •Вопрос 2
- •9.Вывод уравнения Бернулли. Практическое применение.
- •9.Вывод уравнения Бернулли. Практическое применение.
- •Вопрос 2
- •10.Теория подобия – метод научного обобщения экспериментов.
- •Вопрос 2
- •11. Условия и теория подобия.
- •Вопрос 2
- •36.Простейшие термодинамические процессы идеальных газов.
- •4Адиабатный процесс
- •5. Политропный процесс
- •Вопрос 13
- •12. Первая теорема подобия. Преобразование дифференциального уравнения в критериальное. Подобие начальных и граничных условий
- •Вопрос 2
- •35.Параметр состояния термодинамической системы – энтропия. Вывод.
- •13. Вторая теорема подобия. Пример использования.
- •Вопрос 2
- •34. Второй закон термодинамики. Основные постулаты, вытекающие изз второго закона термодинамики.
- •14. Третья теорема подобия. Раскрыть ее сущность.
- •Вопрос 2
- •33.Уравнение Майера.
- •Вопрос 16
- •15. Преобразование дифференциального уравнения Навье-Стокса в критериальное. Гидравлическое подобие
- •Для установившегося потока
- •Вопрос 2
- •32.Первый закон термодинамики. Раскрыть сущность.
- •16. Модифицированные и производные критерии подобия
- •Вопрос 2
- •30.Работа и теплота
- •28. Внутренняя энергия системы. Внутренняя энергия идеального газа.
- •29. Энтальпия идеального газа.
- •19. Гидравлическое сопротивление при движении жидкостей (газов) в трубах и каналах.
- •26. Смеси идеальных газов. Массовая и молярная концентрация. Парциальное давление. Закон Дальтона.
- •21. Сопротивление при свободном движении тел в газах и жидкостях
- •22. Осаждение частиц под действием сил тяжести и инерции. Примеры применения.
- •Основные понятия о науке газодинамике
Вопрос 2
35.Параметр состояния термодинамической системы – энтропия. Вывод.
Пользуясь первым законом термодинамики, уравнением теплоемкости можно исследовать основные термодинамические процесс рабочего тела, которым является идеальный газ.
Предварительно нужно ввести понятие о параметре состояния термодинамической системы:
- Энтропия – (S-T диаграмма)
Dq=dU+pdV=dU+dA
В уравнение dq не является полным дифференциалом, поскольку в правую часть уравнения входит dA, т.к. А не является параметром состояния газа, а следовательно и функции.
Поэтому нельзя проинтегрировать это уравнение.
Из математики известно, что всякий трехчлен можно представить в виде полного дифференциала, если его умножить на интегрирующий множитель.
dq/T=dU/T+pdV/T=dU/T+dA/T
dq/T=S=dU/T+pdV/T=dM/T-VdP/T (*)
dM=CpdT, dU=CvdT
Уравнение (*) можно преобразовать учитывая dM и dU: PV=RT*PdV/T=RdP/P.
dq/T=S= CvdT/T+R*dV/V(изохорный)= CpdT/T-R*dP/P(изобарный) (1)
S=CvlnT+RlnV+const=CplnT- RlnP+const. (2)
Таким образом изменение энтропии ΔS=S2-S1= CvlnT2/T1+R*lnV2/V1+const= CplnT2/T1-R*lnP2/P1+const.
Если представить диаграмму S-T анализируя ур-я (1 и 2), можно заключить, что
dq=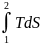 (3)
(3)
Интеграл (3) можно решить, если известна функциональная зависимость Т и S, пользуясь этой зависимостью строят кривые. Площадь под кривыми отображает кол-во тепла привносимого и отводимого в данном процессе.
Под интегральная функция – количество отведенной и привнесенной теплоты.
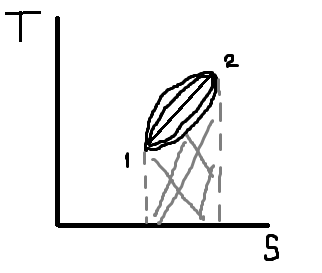 (то
что серым это под интегральная функция)
(то
что серым это под интегральная функция)
Билет 14
13. Вторая теорема подобия. Пример использования.
Вторая теорема подобия. Решение любого дифференциального уравнения, связывающего между собой переменные, влияющие на процесс, может быть представлено в виде зависимости между безразмерными комплексами этих величин, т.е. между критериями подобия.
Если обозначить критерии подобия через 1,2,3,…n то решение дифференциального уравнения может быть представлено в общем виде:
f (1,2,3,…n) = 0. (2.77)
Такие уравнения называют уравнениями обобщенных переменных (обобщёнными) или критериальными уравнениями.
Критерии подобия, которые составлены из величин, входящих в условия однозначности, называются определяющими.
Критерии же, включающие такие величины, которые не являются необходимыми для однозначной характеристики данного процесса, а сами зависят от этих условий, называют определяемыми. Какой из критериев является определяемым, зависит от формулировки задачи. Например, в случае движения жидкости по трубе определяемым является P, т.е. если определяемым является некоторый критерий 1 , то уравнение (2.77) удобнее представить в виде:
1 = f (2,3,…n). (2.78)
Вторая теорема отвечает на вопрос, как обрабатывать результаты опытов, проведенных на моделях: их надо представлять в виде функциональной зависимости между критериями подобия.
Вопрос 2
34. Второй закон термодинамики. Основные постулаты, вытекающие изз второго закона термодинамики.
Представляет собой обобщенный ряд положений вытекающих из наблюдений ОС и анализа закона термодинамики:
Самопроизвольное протекание естественных процессов возникает и развивается при отсутствии равновесия между участвующих в процессе термодинамических систем и ОС.
Самопроизвольно происходящие в природе естественные процессы, работа которых может быть использована человеком всегда протекает лишь в одном направлении от более высокого к более низкому потенциалу.
Ход самопроизвольно протекающих процессов происходит в направление приводящем к установленному равновесию термодинамической системы и ОС, и по достижению этого равновесия процессы прекращаются.
Процесс может протекать в направлении обратном самопроизвольному процессу, если энергия задействована с внешней среды.
Эти формулировки вылились в форму постулатов (Карио, Лазиус, Томсон):
1.Тепло не может переходить от холода к теплу без конденсации.
2.Невозможно осуществлять цикл теплового двигателя без переноса некоторого количества тепла от источника тепла с более высокой t к источнику с более низкой t.
15 билет
