
- •Билет №1
- •Вопрос 1: Показатель политропы в изотермическом, изобарном, изохорном, адиабатном и политропных процессах.
- •Показатель политропы:
- •Вопрос 2: Законы гидрогазодинамики. Физические свойства жидкостей (газов).
- •Билет №2
- •Вопрос 1: Дифференциальное уравнение равновесия Эйлера (вывод). Основное уравнение гидростатики. Дифференциальные уравнения равновесия Эйлера
- •После преобразования находим:
- •Таким образом, условия равновесия элементарного параллелепипеда выражаются системой уравнений:
- •Основное уравнение гидростатики
- •Вопрос 2: Уравнения теплоемкостей в изотермическом, изобарном, изохорном, адиабатном и политропных процессах.
- •43.Уравнения изменений энтальпии в изотермическом, изобарном, изохорном, адиабатном и политропных процессах.
- •3.Основные характеристики движения жидкости. Гидравлический радиус и эквивалентный диаметр.
- •4.Дифференциальное уравнение для установившегося и неустановившегося потока.
- •42.Уравнения изменений внутренней энергии в изотермическом, изобарном, изохорном, адиабатном и политропных процессах.
- •5.Режимы движения жидкостей и расход жидкости при ламинарном движении потока.
- •41.Уравнения количества теплоты, сообщаемое в адиабатном и политропном процессах.
- •6.Дифференциальное уравнение неразрывности потока. Практическое приложение.
- •Вопрос 2
- •Работа при адиабатическом процессе
- •Расчёт теплоты и работы политропных процессов сжатия газов
- •Вопрос 7
- •7. Дифференциальное уравнение движения идеальной жидкости (уравнение эйлера).
- •Вопрос 2
- •9.Вывод уравнения Бернулли. Практическое применение.
- •9.Вывод уравнения Бернулли. Практическое применение.
- •Вопрос 2
- •10.Теория подобия – метод научного обобщения экспериментов.
- •Вопрос 2
- •11. Условия и теория подобия.
- •Вопрос 2
- •36.Простейшие термодинамические процессы идеальных газов.
- •4Адиабатный процесс
- •5. Политропный процесс
- •Вопрос 13
- •12. Первая теорема подобия. Преобразование дифференциального уравнения в критериальное. Подобие начальных и граничных условий
- •Вопрос 2
- •35.Параметр состояния термодинамической системы – энтропия. Вывод.
- •13. Вторая теорема подобия. Пример использования.
- •Вопрос 2
- •34. Второй закон термодинамики. Основные постулаты, вытекающие изз второго закона термодинамики.
- •14. Третья теорема подобия. Раскрыть ее сущность.
- •Вопрос 2
- •33.Уравнение Майера.
- •Вопрос 16
- •15. Преобразование дифференциального уравнения Навье-Стокса в критериальное. Гидравлическое подобие
- •Для установившегося потока
- •Вопрос 2
- •32.Первый закон термодинамики. Раскрыть сущность.
- •16. Модифицированные и производные критерии подобия
- •Вопрос 2
- •30.Работа и теплота
- •28. Внутренняя энергия системы. Внутренняя энергия идеального газа.
- •29. Энтальпия идеального газа.
- •19. Гидравлическое сопротивление при движении жидкостей (газов) в трубах и каналах.
- •26. Смеси идеальных газов. Массовая и молярная концентрация. Парциальное давление. Закон Дальтона.
- •21. Сопротивление при свободном движении тел в газах и жидкостях
- •22. Осаждение частиц под действием сил тяжести и инерции. Примеры применения.
- •Основные понятия о науке газодинамике
Билет №1
Вопрос 1: Показатель политропы в изотермическом, изобарном, изохорном, адиабатном и политропных процессах.
Изотермические, изобарные, изохорные, адиабатные и политропные процессы – это частные случаи политропного процесса.
Политропный процесс – это процесс в кот при подводе и приводе теплоты удельная теплоемкость не изменяется.
Рассмотрим на диаграммах эти процессы:
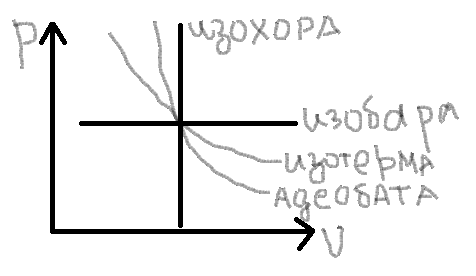
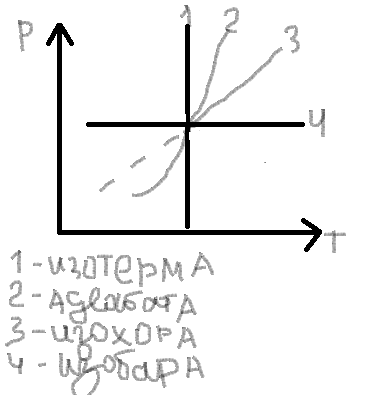

В
соответствии с сущностью понятия
теплоёмкости ![]() ,
предельными частными явлениями
политропного процесса являются изотермический
процесс (
,
предельными частными явлениями
политропного процесса являются изотермический
процесс (![]() )
и адиабатный
процесс (
)
и адиабатный
процесс (![]() ).
).
В случае идеального газа, изобарный процесс и изохорный процесс также являются политропными.
Показатель политропы:
Кривая на термодинамических диаграммах, изображающая политропный процесс, называется «политропа». Для идеального газа уравнение политропы может быть записано в виде:
![]()
где р — давление, V — объем газа, n — «показатель политропы».
![]() .
Здесь
.
Здесь ![]() —
теплоёмкость газа в данном процессе,
—
теплоёмкость газа в данном процессе, ![]() и
и ![]() —
теплоемкости того же газа, соответственно,
при постоянном давлении и объеме.
—
теплоемкости того же газа, соответственно,
при постоянном давлении и объеме.
В зависимости от вида процесса, можно определить значение n:
Изотермический процесс:
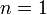 ,
так как
,
так как 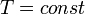 ,
значит, по закону
Бойля — Мариотта
,
значит, по закону
Бойля — Мариотта 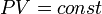 ,
и уравнение политропы вынуждено
выглядеть так:
,
и уравнение политропы вынуждено
выглядеть так: 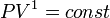 .
.
Изобарный процесс:
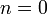 ,
так как
,
так как 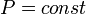 ,
и уравнение политропы вынуждено
выглядеть так:
,
и уравнение политропы вынуждено
выглядеть так: 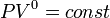 .
.
Адиабатный процесс:
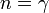 (здесь
(здесь 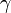 — показатель
адиабаты),
это следует из уравнения
Пуассона.
— показатель
адиабаты),
это следует из уравнения
Пуассона.
Изохорный процесс:
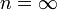 ,
так как
,
так как 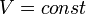 ,
и в процессе
,
и в процессе 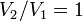 ,
а из уравнения политропы следует, что
,
а из уравнения политропы следует, что 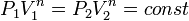 ,
то есть, что
,
то есть, что 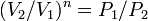 ,
то есть
,
то есть 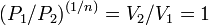 ,
а это возможно, только если
,
а это возможно, только если 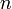 является
бесконечным.
является
бесконечным.
Вопрос 2: Законы гидрогазодинамики. Физические свойства жидкостей (газов).
Гидрогазодинамика – наука о движении воды или воздушных масс в системах.
Многие процессы, протекающие в аппаратах, применяемых для очистки газов и воды, связаны с их движением, перемешиванием в рабочих средах, а также с разделением неоднородных смесей путем осаждения, фильтрования и центрифугирования. Скорость всех указанных физических процессов определяется законами гидро- и газомеханики.
Законы гидромеханики и их практические приложения изучаются в гидравлике, которая состоит из двух разделов: гидростатики и гидродинамики. Гидростатика рассматривает законы равновесия в состоянии покоя, а гидродинамика - законы движения жидкостей и газов.
В гидравлике принято объединять жидкости, газы и пары под единым наименованием – жидкости. Жидкость рассматривается как сплошная однородная среда.
При выводе основных закономерностей в гидравлике вводят понятие о гипотетической идеальной жидкости, которая, в отличие от реальной (вязкой) жидкости абсолютно несжимаема под действием давления, не изменяет плотности при изменении температуры и не обладает вязкостью.
Реальные жидкости делятся на капельные и упругие (газы или пары).
Капельные жидкости практически несжимаемы и обладают лишь малым коэффициентом объемного расширения.
Объем упругих жидкостей сильно изменяется при изменении температуры или давления.
Некоторые физические свойства жидкостей (газов):
Плотность. Масса единицы объема жидкости называется плотностью и обозначается через :
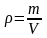 (кг/м3).
(2.6)
(кг/м3).
(2.6)
Плотность капельных жидкостей (газов) сравнительно мало изменяются под действием давления или при изменении температуры.
Плотность газа может быть рассчитана на основе уравнения состояния для идеальных газов:
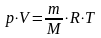 ,
(2.7)
,
(2.7)
где Р – давление, Н/м2;
Т – температура, К;
М - масса 1 кмоль газа, кг/кмоль;
R - универсальная газовая постоянная, которая равна 8314 Дж/(кмольград).
Из уравнения (2.7) получаем:
pVM=mRT
или
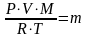 ;
;
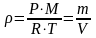 .
.
Объем, занимаемый единицей массы газа, или величина, обратная плотности, называется удельным объемом и обозначается через :
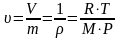 .
.
Давление. В отличие от твердых тел частицы жидкости обладают большой подвижностью и при воздействии силы перемещаются. Жидкость будет находиться в равновесии, если действующие силы распределены по поверхности и направлены перпендикулярно к ней.
На любую поверхность твердых тел граничащая с ней жидкость воздействует с некоторой силой давления, направленной всегда перпендикулярно к этой поверхности. Силы давления появляются при изменении объема жидкости или при ее сжатии.
Давление определяется по формуле:
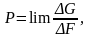
при
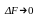
где
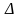 G,
F
– изменение силы и площади соответственно.
G,
F
– изменение силы и площади соответственно.
Приборы для измерения давления (манометры или вакуумметры) показывают не абсолютные давления Рабс внутри замкнутого объема, а разность между абсолютным и атмосферным или барометрическим давлением Ратм.
Эту разность называют избыточным давлением Ризб, если давление в объеме превышает атмосферное, и разрежением Рвак, если оно ниже атмосферного. Таким образом,
Рабс = Ризб + Ратм; Рабс = Ратм - Рвак .
Вязкость. Свойство жидкости оказывать сопротивление усилиям, вызывающим перемещение ее частиц, называется вязкостью.
На
рисунке 2.1 изображены два параллельных
слоя площадью F
каждый, причем расположенный выше слой
движется со скоростью (+d),
большей, чем скорость расположенного
ниже слоя, на бесконечно малую величину
d.
Опыт показывает, что касательная сила
G,
которую надо приложить для сдвига, тем
больше, чем больше градиент
скорости
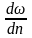 ,
характеризующий изменение скорости,
приходящееся на единицу расстояния по
нормали между слоями.
,
характеризующий изменение скорости,
приходящееся на единицу расстояния по
нормали между слоями.
Кроме того, сила G пропорциональна площади соприкосновения слоев.
Следовательно,
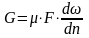 ,
(2.8)
,
(2.8)
где – коэффициент пропорциональности.
Возникающая внутри жидкости сила сопротивления равна приложенной силе G и направлена в противоположную сторону. Отношение этой силы к поверхности соприкосновения слоев обозначают через и называют напряжением внутреннего трения, а также напряжением сдвига или касательным напряжением.
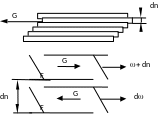


Рисунок 2.1- К характеристике вязкости
Соответственно, уравнение (2.8) примет вид:
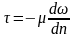 .
(2.9)
.
(2.9)
Коэффициент пропорциональности в уравнении (2.8) или (2.9) называют динамическим коэффициентом вязкости.
Динамическая вязкость в СИ выражается:
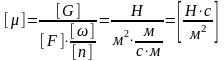 .
.
Иногда вязкость жидкостей характеризуют кинематическим коэффициентом вязкости или кинематической вязкостью:
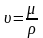
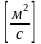 . (2.10)
. (2.10)
Вязкость капельных жидкостей значительно снижается с возрастанием температуры. Вязкость газов, наоборот, увеличивается с ее повышением.
Поверхностное натяжение. В ряде процессов в оборудовании для очистки газов капельная жидкость при движении соприкасается с газом (или паром) или с другой капельной жидкостью, практически не смешивающейся с первой. Поверхность раздела между фазами стремится к минимуму под
действием поверхностных сил. Следовательно, капли, взвешенные в газе (паре) или в другой жидкости, и пузырьки газа в жидкости принимают форму, более или менее близкую к шарообразной. Это объясняется тем, что молекулы жидкости внутри ее объема испытывают примерно одинаковое воздействие соседних молекул, в то время как молекулы, находящиеся непосредственно у поверхности раздела фаз, притягиваются молекулами внутренних слоев жидкости сильнее, чем молекулами окружающей среды. В результате на поверхности жидкости
возникает давление, направленное внутрь жидкости по нормали к ее поверхности, которое и стремится уменьшить эту поверхность до минимальной величины. Следовательно, для создания таких новых поверхностей необходима некоторая затрата энергии. Работу, требуемую для образования единицы новой поверхности называют межфазной, или поверхностным натяжением и обозначают через .
Поверхностное натяжение выражается в следующих единицах:
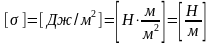 .
.
Из приведенных выражений для следует, что поверхностное натяжение можно рассматривать также как силу, действующую на единицу длины поверхности раздела жидкости и соприкасающейся с ней среды.
Поверхностное натяжение уменьшается с увеличением t. С величиной связаны характеристики смачивания капельными жидкостями твердых материалов; смачивание оказывает существенное влияние на гидродинамические условия протекания процессов в абсорбционных аппаратах.
