
- •Лекция 1: 9.09.2015
- •Требования, предъявляемые к катодным осадкам в гальванотехнике и гидроэлектрометаллургии. 2
- •Механизм электрокристаллизации металлов
- •Лекция 3: 23.09.2015
- •Влияние природы осаждаемого Ме на величину кристаллов и Ме-п
- •Влияние режима электролиза на структуру металлических покрытий/осадков
- •Влияние состава электролита на структуру гальванических осадков
- •Лекция 4: 30.09.2015
- •Условия получения компактных поликристаллических осадков
- •Влияние различных факторов на рс электролита
- •Методы измерения рассеивающей способности
- •Анодные процессы гальванотехники. Выбор материала, вида и площади поверхности анода
- •Обезжиривание
- •Химическое обезжиривание
- •Электрохимическое обезжиривание
- •Промывочные операции
- •Электрополировка поверхностей Ме
- •Цинкование
- •Сульфатные электролиты цинкования
- •Лекция 10: 18.11.2015
- •Хлористоаммонийные и аммиакатные электролиты цинкования
- •Заключительные операции при цинковании
- •Сульфатные электролиты никелирования
- •Блестящее никелирование
- •Перспективные электролиты никелирования
- •Многослойное никелирование
- •1)Би-никель (двухслойное никелирование).
- •Хромирование. Целевое назначение. Электролиты и их сравнительная характеристика
- •Хромирование из сульфатного электролита
- •Усовершенствование процессов хромирования
- •Интенсификация процесса хромирования
- •Физико – химические свойства Cr-п
- •Механизм процесса анодирования
- •Заключительные операции при анодировании
- •Особые случаи анодирования
- •Электроосаждение сплавов
- •Лекция 15: 23.12.2015
- •Электроосаждение Ме-п в насыпном виде
- •1)Наливной колокол
- •2)Погружные вращающиеся барабаны. Они погружаются в гальваническую ванну, аноды с 2-х сторон вдоль граней барабана, он вращается и идет покрытие.
- •Осаждение Ме-п на реверсивном токе
Влияние природы осаждаемого Ме на величину кристаллов и Ме-п
В электрохимии природу Me определяет величина тока обмена, которая устанавливается на границе электрод – раствор и показывает скорость обмена ионов между кристаллической решеткой (где эти ионы превращаются в атомы) и раствором (где атомы превращаются в ионы). Величина тока обмена определяет трудность смещения электродного Ɛ от равновесия под действием электрического тока. Это смещение – поляризация. Чем больше ток обмена, тем труднее внешним током сместить Ɛ от равновесия, следовательно, величина тока обмена определяет величину поляризации, вероятность образования кристаллических зародышей и мелкокристалличность Ме-П. По величине тока обмена Ме-П можно разделить на 3 группы:
1.)Металлы с высоким током обмена (j0): Ag, Pb, Tl, Sb, Cd.
j0=10-3÷10-2 А/см2. Поляризация исходя из тока обмена невысокая: η=10-50 мВ. Размеры кристаллов большие: a=10-2÷10-3 см – параметры кристаллической решетки.
Компактные покрытия таких Me можно получить лишь при наличии ПАВ и комплексных электролитов. В обычных условиях покрытия получаются шероховатыми, порошкообразными, нитевидными.
2.)Металлы, у которых ток обмена несколько ниже: Cu, Zn, Bi.
j0=10-5÷10-4 А/см2, η=30-100 мВ, а=10-5÷10-4 см.
Компактные покрытия здесь можно получить из обычных электролитов, но для получения качественных, равномерных и плотноупакованных покрытий вводят ПАВ и комплексные электролиты, т.е. те вещества, которые дополнительно увеличивают электродную поляризацию.
3.)Металлы группы железа: Fe, Ni, Co.
j0=10-9÷10-8 А/см2, η=100-600 мВ, а=10-8÷10-7 см.
Для
этих Me,
благодаря высокой поляризации, часто
не требуется вводить для обеспечения
мелкокристалличности доп.вещества.
Сам катодный процесс идет с высокой,
почти максимальной
 и осадки покрытия мелкокристаллические,
плотноупакованные и полублестящие.
Причина высокой
и осадки покрытия мелкокристаллические,
плотноупакованные и полублестящие.
Причина высокой
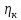 в
том, что данные Me обладают высокой
адсорбционной способностью и в момент
электроосаждения адсорбируют на себе
чужеродные вещества из электролита,
гидроксиды, продукты полуреакций. В
результате образуется адсорбционная
пленка, через которую очень тяжело идет
разряд ионов Ме, т.е. затрудняется стадия
переноса электронов. По другой теории,
высокую поляризацию объясняют тем, что
ионы таких Me
сильно гидратированы, энергия гидратации
велика, и чтобы разорвать гидратную
оболочку требуется значительная внешняя
энергия, которую дает электродная
поляризация.
в
том, что данные Me обладают высокой
адсорбционной способностью и в момент
электроосаждения адсорбируют на себе
чужеродные вещества из электролита,
гидроксиды, продукты полуреакций. В
результате образуется адсорбционная
пленка, через которую очень тяжело идет
разряд ионов Ме, т.е. затрудняется стадия
переноса электронов. По другой теории,
высокую поляризацию объясняют тем, что
ионы таких Me
сильно гидратированы, энергия гидратации
велика, и чтобы разорвать гидратную
оболочку требуется значительная внешняя
энергия, которую дает электродная
поляризация.
Влияние режима электролиза на структуру металлических покрытий/осадков
1.)Влияние плотности тока: чем больше плотность тока, тем больше электродная поляризация, больше вероятность образования центров кристаллизации и тем меньше получаются кристаллы. Это видно из уравнения η=a+b∙lg j. Бесконечно плотность тока повышать нельзя, т.к. для большинства систем возникают диффузионные ограничения по доставке разряжающихся ионов к катодной поверхности. Появляется предельная плотность тока, начиная с которой покрытие будет получаться в виде порошка.

Iпред=
Нужно работать в области, где реализуется тафелевская зависимость. Чтобы повысить предельный ток и рабочую плотность тока, нужно видоизменять режим (перемешивание) или увеличивать концентрацию разряжающихся ионов, что не всегда возможно. В ряде случаев предельная плотность тока по разряжающимся ионам не возникает, но появляются условия, когда в покрытие включается большое количество гидроксидов и они становятся некачественными, а чем больше рабочая плотность тока, тем быстрее проходят эти включения.
2.)Влияние температуры: увеличение температуры облегчает практически все стадии электродного процесса, а значит, снижается поляризация. Кристаллы получаются крупнее и это невыгодно. Тем не менее, большинство процессов ведут при повышенных температурах, т.к. повышение значительно увеличивает коэффициент диффузии разряжающихся ионов, следовательно, повышается предельный ток. В результате, рабочую плотность тока можно тоже значительно увеличить, получая мелкокристаллические осадки. Кроме того, повышение температуры увеличивает растворимость труднорастворимых солей и гидроксидов, значит, облегчается анодный процесс, не включаются гидроксиды в катодный осадок, повышается электропроводность, снижаются энергозатраты, увеличивается равномерность покрытия на поверхности детали.
3.)Перемешивание: действует аналогично температуре, т.к. повышает предельную плотность тока благодаря уменьшению толщины диффузионного слоя, а значит, увеличивается рабочая область плотностей тока, можно работать на повышенных величинах с повышенной поляризацией. Хотя, если первоначальную плотность тока не менять и вводить перемешивание, поляризация будет несколько снижаться. Кроме того, перемешивание благоприятно сказывается на структуре покрытия благодаря лучшему механическому удалению пузырьков H2, который может выделяться наряду с Ме-П. Если пузырьки задерживаются на поверхности, то появляются язвы, что ведет к появлению пор.
4.)Влияние выделяющегося H2.Многие процессы осаждения Ме идут при параллельном выделении H2, и этот процесс негативно сказывается на качестве покрытия и на самой детали, т.к. выделяющийся водород:
А)может интенсивно внедряться в кристаллическую решетку Ме детали, возникает водородная хрупкость самой основы. Десорбируется водород медленно, и при нанесении слоя Ме, со временем выделяющийся H2 разрывает слой покрытия.
Б)может внедряться в само покрытие – наводораживаться, возникают большие внутренние напряжения, и в толстых слоях покрытие растрескивается и отходит от основы. Для устранения наводораживания применяют термообработку деталей с покрытием при T=200-250◦ в течение 2-4 часов.
В)приводит
к быстрому подщелачиванию прикатодного
пространства, в результате чего
образуются труднорастворимые гидроксиды,
которые входят или захватываются в
состав растущего покрытия, оно становится
некачественным. K:
 +2
+2 →Ni;
2H2O+2
→Ni;
2H2O+2 →H2+2OH-
;
→H2+2OH-
;
 +
OH-
→Ni(OH)2↓.
+
OH-
→Ni(OH)2↓.
Образование гидроксидов начинается в тот момент, когда достигается рН гидратообразования этих веществ. Для Ni рН~6. Если рабочая величина рН изначально всегда < рН гидратообразования, то в прикатодном пространстве рН сильно завышена по сравнению с объемным. Чем выше рабочая плотность тока, тем быстрее происходит смещение рН в область, где образуются труднорастворимые гидроксиды. Чтобы замедлить этот процесс, во многие электролиты (простые) вводят буферные добавки. Например, при цинковании: Al2(SO4)3+6H2O→2Al(OH)3+3H2SO4. По мере подщелачивания прикатодной области, равновесие этой реакции будет смещаться вправо, т.к. H2SO4 частично будет нейтрализовать полученные группы OH-, в результате чего рН гидратообразования почти не достигается и процесс можно вести на интенсивных режимах с высокой поляризацией с получением качественных, мелкокристаллических Ме-П. Для каждого вида Ме и электролитов подобраны свои оптимальные буферные добавки.
