
- •Лекция 1: 9.09.2015
- •Требования, предъявляемые к катодным осадкам в гальванотехнике и гидроэлектрометаллургии. 2
- •Механизм электрокристаллизации металлов
- •Лекция 3: 23.09.2015
- •Влияние природы осаждаемого Ме на величину кристаллов и Ме-п
- •Влияние режима электролиза на структуру металлических покрытий/осадков
- •Влияние состава электролита на структуру гальванических осадков
- •Лекция 4: 30.09.2015
- •Условия получения компактных поликристаллических осадков
- •Влияние различных факторов на рс электролита
- •Методы измерения рассеивающей способности
- •Анодные процессы гальванотехники. Выбор материала, вида и площади поверхности анода
- •Обезжиривание
- •Химическое обезжиривание
- •Электрохимическое обезжиривание
- •Промывочные операции
- •Электрополировка поверхностей Ме
- •Цинкование
- •Сульфатные электролиты цинкования
- •Лекция 10: 18.11.2015
- •Хлористоаммонийные и аммиакатные электролиты цинкования
- •Заключительные операции при цинковании
- •Сульфатные электролиты никелирования
- •Блестящее никелирование
- •Перспективные электролиты никелирования
- •Многослойное никелирование
- •1)Би-никель (двухслойное никелирование).
- •Хромирование. Целевое назначение. Электролиты и их сравнительная характеристика
- •Хромирование из сульфатного электролита
- •Усовершенствование процессов хромирования
- •Интенсификация процесса хромирования
- •Физико – химические свойства Cr-п
- •Механизм процесса анодирования
- •Заключительные операции при анодировании
- •Особые случаи анодирования
- •Электроосаждение сплавов
- •Лекция 15: 23.12.2015
- •Электроосаждение Ме-п в насыпном виде
- •1)Наливной колокол
- •2)Погружные вращающиеся барабаны. Они погружаются в гальваническую ванну, аноды с 2-х сторон вдоль граней барабана, он вращается и идет покрытие.
- •Осаждение Ме-п на реверсивном токе
Усовершенствование процессов хромирования
Работа
проводилась в плане упрощения анализа
концентрации катализатора и повышения
Вт. Известно, что в сульфатном хромировании
нужно четко поддерживать соотношение
100:1, часто анализировать электролит,
т.к. тратится CrO3
и кислота. Поэтому разработаны
саморегулирующиеся электролиты
хромирования. В них вместо H2SO4
используется сульфат стронция SrSO4,
который плохо растворим и находится в
избыточном количестве на дне ванны, а
по мере израсходования иона
 подрастворяется, в результате чего
количество ионов
подрастворяется, в результате чего
количество ионов
 стабилизируется. Аналогично действует
K2SiF6
– фторсиликат калия, где в образовании
пленки участвует SiF6.
Вт почти как в сульфатном, но такая соль
тоже плохо растворима и концентрация
ионов катализатора в объеме находится
в нужном количестве. Правда такой
электролит отличается сильной
агрессивностью к стальным деталям.
Незащищенное оборудование быстро
корродирует, но в таких электролитах
достигается максимальная прочность
сцепления покрытия со стальной основой.
Это важно для хромированных деталей,
которые работают в условиях трения и
износа. Для повышения Вт используют
модифицированный электролит хромирования,
который называется тетрахроматным. В
нем часть серной
и
хромовой кислот нейтрализована обычной
щелочью, в результате исходным веществом
начинают работать тетрахроматные
комплексы:
стабилизируется. Аналогично действует
K2SiF6
– фторсиликат калия, где в образовании
пленки участвует SiF6.
Вт почти как в сульфатном, но такая соль
тоже плохо растворима и концентрация
ионов катализатора в объеме находится
в нужном количестве. Правда такой
электролит отличается сильной
агрессивностью к стальным деталям.
Незащищенное оборудование быстро
корродирует, но в таких электролитах
достигается максимальная прочность
сцепления покрытия со стальной основой.
Это важно для хромированных деталей,
которые работают в условиях трения и
износа. Для повышения Вт используют
модифицированный электролит хромирования,
который называется тетрахроматным. В
нем часть серной
и
хромовой кислот нейтрализована обычной
щелочью, в результате исходным веществом
начинают работать тетрахроматные
комплексы:
 (иногда
(иногда
 ).
В виду того, что исходный хромовый анион
модифицирован, он разряжается с другими
возможностями, блокируя поверхность
для выделения Н2
в результате разряжается сам с более
высоким Вт=30-40%. В нем наоборот покрытия
получаются не твердыми, а более мягкими,
как правило, не блестящими, а серыми,
но легко полируются механически до
блестящего состояния.
).
В виду того, что исходный хромовый анион
модифицирован, он разряжается с другими
возможностями, блокируя поверхность
для выделения Н2
в результате разряжается сам с более
высоким Вт=30-40%. В нем наоборот покрытия
получаются не твердыми, а более мягкими,
как правило, не блестящими, а серыми,
но легко полируются механически до
блестящего состояния.
Интенсификация процесса хромирования
За счет повышения рабочей плотности тока – это полезно, т.к. Вт будет возрастать, правда одновременно электролит будет греться, а тепло снижать Вт. Часто Cr-П надо наносить большой толщины (десятки микрон или мм), тогда применяют технологию проточного электролита хромирования: деталь – катод и анод сближают на небольшое расстояние и через это пространство быстро прокачивают электролит, процесс можно вести на плотности тока до 200 А/дм2, т. е. в минуту сажать несколько микрон. За счет прокачки снижаются диффузионные ограничения, удаляется газ и отводится тепло, значит неплохие Вт и рабочая плотность тока. Примерно такие же принципы заложены, когда хромирование проводится в ультразвуковой установке, правда эта технология пригодна для небольших по размерам деталей.
Физико – химические свойства Cr-п
Ими можно управлять, меняя плотность тока и температуру. Исходя из соотношения этих величин можно получать твердый, серый, шероховатый, блестящий, матовый или молочный хром. Зона получения:

При низких температурах до 35◦С в широком диапазоне плотностей тока получается грубый, серый и шероховатый хром. Он самый твердый и практически не используется, некачественный.
II область является основной, t=45-60◦С, блестящий, декоративный, износостойкий и твердый хром в широком диапазоне плотностей тока.
При t>60◦ матовый или молочный хром, формируется относительно мягкий, более пластичный и легко полируется до блеска, тоже используют на практике.
Если
не следить за тепловым режимом ванны,
то можно уйти в ненужную область. При
выделении джоулева тепла Cr-П переходит
из блестящего в матовое, ванна должна
быть с охлаждением. Различие во внешнем
виде Cr-П связано с условиями кристаллизации
хрома, и в зависимости от температуры
меняется тип кристаллической решетки.
При хромировании кристаллизация
происходит с формированием отдельных
блоков, которые называются соматоиды,
структура напоминает цветную капусту.
При низких температурах формирование
соматоидов происходит из кристалликов
наименьших размеров. Эти кристаллы
быстро пассивируются, образуются новые
кристаллические зародыши, которые в
размерах вырасти не успевают. В результате
формируется достаточно плотная упаковка,
а решетка тетрагональная, покрытия
весьма напряженные и быстро образуются
трещины. С повышением температуры
соматоиды начинают формироваться из
кристаллов больших размеров и на ряду
с тетрагональной решеткой образуется
кубическая гранецентрированная,
появляется блеск и эта переходная
решетка обеспечивает необходимые
функциональные характеристики. При
максимальной температуре кристаллы
успевают вырасти, соматоиды формируются
из кристаллов больших размеров, блеск
пропадает, появляется матовость и
молочный оттенок. Кубическая решетка
дает пластичность и меньшую твердость.
Несмотря на вид полученных покрытий,
их можно принудительно модифицировать.
Например, блестящие Cr-П хороши, но пленка
масла не задерживается и износостойкость
в результате невысокая. Часто Cr-П
подвергают анодной обработке в том же
электролите хромирования, при котором
растворяются, прежде всего, границы
между кристаллическими блоками,
образуется сетка микроуглублений,
которая легко удерживает масленую
пленку и детали работают долгое время
на высоких нагрузках. Все современные
работы по хромированию направлены в
сторону создания электролитов на основе
 ,
т.к. они безвредны, унос минимальный,
могут работать с более высоким Вт и
электрохимические эквиваленты больше
,
т.к. они безвредны, унос минимальный,
могут работать с более высоким Вт и
электрохимические эквиваленты больше
 ,
при равных условиях процесс в 2 раза
пойдет быстрее.
,
при равных условиях процесс в 2 раза
пойдет быстрее.
 100-120
г/л
100-120
г/л
 20-30
г/л
20-30
г/л
 100
г/л
100
г/л
 80
г/л
80
г/л
рН=1-2, t=30-40◦С, j=30-50 А/дм2
Оксалат
Na
скорее всего работает как лиганд для
 ,
сульфат Al
и Na
как электропроводящие добавки,
одновременно
,
сульфат Al
и Na
как электропроводящие добавки,
одновременно
 мб буферной добавкой (см. цинкование).
Авторы аноды не указывают (хромовые
(
мб буферной добавкой (см. цинкование).
Авторы аноды не указывают (хромовые
( ,
,
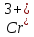 ),
если нерастворимые (
),
если нерастворимые ( до
до
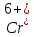 )).
)).
Лекция 14: 16.12.2015
Оксидирование алюминия
-
вид анодной обработки поверхности Al и
его сплавов. Здесь деталь загружается
в электролит в качестве анода и на ней
идут процессы окисления. В качестве
противоэлектродов – катодов, в
зависимости от вида электролита мб
использованы нерастворимые Ме (Pb,
нержавеющая сталь, графит). На катоде
– восстановление, выделение Н2.
В практике широко применяют анодирование
Al – процесс искусственного наращивания
естественной оксидной пленки на
поверхности Al. Естественная оксидная
пленка быстро формируется на поверхности.
Благодаря ее наличию,
 смещается от равновесного значения в
«+»
сторону на ~1 В и это обеспечивает
неплохую коррозионную стойкость Al
в нейтральных средах, но естественная
оксидная пленка Al2O3
имеет δ=0,01-0,02 мкм, является непрочной,
не твердой, быстро истирается и быстро
возобновляется. Если ее увеличить по
толщине, то Al можно придать новые
функциональные свойства. За счет толстой
оксидной пленки, Ме может приобретать
высокую твердость, износостойкость,
высокую коррозионную стойкость во
многих средах и высокие диэлектрические
характеристики. Это делают с помощью
анодирования. Кроме функциональных
свойств, анодная пленка обладает
высокими декоративными свойствами. В
зависимости от доп. обработки, в том
числе и в растворах пассивации и
растворах различных красителей можно
получить пленку различной цветовой
гаммы. Анодная пленка формируется
различной толщины для защитно-декоративных
целей, в том числе под окраску, где
достаточно 15-20 мкм; для защиты от коррозии
– несколько десятков; для обеспечения
твердости и износостойкости δ≈200 мкм.
Электролитов для анодирования Al не так
много, т.к. и сам Al и оксидная пленка
являются амфотерными, а значит, будут
растворяться в сильнощелочных и
сильнокислых средах, поэтому такие
среды не пригодны для анодирования. В
HNO3
при электролизе формируется тонкая
пленка, но в ходе процесса толщина не
увеличивается. Наиболее часто используют
электролит анодирования на основе
20%-ной H2SO4 200-250
г/л, именно в ней можно сформировать
оксидную пленку различной толщины и
свойств. Есть электролиты меньшей
интенсивности: на основе щавелевой
кислоты – оксолатные, в них, в отличие
от сернокислого, анодные пленки
получаются малопористыми, весьма
коррозионностойкими и эластичными.
Недостаток такого электролита: рост
напряжения на ванне в ходе самого
процесса анодирования. Существует
электролит на основе хромового ангидрида,
который позволяет получать слои
небольшой δ=3-4 мкм, малопористые, с очень
высокой коррозионной стойкостью. Здесь
сказывается доп.действие CrO3
на пассивацию поверхности Al, такой
электролит стараются применять на
деталях со сварными швами, труднодоступными
местами и для деталей, где сопряжены
несколько Al-сплавов.
Формирование оксидной пленки возможно
в условиях, когда под действием
проходящего тока она увеличивается в
толщине, а под действием электролита
эта пленка частично подрастворяется,
а стало быть толстые анодные слои можно
получить, когда скорость 1-ого процесса
превышает скорость 2-ого и это связано
с механизмом образования оксидной
пленки.
смещается от равновесного значения в
«+»
сторону на ~1 В и это обеспечивает
неплохую коррозионную стойкость Al
в нейтральных средах, но естественная
оксидная пленка Al2O3
имеет δ=0,01-0,02 мкм, является непрочной,
не твердой, быстро истирается и быстро
возобновляется. Если ее увеличить по
толщине, то Al можно придать новые
функциональные свойства. За счет толстой
оксидной пленки, Ме может приобретать
высокую твердость, износостойкость,
высокую коррозионную стойкость во
многих средах и высокие диэлектрические
характеристики. Это делают с помощью
анодирования. Кроме функциональных
свойств, анодная пленка обладает
высокими декоративными свойствами. В
зависимости от доп. обработки, в том
числе и в растворах пассивации и
растворах различных красителей можно
получить пленку различной цветовой
гаммы. Анодная пленка формируется
различной толщины для защитно-декоративных
целей, в том числе под окраску, где
достаточно 15-20 мкм; для защиты от коррозии
– несколько десятков; для обеспечения
твердости и износостойкости δ≈200 мкм.
Электролитов для анодирования Al не так
много, т.к. и сам Al и оксидная пленка
являются амфотерными, а значит, будут
растворяться в сильнощелочных и
сильнокислых средах, поэтому такие
среды не пригодны для анодирования. В
HNO3
при электролизе формируется тонкая
пленка, но в ходе процесса толщина не
увеличивается. Наиболее часто используют
электролит анодирования на основе
20%-ной H2SO4 200-250
г/л, именно в ней можно сформировать
оксидную пленку различной толщины и
свойств. Есть электролиты меньшей
интенсивности: на основе щавелевой
кислоты – оксолатные, в них, в отличие
от сернокислого, анодные пленки
получаются малопористыми, весьма
коррозионностойкими и эластичными.
Недостаток такого электролита: рост
напряжения на ванне в ходе самого
процесса анодирования. Существует
электролит на основе хромового ангидрида,
который позволяет получать слои
небольшой δ=3-4 мкм, малопористые, с очень
высокой коррозионной стойкостью. Здесь
сказывается доп.действие CrO3
на пассивацию поверхности Al, такой
электролит стараются применять на
деталях со сварными швами, труднодоступными
местами и для деталей, где сопряжены
несколько Al-сплавов.
Формирование оксидной пленки возможно
в условиях, когда под действием
проходящего тока она увеличивается в
толщине, а под действием электролита
эта пленка частично подрастворяется,
а стало быть толстые анодные слои можно
получить, когда скорость 1-ого процесса
превышает скорость 2-ого и это связано
с механизмом образования оксидной
пленки.
