
- •Лекция 1: 9.09.2015
- •Требования, предъявляемые к катодным осадкам в гальванотехнике и гидроэлектрометаллургии. 2
- •Механизм электрокристаллизации металлов
- •Лекция 3: 23.09.2015
- •Влияние природы осаждаемого Ме на величину кристаллов и Ме-п
- •Влияние режима электролиза на структуру металлических покрытий/осадков
- •Влияние состава электролита на структуру гальванических осадков
- •Лекция 4: 30.09.2015
- •Условия получения компактных поликристаллических осадков
- •Влияние различных факторов на рс электролита
- •Методы измерения рассеивающей способности
- •Анодные процессы гальванотехники. Выбор материала, вида и площади поверхности анода
- •Обезжиривание
- •Химическое обезжиривание
- •Электрохимическое обезжиривание
- •Промывочные операции
- •Электрополировка поверхностей Ме
- •Цинкование
- •Сульфатные электролиты цинкования
- •Лекция 10: 18.11.2015
- •Хлористоаммонийные и аммиакатные электролиты цинкования
- •Заключительные операции при цинковании
- •Сульфатные электролиты никелирования
- •Блестящее никелирование
- •Перспективные электролиты никелирования
- •Многослойное никелирование
- •1)Би-никель (двухслойное никелирование).
- •Хромирование. Целевое назначение. Электролиты и их сравнительная характеристика
- •Хромирование из сульфатного электролита
- •Усовершенствование процессов хромирования
- •Интенсификация процесса хромирования
- •Физико – химические свойства Cr-п
- •Механизм процесса анодирования
- •Заключительные операции при анодировании
- •Особые случаи анодирования
- •Электроосаждение сплавов
- •Лекция 15: 23.12.2015
- •Электроосаждение Ме-п в насыпном виде
- •1)Наливной колокол
- •2)Погружные вращающиеся барабаны. Они погружаются в гальваническую ванну, аноды с 2-х сторон вдоль граней барабана, он вращается и идет покрытие.
- •Осаждение Ме-п на реверсивном токе
Цинкование
Процесс
наиболее распространенный из-за
простоты, хорошего качества покрытия,
невысокой стоимости, возможности
нанесения на крупные и крайне мелкие
детали, покрытие можно наносить на
подвесах и насыпью, самое главное –
оно наиболее надежно и электрохимически
защищает основной Ме, т.е. сталь. Покрытие
является анодным по отношению к стали,
и благодаря более электроотрицательному
 ,
защита идет за счет собственного
растворения покрытия, а сама деталь не
разрушается, т.к. находится под
протекторной защитой и на ней идут
восстановительные деполяризующие
процессы. Защита возможна при наличии
пор и механических повреждений. Толщина
Zn-П в большинстве случаев 6-15 микрон, но
минимальной толщины часто не хватает
в жестких и особо жестких условиях, в
частности при наличии сернистого газа
или NaCl. В этих условиях целесообразнее
применять аналог цинка – Cd-П,
которые более стойки в морской атмосфере.
Но кадмий – дорог, признан токсичным
и от него отходят. Для увеличения
коррозионной стойкости Zn-П дополнительно
осветляют, хроматируют, а в последнее
время хромитируют и пропитывают
полимерами: коррозионная стойкость
повышается в 2-3 раза. Такие покрытия
применяются в наиболее жестких условиях.
За счет подбора электролитов можно
обеспечить качественное и равномерное
покрытие на различных мелких деталях,
что и используют в практике. По
механическим свойствам покрытия
являются ненапряженными, хорошо
развальцовываются и скручиваются. Но
Zn-П склонно к наводораживанию, что
вызывает значительные внутренние
напряжения и разрушение не только
покрытия, но и самой детали. От
наводораживания нужно избавляться.
Кроме того, электроотрицательный
,
защита идет за счет собственного
растворения покрытия, а сама деталь не
разрушается, т.к. находится под
протекторной защитой и на ней идут
восстановительные деполяризующие
процессы. Защита возможна при наличии
пор и механических повреждений. Толщина
Zn-П в большинстве случаев 6-15 микрон, но
минимальной толщины часто не хватает
в жестких и особо жестких условиях, в
частности при наличии сернистого газа
или NaCl. В этих условиях целесообразнее
применять аналог цинка – Cd-П,
которые более стойки в морской атмосфере.
Но кадмий – дорог, признан токсичным
и от него отходят. Для увеличения
коррозионной стойкости Zn-П дополнительно
осветляют, хроматируют, а в последнее
время хромитируют и пропитывают
полимерами: коррозионная стойкость
повышается в 2-3 раза. Такие покрытия
применяются в наиболее жестких условиях.
За счет подбора электролитов можно
обеспечить качественное и равномерное
покрытие на различных мелких деталях,
что и используют в практике. По
механическим свойствам покрытия
являются ненапряженными, хорошо
развальцовываются и скручиваются. Но
Zn-П склонно к наводораживанию, что
вызывает значительные внутренние
напряжения и разрушение не только
покрытия, но и самой детали. От
наводораживания нужно избавляться.
Кроме того, электроотрицательный
 по отношению к стали сохраняется до
t=50-60◦C,
а дальше Ɛ облагораживается и
электрохимическая защита снижается.
Это реализуется даже в горячей воде,
когда поверхность Zn покрывается
карбонатами и гидроксидами, и защита
лишь за счет толщины пленки, т.е. по
катодному механизму, что менее эффективно.
Тоже касается хроматных пленок: теряют
защитную способность при горячих
операциях. Электролиты цинкования как
и многие другие делятся на простые и
комплексные.
по отношению к стали сохраняется до
t=50-60◦C,
а дальше Ɛ облагораживается и
электрохимическая защита снижается.
Это реализуется даже в горячей воде,
когда поверхность Zn покрывается
карбонатами и гидроксидами, и защита
лишь за счет толщины пленки, т.е. по
катодному механизму, что менее эффективно.
Тоже касается хроматных пленок: теряют
защитную способность при горячих
операциях. Электролиты цинкования как
и многие другие делятся на простые и
комплексные.
!дальнейшая схема может использоваться и в других технологиях!
В простых электролитах осаждение Ме или восстановление из простых гидратированных ионов:
К:
 ,
,
 - пригодно для кадмирования, оловянирования,
свинцевания, никелирования. А:
в обратную сторону.
- пригодно для кадмирования, оловянирования,
свинцевания, никелирования. А:
в обратную сторону.
В
простых электролитах поляризация для
осаждения Zn небольшая, значит, кристаллы
получаются весьма крупными и для
улучшения качества покрытия вводят
ПАВ, увеличивающие ;
Вт высокий, более 90%, т.е. покрытие не
наводораживается и механические
характеристики не ухудшаются. В простых
электролитах можно работать на высоких
плотностях тока, т.е. интенсивных
режимах. Но т.к. поляризация мала,
поляризуемость невысокая и снижается
с ростом плотности тока, РС электролитов
невысокая, значит они дают неравномерные
по толщине покрытия, поэтому их
целесообразно использовать для покрытия
простых, листовых деталей. Т.к.
;
Вт высокий, более 90%, т.е. покрытие не
наводораживается и механические
характеристики не ухудшаются. В простых
электролитах можно работать на высоких
плотностях тока, т.е. интенсивных
режимах. Но т.к. поляризация мала,
поляризуемость невысокая и снижается
с ростом плотности тока, РС электролитов
невысокая, значит они дают неравномерные
по толщине покрытия, поэтому их
целесообразно использовать для покрытия
простых, листовых деталей. Т.к.
 в простых электролитах высокий, можно
использовать растворимые аноды из того
же Ме, что и Ме-П. Такие аноды работают
в активной области, растворяются с
Вт=100%, состав ванны во времени почти не
меняется. Простые электролиты устойчивы
к работе, недорогие и достаточно просто
утилизируются. К ним относят сульфатные
(ZnSO4),
хлоридные (ZnCl2)
и борфторатные (Zn(BF4)2)
электролиты цинкования. Они являются
слабокислыми, концентрация соли Ме
может быть большой и определяется она
растворимостью. Например, борфторатное
цинкование благодаря хорошей растворимости
соли может работать на максимальных
плотностях тока – интенсивных режимах.
в простых электролитах высокий, можно
использовать растворимые аноды из того
же Ме, что и Ме-П. Такие аноды работают
в активной области, растворяются с
Вт=100%, состав ванны во времени почти не
меняется. Простые электролиты устойчивы
к работе, недорогие и достаточно просто
утилизируются. К ним относят сульфатные
(ZnSO4),
хлоридные (ZnCl2)
и борфторатные (Zn(BF4)2)
электролиты цинкования. Они являются
слабокислыми, концентрация соли Ме
может быть большой и определяется она
растворимостью. Например, борфторатное
цинкование благодаря хорошей растворимости
соли может работать на максимальных
плотностях тока – интенсивных режимах.
Комплексные
электролиты, как правило, щелочные ионы
Ме, завязанные в «─» заряженный комплекс.
Процесс восстановления из комплекса
идет тяжело с повышенной поляризацией,
необходимой для разрыва комплекса, на
ряду с ней увеличивается поляризуемость,
а при наличии высоко электропроводной
среды, необходимой для устойчивости
комплекса достигается максимальная
РС. Значит, из комплексных электролитов
будут получаться наиболее равномерные
по толщине Ме-П. Это целесообразно
использовать в тех технологиях, где
детали сложно-профильные или при
покрытии мелких деталей в насыпном
виде. Рассеивающей способности
способствует также тенденция снижения
Вт с ростом плотности тока. Для РС это
хорошо, но снижение Вт приводит к
перераспределению тока на процесс
выделения H2,
а покрытие на детали будет наводораживаться.
Т.е. потребуется доп.обезводораживающая
термообработка. Кроме того, комплексные
электролиты для устойчивости имеют
относительно малую концентрацию ионов
Ме по отношению к лиганду. Это отношение
может достигать 1:10, 1:12, что приводит к
быстрому достижению на интенсивных
режимах концентрационных ограничений,
значит в таких электролитах на высоких
плотностях тока работать проблематично
и если в простых электролитах рабочая
j=8-10 А/дм2,
то в комплексных не выше 2-4 А/дм2.
Комплексные электролиты неустойчивы
в работе, т.к. они щелочные и электролиты
быстро карбонизируются: Na2CO3
копится и покрытия шероховатые. Кроме
того, часто для устойчивости комплекса
нужен избыток лиганда, а он может
окисляться на аноде, как в цианистых
электролитах. Также некоторые лиганды
окисляются кислородом воздуха. Т.к.
 заведомо меньше 100%, нужно подбирать
режимы работы анодов. Если плотность
тока минимальна (~1),
заведомо меньше 100%, нужно подбирать
режимы работы анодов. Если плотность
тока минимальна (~1),
 – большой и можно использовать активные
растворимые цинковые аноды. Если же
– большой и можно использовать активные
растворимые цинковые аноды. Если же
 велика и
велика и
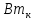 мал (~70%), требуется использовать
транспассивную работу анода или
комбинацию растворимых и нерастворимых
стальных анодов. К комплексным
электролитам относят:
мал (~70%), требуется использовать
транспассивную работу анода или
комбинацию растворимых и нерастворимых
стальных анодов. К комплексным
электролитам относят:
 .
Лучшими характеристиками обладают
цианистые электролиты, дают наиболее
качественное и равномерное Zn-П. Но в
настоящее время практически не
применяются из-за высокой ядовитости
цианистых солей. Их заменой являются
цинкатные электролиты: ZnO и NaOH. Качество
покрытия немного хуже, но за счет
доп.операций осветления и хроматирования
достигается хорошее качество и защита
от коррозии. Существуют такие электролиты
цинкования, содержащие NH3-комплекс
цинка и в зависимости от количества
лиганда - NH3,
эти электролиты могут быть слабокислыми
и в большей степени попадают под
характеристики простых кислых
электролитов. Если NH3
много, то такие электролиты используют
в слабощелочной среде, и в большей
степени относятся к комплексным. В
настоящее время такие электролиты
распространены из-за хорошего Вт,
средние рабочие j=3-4 А/дм2,
недорогие, устойчивы в работе, имеют
хорошую РС. Покрытия получаются весьма
равномерными и благодаря высокому Вт
покрытия ненаводораживаются. Недостаток:
промывные сточные воды тяжело очистить
от комплексов цинка, которые биологически
трудно разрушаются, весьма агрессивны
к металлическому оборудованию, т.к. при
наличии NH3
.
Лучшими характеристиками обладают
цианистые электролиты, дают наиболее
качественное и равномерное Zn-П. Но в
настоящее время практически не
применяются из-за высокой ядовитости
цианистых солей. Их заменой являются
цинкатные электролиты: ZnO и NaOH. Качество
покрытия немного хуже, но за счет
доп.операций осветления и хроматирования
достигается хорошее качество и защита
от коррозии. Существуют такие электролиты
цинкования, содержащие NH3-комплекс
цинка и в зависимости от количества
лиганда - NH3,
эти электролиты могут быть слабокислыми
и в большей степени попадают под
характеристики простых кислых
электролитов. Если NH3
много, то такие электролиты используют
в слабощелочной среде, и в большей
степени относятся к комплексным. В
настоящее время такие электролиты
распространены из-за хорошего Вт,
средние рабочие j=3-4 А/дм2,
недорогие, устойчивы в работе, имеют
хорошую РС. Покрытия получаются весьма
равномерными и благодаря высокому Вт
покрытия ненаводораживаются. Недостаток:
промывные сточные воды тяжело очистить
от комплексов цинка, которые биологически
трудно разрушаются, весьма агрессивны
к металлическому оборудованию, т.к. при
наличии NH3 поверхность депассивируется, образуются
гигроскопичные соли, содержащие аммоний,
который является активатором для
стальной поверхности. Для хлористоаммонийных
и аммиакатных в настоящие время создано
достаточно много блескообразующих и
улучшающих добавок. Сопоставить все
электролиты цинкования можно по
поляризационным кривым:
поверхность депассивируется, образуются
гигроскопичные соли, содержащие аммоний,
который является активатором для
стальной поверхности. Для хлористоаммонийных
и аммиакатных в настоящие время создано
достаточно много блескообразующих и
улучшающих добавок. Сопоставить все
электролиты цинкования можно по
поляризационным кривым:

