
- •Лекция 1: 9.09.2015
- •Требования, предъявляемые к катодным осадкам в гальванотехнике и гидроэлектрометаллургии. 2
- •Механизм электрокристаллизации металлов
- •Лекция 3: 23.09.2015
- •Влияние природы осаждаемого Ме на величину кристаллов и Ме-п
- •Влияние режима электролиза на структуру металлических покрытий/осадков
- •Влияние состава электролита на структуру гальванических осадков
- •Лекция 4: 30.09.2015
- •Условия получения компактных поликристаллических осадков
- •Влияние различных факторов на рс электролита
- •Методы измерения рассеивающей способности
- •Анодные процессы гальванотехники. Выбор материала, вида и площади поверхности анода
- •Обезжиривание
- •Химическое обезжиривание
- •Электрохимическое обезжиривание
- •Промывочные операции
- •Электрополировка поверхностей Ме
- •Цинкование
- •Сульфатные электролиты цинкования
- •Лекция 10: 18.11.2015
- •Хлористоаммонийные и аммиакатные электролиты цинкования
- •Заключительные операции при цинковании
- •Сульфатные электролиты никелирования
- •Блестящее никелирование
- •Перспективные электролиты никелирования
- •Многослойное никелирование
- •1)Би-никель (двухслойное никелирование).
- •Хромирование. Целевое назначение. Электролиты и их сравнительная характеристика
- •Хромирование из сульфатного электролита
- •Усовершенствование процессов хромирования
- •Интенсификация процесса хромирования
- •Физико – химические свойства Cr-п
- •Механизм процесса анодирования
- •Заключительные операции при анодировании
- •Особые случаи анодирования
- •Электроосаждение сплавов
- •Лекция 15: 23.12.2015
- •Электроосаждение Ме-п в насыпном виде
- •1)Наливной колокол
- •2)Погружные вращающиеся барабаны. Они погружаются в гальваническую ванну, аноды с 2-х сторон вдоль граней барабана, он вращается и идет покрытие.
- •Осаждение Ме-п на реверсивном токе
Хлористоаммонийные и аммиакатные электролиты цинкования
В последнее время стали применяться наиболее широко, т.к. они просты по составу, недорогие, обладают хорошей РС, работают в широком диапазоне рН, могут работать на повышенных плотностях тока и Вт может быть почти 100%. Значит, отсутствует наводораживание поверхности и покрытия. Для таких электролитов создано большое количество разнообразных блескообразующих добавок, причем полученные покрытия могут подвергаться различным видам доп.обработки и операции термообработки не нужны. Электролиты делятся в зависимости от рН на слабокислые 4,3-6,8 и слабощелочные 7,5-9. Первые обычно называют хлористоаммонийными, т.к. в них требуется значительное количество NH4Cl, как на построение комплекса, так и на создания нужной электропроводности. Слабощелочные чаще называют аммиакатными, т.к. в них преимущественно присутствуют различные аммиакатные цинковые комплексы. Электролит готовят путем растворения ZnO в NH4Cl:
Zn+2NH4Cl→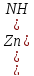
 +
NH4Cl→
+
NH4Cl→ +HCl,
+HCl,

 +
NH4Cl→
+
NH4Cl→ +HCl,
+HCl,

Для щелочной среды формирование комплексов путем добавления NH3:
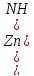 +2NH4Cl→
+2NH4Cl→ Cl]+2H2O,
Cl]+2H2O,

Меняя
количество лиганда можно менять
прочность комплексов и поляризационные
характеристики. Максимальная РС там,
где прочность комплексов наиболее
высокая, но с ростом плотности тока
быстрее будет снижаться Вт, т.е. большая
плотность тока пойдет на выделение Н2.
Это невыгодно, поэтому в слабощелочных
электролитах стараются работать на
невысоких j<3 А/дм2,
Вт>85%. В слабокислых электролитах
комплексы не столь прочные, РС там ниже,
но ее увеличивают за счет избыточного
количества хлорида аммония, который
начинает работать как электропроводящая
добавка. Кроме того, улучшить РС и
качество покрытия в таких электролитах
можно путем введения добавок ПАВ и
блескообразователей. Слабокислые
растворы ввиду малой прочности комплекса
как простые кислые, Zn разряжается как
из аммонийного комплекса с минимальным
количеством аммиака, так и из простых
гидратированных ионов. Разряд этих
веществ идет легко, значит можно ожидать
высокий Вт=95-98% и можно работать на
высоких j=6-8 А/дм2,
анодный процесс слабокислых растворов
не затруднен, идет активное растворение
анодов с Вт=100%, но при наличии слабокислой
среды и хороших лигандов аноды склонны
к интенсивной коррозии и с учетом этого
 =120%
- это плохо. Т.е. электролит пересыщается
по ионам цинка. Лиганда может не хватить
на образование комплекса, снизится
качество и РС, особенно коррозионные
процессы усиливаются с ростом температуры,
в том числе за счет выделяющегося
джоулева тепла. Поэтому такие ванны
принудительно охлаждают при повышении
температуры. В слабощелочных электролитах
проблема коррозии отсутствует, но при
повышении рН, аноды могут пассивироваться
за счет образования труднорастворимых
оксидных пленок. Нужно вводить добавки
депассиваторов – ацетат аммония
C2H3O2NH4,
NH4CNS.
Слабощелочные электролиты не требуют
введения буферных добавок, т.к. при
увеличении рН преимущественно
образовываются не аммиакатные, а
цинкатные комплексы, что неплохо. В
слабокислых требуется введение буферных
добавок и часто вводят борную кислоту,
чтобы рН прикатодной области не
сместилось в зону образования Zn(OH)2
– нерастворимого гидроксида. Нейтральные
электролиты цинкования здесь не
используют, т.к. не смотря на высокую
растворимость NH4Cl,
здесь минимальная растворимость ZnO и
надежного комплексообразования добиться
нельзя. Часто для повышения РС как в
кислых, так и слабощелочных электролитах
дополнительно в их состав вводят
уротропин. Он образует достаточно
прочный комплекс с ионами Zn в средах,
близких к нейтральным. Пример: ZnO
22-25 г/л
=120%
- это плохо. Т.е. электролит пересыщается
по ионам цинка. Лиганда может не хватить
на образование комплекса, снизится
качество и РС, особенно коррозионные
процессы усиливаются с ростом температуры,
в том числе за счет выделяющегося
джоулева тепла. Поэтому такие ванны
принудительно охлаждают при повышении
температуры. В слабощелочных электролитах
проблема коррозии отсутствует, но при
повышении рН, аноды могут пассивироваться
за счет образования труднорастворимых
оксидных пленок. Нужно вводить добавки
депассиваторов – ацетат аммония
C2H3O2NH4,
NH4CNS.
Слабощелочные электролиты не требуют
введения буферных добавок, т.к. при
увеличении рН преимущественно
образовываются не аммиакатные, а
цинкатные комплексы, что неплохо. В
слабокислых требуется введение буферных
добавок и часто вводят борную кислоту,
чтобы рН прикатодной области не
сместилось в зону образования Zn(OH)2
– нерастворимого гидроксида. Нейтральные
электролиты цинкования здесь не
используют, т.к. не смотря на высокую
растворимость NH4Cl,
здесь минимальная растворимость ZnO и
надежного комплексообразования добиться
нельзя. Часто для повышения РС как в
кислых, так и слабощелочных электролитах
дополнительно в их состав вводят
уротропин. Он образует достаточно
прочный комплекс с ионами Zn в средах,
близких к нейтральным. Пример: ZnO
22-25 г/л
NH4Cl 150-200 г/л
C6H12N4 80-100 г/л
H3BO3 10-25 г/л
рН=7,6÷8,3, j=1÷5 А/дм2, t=20÷50◦
Уротропин также вводят в состав слабокислых электролитов. В этих условиях повышается поляризуемость и улучшается в хлористоаммонийных РС. Аналогично уротропину действуют спец.соли Ликонда SR-A, SR-B:
ZnCl2 40-120 г/л
NH4Cl 180-200 г/л
Ликонда SR-A 30-70 г/л
Ликонда SR-B 3-5 г/л
рН=4,5÷6, j=05,÷5 А/дм2, t=15÷30◦
Для
создания устойчивых значений рН вводят
H3BO3
15-25 г/л. В слабокислых электролитах
взамен солей Ликонда предложены
блескообразующие и улучшающие добавки
типа ЦКН, ЛГ, Экомет. Хлористоаммонийные
электролиты широко используются для
нанесения покрытия на ответственные
детали в насыпном виде во вращающихся
барабанах и колоколах, можно работать
на интенсивных режимах, не боясь
наводораживания детали. ! При использовании
любого электролита цинкования в случае
нанесения покрытия насыпью, рабочая
плотность тока выбирается в пределах
 от
плотности тока рекомендованной для
данных электролитов при покрытии детали
на подвесах.!
от
плотности тока рекомендованной для
данных электролитов при покрытии детали
на подвесах.!
