- •8.Современные представления о гемопоэзе. Доказательтства существования родоначальной гемопоэтической клетки (эксперименты j.Till McCullach).
- •9.Основные этапы созревания гранулоцитов и моноцитов, опишите морфологические и цитохимические признаки клеток миелопоэза. Клиническое значение цитологического исследования клеток миелопоэза.
- •10.Основные этапы созревания, цитологическая и иммунофенотипическая характеристика лимфоцитов. Клиническое значение иммунофенотипирования.
- •11.Красный кровяной росток, этапы созревания, функционирование эритропоэтического ростка.
- •12.Цитологическое исследование костного мозга: методика, клиническое значение. Нормальная миелограмма. Клетки костномозгового окружения, морфологическая оценка и клиническое значение.
- •13.Методология и клиническое значение цитогенетических методов исследования костного мозга.
- •14.Хронические миелопролиферативные заболевания. Патогенез, диагностика.
- •15.Синдром недостаточности костного мозга. Причины, патогенез, диагностика. Миелодиспластические синдромы. Патогенез, современная классификация, диагностические критерии, прогноз.
- •16.Острый миелолейкоз. Методы цитохимического анализа миелобластов.
- •17.Методология и клиническое значение иммунофенотипирования клеток. Классификация лимфом. Значение лабораторных методов диагностики.
- •20.Цитологические характеристики и клиническое значение исследования бластов в крови и препарате костного мозга.
- •21.Понятие анемии. Классификация анемий.
- •22.Железодефицитная анемия, показатели обмена железа.
- •24.Диагностика гемолитических состояний. Методы ищучения аномальных форм гемоглобина.
- •25.Анемия хронических заболеваний. Этиология, патогенез, диагностика.
- •26.Апластические анемии.
- •27.Лейкопении и лейкоцитозы. Причины, диагностика.
- •28.Тромбоцитопении. Причины, подходы к дифференциальной диагностики.
- •29.Тромбоцитозы. Причины, дифференциальный диагноз, значение лабораторных методов диагностики.
- •31.Стадии созревания мегакариоцитов, морфологические и иммунофенотипические характеристики. Структура и функция рецепторов тромбоцитов, роль арахидоновой кислоты, простациклин, тромбоксан.
- •32.Физиология образования мочи. Подготовка, хранение и транспортировка мочи для клинического исследования.
- •33.Клиническое исследование мочи. Возможности визуальной колориметрии мочи в сравнении со стандартным клиническим исследованием.
- •34.Лейкоцитурия. Методы диагностики, клиническое значение. Дифференциальный диагноз септической и асептической лейкоцитурии.
- •35.Эритроцитурия. Этиология и механизмы эритроцитурии. Методы диагностики, клиническое значение.
- •36.Клиническое значение и методы выявления протеинурии.
- •37.Диагностика протеинурии переполнения. Феномен Бенс-Джонса. Понятие о моноклональных гаммапатиях
- •38.Клиническое значение выявления микроальбуминурии.
- •39.Методика микроскопирования осадка мочи. Патологические изменения и клиническое значение.
- •40.Клиническое исследование транссудатов и экссудатов. Плевральный выпот. Спинномозговой ликвор.
- •41.Клиническое исследование мокроты. Бронхоальвеолярный лаваж.
- •42.Принципы и основные параметры копрологического исследования. Клиническое значение.
- •45.Современные подходы к стандартизации коагуляционных тестов. Технология определения международного нормализированного отношения (мно). Клиническое значение мно.
- •46.Диссеминированное внутрисосудистое свертывание.
- •47.Болезнь Виллебранда. Этиология, классификация, диагностика.
- •48.Гемофилии. Классификация, подходы к диагностике, значение лабораторных методов.
- •49.Определение волчаночных антикоагулянтов. Ингибиторные коагулопатии. Антифосфолипидный синдром. Клинические проявления, диагностика.
- •50.Буферные растворы, основные характеристики. Требования, предъявляемые к буферным растворам в биологических исследованиях. Буферные свойства белков и аминокислот, уравнение Гендерсона-Хассельбаха.
- •51.Ионометрия. Ионоселективные электроды. Кислотность среды и ее измерения. Индикаторы.
- •52.Нарушения кислотно-щелочного равновесия.
- •53.Нарушения обмена калия. Причины, методы диагностики.
- •54.Центрифугирование. Принцип метода, основные определения, конструктивные особенности центрифуг. Препаративное и аналитическое центрифугирование. Аналитические ультрацентрифуги и их применение.
- •55.Хроматографические методы разделения веществ, их применение в клинической диагностике.
- •56.Электрофоретические методы разделения биоматериалов. Примеры применения в клинической практике. Значение электрофореза в протеомном анализе.
- •57.Лимфоплазмоклеточные дискразии. Клинические формы, диагностические критерии, методы лабораторной диагностики.
- •58.Диагностика и клиническое значение наследственных и приобретенных гиперлипидемий.
- •60.Методы и единицы измерения активности ферментов плазмы крови. Лабораторная диагностика заболеваний печени. Алт и аст. Γ-Глютамилтранспептидаза. Щелочная фосфатаза. Гепатоцитолиз. Холестаз.
- •61.Биохимическая диагностика инфаркта миокарда. Креатинкиназа. Лактатдегидрогеназа. Другие биохимические показатели повреждения миокарда.
- •62.Наследственные гипербилирубинемии. Диагностика желтухи. Нарушения обменов порфиринов.
- •63.Диагностика сахарного диабета. Значение определения гликозилированного гемоглабина.
- •64.Гипоальбуминемия. Дифференциальная диагностика.
- •65.Методы оценки фильтрационной функции почек. Хбп, Клиническое значение креатинина в крови.
- •66.Нарушение обмена пуринов. Подагра, хронический уратный интерстициальный нефрит.
- •67.Нефелометрический и турбидиметрический анализ в клинической практике. Отличие от других методов фотометрии.
- •69.Методы лабораторной диагностики воспаления. Клетки, вовлеченные в воспалительные процессы (нейтрофилы, моноциты, макрофаги, эндотелиальные клетки). Цитокины. Аутовоспалительные заболевания.
- •71.Скв, классификация, критерии диагностики. Le-клеточный феномен, антинуклеарные ат и их разновидности. Принципы лечения. Системная склеродермия, клиническая картина, диагностика, принципы лечения.
- •72.Системные васкулиты. Клиническая характеристика, проблемы классификации. Anca-феномен.
- •73. Криоглобулинемия, причины, патогенез, клинические проявления, методы диагностики.
- •74.Паранеопластический синдром (дерматомиозит и другие паранеопластические реакции), роль иммунологических методов диагностики, определение онкогенов.
- •75.Иммуносерологические исследования. Биологические основы определения групп крови. Клиническое значение определения групп крови.
- •76.Полимеразная цепная реакция. Современные методы диагностики инфекции. Достижения в молекулярной диагностике наследственных заболеваний. Понятие о геномике и протеомике.
61.Биохимическая диагностика инфаркта миокарда. Креатинкиназа. Лактатдегидрогеназа. Другие биохимические показатели повреждения миокарда.
При инфаркте миокарда (ИМ) в результате некроза клеток сердечной мышцы в кровеносное русло попадают содержащиеся в них ферменты и белки. По их наличию, времени появления и концентрации в плазме крови можно оценить ущерб, нанесенный сердечной мышце. Эти сведения дополняют данные ЭКГ и помогают в ранней диагностике ИМ, что позволяет своевременно избрать правильную тактику лечения.
Идеальный биохимический маркер должен обладать наивысшей специфичностью и чувствительностью в отношении некроза миокарда, в течение короткого времени после начала симптомов ИМ достигать в крови диагностически значимого уровня, этот уровень должен сохраняться в течение многих дней. В настоящее время маркера, полностью отвечающего всем этим требованиям, не существует, поэтому для диагностики ИМ рекомендуется параллельно использовать два маркера — "ранний" и "поздний". Содержание "раннего" маркера при ИМ диагностически значимо повышается в крови в первые часы заболевания, "поздний" —достигает диагностически значимого уровня только через 6—9 ч, но обладает высокой специфичностью в отношении некроза миокарда.
Ранние маркеры некроза миокарда:
Миоглобин
МВ-КФК (сердечная форма креатинфосфокиназы — КФК)
Сердечная форма белка, связывающего жирные кислоты (сБСЖК)
Поздние маркеры некроза миокарда:
Лактатдегидрогеназа (ЛДГ)
Аспартатаминотрансфераза (АсАТ)
Сердечные тропонины I и Т
Среди множества биохимических маркеров, которые могут менять свою концентрацию в плазме крови при ИМ, наиболее кардиоспецифическими являются тропонины, МВ-фракция креатенинфосфокиназы (КФК-МВ) и миоглобулин, которые и представляют наибольшую диагностическую ценность.
Тропонин - является ферментом «быстрого реагирования», поскольку попадает в периферический кровоток из зоны некроза уже в первые часы повреждения миокарда. Тропонины Т и I присутствуют только в клетках миокарда, поэтому повышение их концентрации в крови является достоверным признаком ИМ и показателем его распространенности. Отрицательный тропониновый тест вначале сердечного приступа и через 12 часов позволяет исключить у больного ИМ и диагностировать нестабильную стенокардию. Даже незначительное повышение уровня тропонинов в периферической крови через 6-12 часов после болевого приступа расценивается как признак ишемии миокарда ведущей к некрозу и позволяет выявить ИМ без явных клинических симптомов и ЭКГ-признаков заболевания.
МВ-фракция креатенинфосфокиназы (МВ-КФК) содержится преимущественно в клетках миокарда, но в небольшом количестве присутствует и в скелетных мышцах, поэтому активность этого фермента в крови может повышаться при повреждении не только сердечной мышцы, но и других мышечных групп. Судить о повреждении миокарда на фоне сердечного приступа позволяет нарастание активности МВ-КФК в динамике. Для диагностики ИМ в первые сутки от начала сердечного приступа ее определяют 2-3 раза каждые 8 часов. Три отрицательных результата позволяют исключить ИМ, а нарастание концентрации этого фермента в крови с высокой долей вероятности свидетельствует об ИМ. Уровень активности MB - КФК позволяет определить величину инфаркта миокарда и тяжесть заболевания.
Миоглобин — очень ранний и чувствительный, но менее специфичный маркер ИМ, поскольку содержание этого мышечного белка в крови может увеличиваться и по другим причинам. Миоглобин при сердечном приступе появляется в крови еще до формирования очага некроза, на стадии выраженного ишемического повреждения сердечной мышцы. Повышение уровня миоглобина в 10 раз и больше указывает на некроз мышечных клеток.
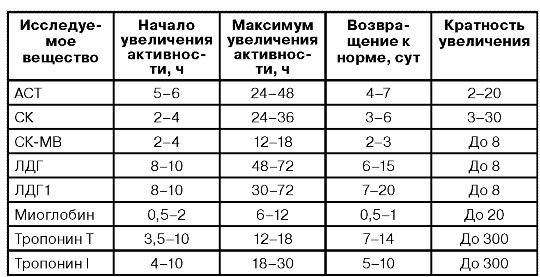
Лактатдегидрогеназа (ЛДГ) — фермент, принимающий участие в реакциях гликолиза, катализируя превращение лактата в пируват, при этом образуется NADH. ЛДГ имеет пять изо-энзимов. В сердечной мышце содержится преимущественно изоэнзим ЛДГ-1. При ИМ концентрация ЛДГ начинает превышать нормальный уровень через 14—48 ч после начала симптомов, достигает максимального значения на 3—6-е сутки заболевания и возвращается к норме на 7—14-е сутки болезни. ЛДГ-1 была обнаружена также в эритроцитах, почках, мозге, желудке, повышение концентрации этого белка в крови больных далеко не всегда связано с некрозом миокарда. Отношение ЛДГ-1/ЛДГ-2, превышающее 0,76, обладает 90% специфичностью при выявлении некроза миокарда. Это соотношение может увеличиваться и в случае отсутствия ИМ, если у больного имеются массивный гемолиз, мегалобластическая анемия, распространенное повреждение скелетных мышц, тяжелое заболевание печени. Из-за позднего повышения концентрации ЛДГ в сыворотке крови этот маркер не применяется для ранней диагностики ИМ и суждения об успехе тромболитической терапии, однако ЛДГ длительно использовалась для диагностики ИМ в поздние сроки заболевания.
Аспартатаминотрансфераза (АсАТ) – фермент, который катализирует преобращение оксалоацетата в аспартат, перенося NH3 на первую молекулу. Вторым продуктом реакции является α-кетоглутарат. Реакция играет важную роль в высвобождении NH3 из аминокислот, который затем перерабатывается в цикле мочевины, так как аспартат, полученный в процессе реакции, нужен для образования аргининосукцината. У больных ИМ уровень АсАТ превышает норму через 8—12 ч после начала боли, достигает максимального значения к 24—З6-му часу и возвращается к норме за 3—4 дня. Большое количество этого фермента содержится в тканях печени, что сильно снижает его специфичность в отношении некроза миокарда. АсАТ неудобна как для ранней, так и для поздней диагностики ИМ, она используется только в сочетании с более чувствительными и специфичными маркерами. Низкая специфичность в отношении некроза миокарда послужила причиной того, что использование этого маркера, как и ЛДГ, для диагностики ИМ в настоящее время также признано нецелесообразным..
Повышение АСТ, превышающее повышение АЛТ, характерно для повреждения сердечной мышцы; если же показатель АЛТ выше, чем АСТ, то это, как правило, свидетельствует о разрушении клеток печени.
Неспецифическая реакция на повреждение миокарда включает нейтрофильный лейкоцитоз (появляется через несколько часов после окклюзии и длится 3-7 сут, число лейкоцитов достигает 12000-15000 в мкл). СОЭ повышается медленнее, достигает пика в 1-ю неделю и часто остается повышенной в течение 1-2 нед.
сБСЖК по последовательности аминокислот идентичен БСЖК, содержащемуся в поперечнополосатой мышечной ткани скелетных мышц, однако представлен в скелетной мускулатуре в минимальном количестве. Максимальное количество сБСЖК находится в ткани миокарда — 0,5 мг/г. Единственная мышца, в которой имеется относительно большое количество сБСЖК, — это диафрагма (примерно 25% от содержания в ткани миокарда). Некоторое количество сБСЖК содержится в тканях аорты, и можно предположить, что содержание его повышается, в крови при расслаивающей аневризме аорты. Так как сБСЖК в основном свободно расположен в цитоплазме клеток, в случае повреждения клеточной мембраны кардиомиоцита он быстро попадает в кровоток. В крови здоровых людей циркулирует небольшое количество сБСЖК.