
- •Часть I
- •Оглавление
- •Соединения кислорода и серы
- •Лекарственные средства группы водорода пероксида
- •Гидроперит Hydroperitum
- •Химические свойства водорода пероксида
- •Получение
- •Описание и растворимость
- •Подлинность
- •Чистота
- •Количественное определение
- •1 Молекула МgO2 → 1 молекула h2o2
- •Определение стабилизатора натрия бензоата в растворе водорода пероксида
- •Хранение
- •Вода для инъекций Aqua pro injectionibus
- •Анализ воды очищенной и воды для инъекций в условиях аптек
- •Чистота
- •Количественное определение
- •Хранение
- •Применение
- •Формы выпуска
- •Галогены и их соединения со щелочными металлами Общая характеристика
- •Распространение в природе
- •Биологическое значение
- •Медицинское значение
- •Галогены
- •Получение
- •Описание и растворимость
- •Подлинность
- •Чистота
- •Количественное определение
- •Хранение
- •Чистота
- •Количественное определение
- •Хранение
- •Применение
- •Соли галогенводородных кислот
- •Получение
- •Описание и растворимость
- •Подлинность
- •Чистота
- •Количественное определене
- •Хранение
- •Применение
- •Получение
- •Описание и растворимость
- •Подлинность
- •Количественное определение
- •Описание и растворимость
- •Физические и химические свойства
- •Подлинность
- •Чистота
- •Количественное определение
- •Хранение
- •Описание и растворимость
- •Подлинность
- •Чистота
- •Количественное определение
- •Хранение
- •Чистота
- •Количественное определение
- •Хранение
- •Распространение в природе
- •Биологическая роль
- •Соединения магния
- •Получение
- •Описание и растворимость
- •Подлинность
- •Чистота
- •Количественное определение
- •Хранение
- •Применение
- •Соединения кальция
- •Получение
- •Описание и растворимость
- •Подлинность
- •Чистота
- •Количественное определение
- •Хранение
- •Описание и растворимость
- •Подлинность
- •Чистота
- •Количественное определение
- •Распространение в природе
- •Чистота
- •Количественное определение
- •Хранение
- •Применение
- •Формы выпуска
- •Соединения алюминия
- •Получение
- •Описание и растворимость
- •Подлинность
- •Чистота
- •Количественное определение
- •Хранение
- •Применение
- •Соединения цинка
- •Получение
- •Описание и растворимость
- •Подлинность
- •Чистота
- •Количественное определение
- •Хранение
- •Чистота
- •Количественное определение
- •Хранение
- •Чистота
- •Количественное определение
- •Хранение
- •Количественное определение
- •Количественное определение
- •Хранение
- •Применение
- •Формы выпуска
Хранение
Список Б. В склянках темного стекла с притертыми пробками в защищенном от света месте. При длительном хранении спирт окисляется под действием йода с образованием кислот (CH3COOH и HI), которые оказывают раздражающее действие на кожу:
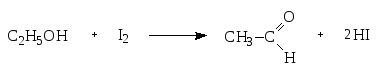
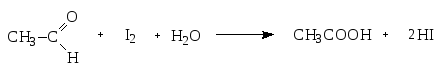
Как скоропортящийся ЛП, раствор йода 5% ежеквартально подлежит переконтролю.
Применение
Антисептическое средство. Применяют наружно для обработки ран, подготовки операционного поля.
ГАЛОГЕНВОДОРОДНЫЕ КИСЛОТЫ
Кислота хлороводородная – Acidum hydrochloricum
Содержание хлороводорода (НCI) 24,8 – 25,2%
Кислота хлороводородная разведенная
Acidum hydrochloricum dilutum
Содержание хлороводорода (НCI) 8,2 – 8,4%
Получение
Растворением в воде газа хлороводорода, который получают прямым синтезом из водорода и хлора, образующихся при электролизе раствора натрия хлорида:
Электролиз
2NaCI + 2H2O CI2 + 2NaОН + H2
Н2 + CI2 2НCI + 187,4 кДж
НCI + H2O Раствор кислоты хлороводородной 35-36%.
Полученный 35-36% раствор кислоты хлороводородной разбавляют до необходимой концентрации.
Описание
Бесцветные прозрачные летучие жидкости со своеобразным запахом, кислой реакции среды. Смешиваются с водой и спиртом во всех соотношениях.
Подлинность
1. Реакция окисления хлорид-иона марганца (IV) оксидом до свободного хлора:
4НСI + MnO2 → CI2 + MnCI2 + 2H2O
Хлор обнаруживают по запаху.
2. Реакция осаждения хлорид-иона раствором серебра нитрата в азотнокислой среде:
НСI + AgNO3 → AgCI + НNO3
Образуется белый творожистый осадок серебра хлорида, растворимый в растворе аммиака:
AgCI↓ + 2NH4OH → [Ag(NH3)2]CI + 2H2O
3. Доказательство протона. К ЛВ прибавляют метиловый оранжевый или метиловый красный; раствор окрашивается в розовый цвет.
Чистота
Определяют специфические примеси:
1. Свободный хлор. Обнаруживают по реакции с раствором калия йодида в присутствии хлороформа. Не должно наблюдаться фиолетовой окраски хлороформного слоя (примесь не допустима). В присутствии примеси протекает реакция:
CI2 + 2KI → I2 + 2KCI
2. Сернистая кислота. При прибавлении к ЛВ раствора йода и раствора крахмала должно сохраняться синее окрашивание (примесь не допустима).
При наличии примеси протекает реакция:
I2 + Н2SO3 + H2O → 2HI + Н2SO4
Количественное определение
1. Алкалиметрический метод нейтрализации. Индикатор – метиловый оранжевый.
НСI + NaOH → NaCI + H2O
fэкв (НСI) = 1
2. Аргентометрический метод (вариант Фольгарда). Основан на осаждении хлорид-ионов серебра нитратом. Вариант обратного титрования. Индикатор – железоаммониевые квасцы.
Хранение
Список Б. В склянках с притертыми пробками.
Применение
При пониженной кислотности желудочного сока. Для приема внутрь используется кислота хлороводородная разведенная в виде капель или микстур.
Соли галогенводородных кислот
(Галогениды калия и натрия)
|
Лекарственное вещество. Формула
|
МНН и латинское название. Формы выпуска
|
|
Натрия хлорид
NaCI |
Sodium chloride* Natrii chloridum Субстанция; растворы для инъекций: изотонический 0,9%, гипертонический 10%
|
|
Калия хлорид
KCI |
Potassium chloride* Kalii chloridum Субстанция; раствор для инъекций 4%; раствор для приема внутрь 10%; таблетки 0,5 и 1,0 г
|
|
Натрия бромид
NaBr |
Sodium bromide* Natrii bromidum Субстанция; таблетки 0,5 г; 3% раствор для приема внутрь
|
|
Калия бромид
KBr |
Potassium bromide* Kalii bromidum Субстанция; таблетки 0,5 г
|
|
Натрия йодид
NaI |
Sodium iodide* Natrii iodidum Субстанция
|
|
Калия йодид
KI |
Potassium iodide* Kalii iodidum Субстанция; таблетки 0,2 мг; 0,125; 0,25 и 0,5 г; глазные капли; 3% раствор для приема внутрь
|
