
- •Часть I
- •Оглавление
- •Соединения кислорода и серы
- •Лекарственные средства группы водорода пероксида
- •Гидроперит Hydroperitum
- •Химические свойства водорода пероксида
- •Получение
- •Описание и растворимость
- •Подлинность
- •Чистота
- •Количественное определение
- •1 Молекула МgO2 → 1 молекула h2o2
- •Определение стабилизатора натрия бензоата в растворе водорода пероксида
- •Хранение
- •Вода для инъекций Aqua pro injectionibus
- •Анализ воды очищенной и воды для инъекций в условиях аптек
- •Чистота
- •Количественное определение
- •Хранение
- •Применение
- •Формы выпуска
- •Галогены и их соединения со щелочными металлами Общая характеристика
- •Распространение в природе
- •Биологическое значение
- •Медицинское значение
- •Галогены
- •Получение
- •Описание и растворимость
- •Подлинность
- •Чистота
- •Количественное определение
- •Хранение
- •Чистота
- •Количественное определение
- •Хранение
- •Применение
- •Соли галогенводородных кислот
- •Получение
- •Описание и растворимость
- •Подлинность
- •Чистота
- •Количественное определене
- •Хранение
- •Применение
- •Получение
- •Описание и растворимость
- •Подлинность
- •Количественное определение
- •Описание и растворимость
- •Физические и химические свойства
- •Подлинность
- •Чистота
- •Количественное определение
- •Хранение
- •Описание и растворимость
- •Подлинность
- •Чистота
- •Количественное определение
- •Хранение
- •Чистота
- •Количественное определение
- •Хранение
- •Распространение в природе
- •Биологическая роль
- •Соединения магния
- •Получение
- •Описание и растворимость
- •Подлинность
- •Чистота
- •Количественное определение
- •Хранение
- •Применение
- •Соединения кальция
- •Получение
- •Описание и растворимость
- •Подлинность
- •Чистота
- •Количественное определение
- •Хранение
- •Описание и растворимость
- •Подлинность
- •Чистота
- •Количественное определение
- •Распространение в природе
- •Чистота
- •Количественное определение
- •Хранение
- •Применение
- •Формы выпуска
- •Соединения алюминия
- •Получение
- •Описание и растворимость
- •Подлинность
- •Чистота
- •Количественное определение
- •Хранение
- •Применение
- •Соединения цинка
- •Получение
- •Описание и растворимость
- •Подлинность
- •Чистота
- •Количественное определение
- •Хранение
- •Чистота
- •Количественное определение
- •Хранение
- •Чистота
- •Количественное определение
- •Хранение
- •Количественное определение
- •Количественное определение
- •Хранение
- •Применение
- •Формы выпуска
Описание и растворимость
Кислота борная – бесцветные, блестящие, слегка жирные на ощупь чешуйки или мелкий кристаллический порошок без запаха.
Растворима в 25 частях воды, в 4 частях кипящей воды, в 25 частях спирта и медленно в 7 частях глицерина.
Натрия тетраборат – бесцветные, прозрачные, легко выветривающиеся кристаллы или белый кристаллический порошок.
Растворим в воде, очень легко в кипящей воде, практически не растворим в спирте, легко растворим в глицерине.
Физические и химические свойства
1. Отношение кислоты борной к нагреванию.
Кристаллическая кислота борная при длительном нагревании до 100 0С теряет воду и превращается в кислоту метаборную HBO2, при более сильном нагревании образуется кислота тетраборная H2B4O7 в виде стекловидной сплавленной массы, а при полной потере воды образуется борный ангидрид B2O3.
При нагревании водных или спиртовых растворов кислоты борной она улетучивается с парами растворителя.
2. Кислотно-основные.
Кислота борная относится к очень слабым кислотам. Кдис = 6,4 • 10-10
Водные растворы кислоты борной имеют слабокислую реакцию среды. При взаимодействии со щелочами образует соли: метабораты (NaBO2) или тетрабораты (Na2B4O7). Соли ортоборной кислоты H3BO3 не образуются.
Водные растворы натрия тетрабората имеют щелочную реакцию среды, так как происходит гидролиз:
Na2B4O7 + 7H2O ↔ 4H3BO3 + 2NaOH
3. Кислота борная с одноатомными алифатическими спиртами образует эфиры, с многоатомными спиртами и полифенолами – комплексные соединения.
При взаимодействии с глицерином кислота борная образует кислоту глицеринборную, которая проявляет более сильные кислотные свойства. Растворы кислоты борной в глицерине имеют кислую реакцию среды.
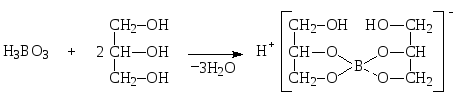
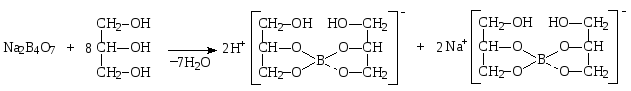
Натрия тетраборат тоже взаимодействует с глицерином. При этом образуются натриевая соль глицеринборной кислоты и свободная глицеринборная кислота, поэтому растворы натрия тетрабората в глицерине имеют кислую реакцию среды.
Подлинность
1. Общие реакции.
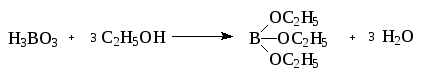
1.1. Реакция образования борноэтилового эфира. Раствор кислоты борной в этаноле горит пламенем, окаймленным зеленым цветом.
Для натрия тетрабората реакция образования борноэтилового эфира проводится в присутствии кислоты серной концентрированной.
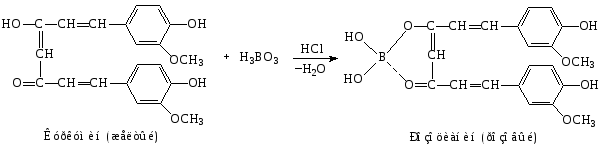
2. Реакция с куркумином – образование комплексных соединений.
Для проведения реакции используется куркумовая бумага (фильтровальная бумага, пропитанная раствором куркумина), на которую наносится раствор ЛВ и кислота хлороводородная разведенная. После высушивания бумага окрашивается в розовый цвет, при смачивании раствором аммиака окраска переходит в зеленовато-черную.
2. Специфические реакции.
Натрия тетраборат – реакции на катион натрия (см. с. 24).
Чистота
Определяют общие примеси: хлориды, сульфаты, железо, тяжелые металлы.
Для кислоты борной определяют:
1. Прозрачность и цветность водного и спиртового растворов – должны быть прозрачными и бесцветными.
2. Примесь минеральных кислот (используются при получении кислоты борной). При добавлении к водному извлечению из лекарственного вещества индикатора метилового оранжевого не должно быть розового окрашивания. Сама борная кислота, как очень слабая, не дает розового окрашивания с этим индикатором.
