
- •Часть I
- •Оглавление
- •Соединения кислорода и серы
- •Лекарственные средства группы водорода пероксида
- •Гидроперит Hydroperitum
- •Химические свойства водорода пероксида
- •Получение
- •Описание и растворимость
- •Подлинность
- •Чистота
- •Количественное определение
- •1 Молекула МgO2 → 1 молекула h2o2
- •Определение стабилизатора натрия бензоата в растворе водорода пероксида
- •Хранение
- •Вода для инъекций Aqua pro injectionibus
- •Анализ воды очищенной и воды для инъекций в условиях аптек
- •Чистота
- •Количественное определение
- •Хранение
- •Применение
- •Формы выпуска
- •Галогены и их соединения со щелочными металлами Общая характеристика
- •Распространение в природе
- •Биологическое значение
- •Медицинское значение
- •Галогены
- •Получение
- •Описание и растворимость
- •Подлинность
- •Чистота
- •Количественное определение
- •Хранение
- •Чистота
- •Количественное определение
- •Хранение
- •Применение
- •Соли галогенводородных кислот
- •Получение
- •Описание и растворимость
- •Подлинность
- •Чистота
- •Количественное определене
- •Хранение
- •Применение
- •Получение
- •Описание и растворимость
- •Подлинность
- •Количественное определение
- •Описание и растворимость
- •Физические и химические свойства
- •Подлинность
- •Чистота
- •Количественное определение
- •Хранение
- •Описание и растворимость
- •Подлинность
- •Чистота
- •Количественное определение
- •Хранение
- •Чистота
- •Количественное определение
- •Хранение
- •Распространение в природе
- •Биологическая роль
- •Соединения магния
- •Получение
- •Описание и растворимость
- •Подлинность
- •Чистота
- •Количественное определение
- •Хранение
- •Применение
- •Соединения кальция
- •Получение
- •Описание и растворимость
- •Подлинность
- •Чистота
- •Количественное определение
- •Хранение
- •Описание и растворимость
- •Подлинность
- •Чистота
- •Количественное определение
- •Распространение в природе
- •Чистота
- •Количественное определение
- •Хранение
- •Применение
- •Формы выпуска
- •Соединения алюминия
- •Получение
- •Описание и растворимость
- •Подлинность
- •Чистота
- •Количественное определение
- •Хранение
- •Применение
- •Соединения цинка
- •Получение
- •Описание и растворимость
- •Подлинность
- •Чистота
- •Количественное определение
- •Хранение
- •Чистота
- •Количественное определение
- •Хранение
- •Чистота
- •Количественное определение
- •Хранение
- •Количественное определение
- •Количественное определение
- •Хранение
- •Применение
- •Формы выпуска
Чистота
Все шесть ЛВ подвергают следующим испытаниям:
1. Прозрачность и цветность водного раствора (должны быть прозрачными и бесцветными).
2. Кислотность или щелочность водного раствора (должны иметь нейтральную реакцию среды).
3. Предельное содержание общих примесей (железо, тяжелые металлы, сульфаты, мышьяк).
4. Отсутствие катионов бария и кальция (не должно появляться мути при добавлении к раствору ЛВ кислоты серной разведенной).
5. Потеря в массе при высушивании.
В отдельных ЛВ дополнительно проверяют отсутствие специфических примесей.
Натрия хлорид, калия хлорид.
1. Отсутствие магния (Mg2+) (с Na2HPO4 и NH4OH) и аммония (NH4+) (с реактивом Несслера).
2. В натрия хлориде – отсутствие калия (К+) (реакция с виннокаменной кислотой); в калия хлориде – отсутствие натрия (Na+) (по окрашиванию пламени), т.к. Na+ и К+ являются физиологическими антагонистами.
Натрия бромид, калия бромид (MeBr).
1. Отсутствие йодидов (I–). К раствору ЛВ прибавляют FeCl3 и крахмал; не должно быть синего окрашивания.
При наличии примеси:
2MeI + 2FeCl3 → I2 + 2FeCl2 + 2MeCl
I2 + крахмал → синее окрашивание
Сами ЛВ железа (III) хлоридом не окисляются.
2. Отсутствие броматов (BrO3–). К раствору ЛВ прибавляют кислоту серную разведенную; не должно быть желтого окрашивания.
При наличии примеси:
MeBrO3 + 5MeBr + 3H2SO4 → 3Br2 + 3Me2SO4 + 3H2O
(Примесь) (ЛВ) (Реактив) (Желтое
окрашивание)
Натрия йодид, калия йодид (MeI).
1. Отсутствие цианидов (СN–). При добавлении к раствору ЛВ FeSO4 и FeCl3 не должно появляться синего окрашивания. В присутствии примеси образуется железа (III) гексацианоферрат (II) (см. с. 18).
2. Отсутствие йодатов (IO3–). К раствору ЛВ прибавляют кислоту серную разведенную и крахмал; не должно появляться синего окрашивания.
В присутствии примеси:
MeIO3 + 5MeI + 3H2SO4 → 3I2 + 3Me2SO4 + 3H2O
(Примесь) (ЛВ) (Реактив)
I2 + крахмал → синее окрашивание
3. Отсутствие тиосульфат (S2O32–) и сульфит (SO32–)-ионов. К раствору ЛВ прибавляют крахмал и 1 каплю раствора йода (0,1 моль/л) УЧ (Ѕ I2); должно появиться синее окрашивание.
I2 + крахмал → синее окрашивание
В присутствии примесей йод восстанавливается до йодида:
I2 + 2Na2S2O3 → 2НI + Na2S4O6
I2 + Na2SO3 + H2O → 2НI + Na2SO4
4. Отсутствие нитратов (NO3–). При нагревании ЛВ с цинком в щелочной среде не должен выделяться аммиак (красная лакмусовая бумага не должна окрашиваться в синий цвет).
При наличии примеси протекает реакция окисления-восстановления:
NaNO3 + 4Zn + 7NaOH → NH3↑ + 4Na2ZnO2 + 2H2O
Количественное определене
1. Аргентометрический метод. Основан на свойстве галогенид-ионов количественно осаждаться серебра нитратом с образованием галогенидов серебра.
MeHal + AgNO3 → AgHal + MeNO3
fэкв (ЛВ) = 1
1.1. Натрия хлорид, калия хлорид, натрия бромид, калия бромид.
Вариант Мора (прямое титрование); индикатор – калия хромат. Среда – нейтральная.
NaСI + AgNO3 → AgCI + NaNO3
NaBr + AgNO3 → AgBr + NaNO3
Индикация: 2AgNO3 + K2CrO4 Ag2CrO4 + 2KNO3
Осадок коричневато- красного цвета
Метод может быть использован для количественного определения хлоридов и бромидов в ЛП, содержащих ЛВ слабо-основного характера (например, натрия бензоат), создающих слабо-щелочную реакцию среды.
Натрия йодид и калия йодид не определяют, т.к. йодиды адсорбируются на осадке AgI, окраска появиться до точки эквивалентности (заниженные результаты).
1.2. Натрия йодид, калия йодид.
1.2.1. Вариант Фаянса (прямое титрование); индикатор – натрия эозинат (адсорбционный индикатор). Среда – уксуснокислая (разбавленная CH3cooh).
а) NaInd Ind + Na+
Эозинат натрия
б) NaI + AgNO3 AgI + NaNO3
в) Ind- + AgI + AgNO3 [(AgI)Ag+]Ind + NO
Изб. капля Розовый осадок
Вариант Фаянса может быть применен для определения хлоридов и бромидов натрия и калия. В качестве индикаторов используются бромфеноловый синий и флуоресцеин. Натрия эозинат не применяют, т.к. он адсорбируется на осадках AgCI и AgBr раньше точки эквивалентности.
1.2.2. Вариант Кольтгофа (прямое титрование). Используется для определения натрия и калия йодидов (селективный метод) в многокомпонентных ЛП, содержащих другие галогениды (например, NaСI, KСI, CaCl2, NaBr, KBr). Титрант: раствор серебра нитрата.
Индикатор: йодкрахмальный – 1 капля раствора калия йодата (0,1 моль/л) УЧ (1/6 KIO3), раствор крахмала (2 мл) и по каплям разведенной кислоты серной до появления синего окрашивания.
KIO3 + 5KI + 3H2SO4 → 3I2 + 3K2 SO4 + 3H2O Уравнение
I2 + КI + крахмал синее окрашивание индикации
По мере титрования из раствора осаждаются йодиды, связываясь с серебра нитратом:
KI + AgNO3 → AgI + KNO3
В точке эквивалентности происходит обесцвечивание раствора, т. к. йодиды полностью исчезнут из раствора.
Хлориды и бромиды не мешают определению, т.к. могут осаждаться только после йодид-ионов (ПР AgI = 1,5 1016; ПР AgBr = 4,4 1013; ПР AgCI = 1,8 1010).
1.3. Для количественного определения натрия и калия хлоридов, бромидов и йодидов в ЛП используются также варианты:
1.3.1. Фольгарда (обратное титрование).
1.3.2. Фольгарда в модификации Кольтгофа (косвенный или видоизмененный вариант Фольгарда).
(См. МУ «Фармацевтический анализ по функциональным группам и общие титриметрические методы анализа, Пермь, 2008 – с. 85-87).
Аргентометрический метод дает точные результаты, быстр в выполнении. Недостаток: титрант серебра нитрат – дорогостоящий реактив, поэтому метод не экономичен.
2. Меркуриметрический метод. Основан на свойстве галогенид-ионов количественно взаимодействовать с солями ртути (II) с образованием труднодиссоциируемых (малоионизированных) галогенидов ртути (II).
Применяют для всех галогенидов натрия и калия.
Титранты – легко ионизированные соли ртути (II): ртути (II) нитрат – Hg(NO3)2, ртути (II) перхлорат – Hg(CIO4)2.
2MeHal + Hg(NO3)2 → HgHal2 + 2MeNO3
fэкв(MeHal) = 1
Среда: азотнокислая.
Индикатор: дифенилкарбазон.
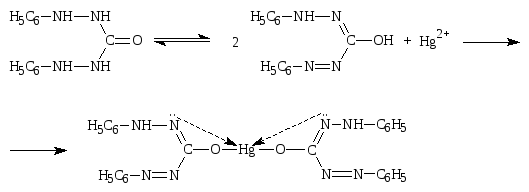
Светло-сиреневое окрашивание
Йодиды натрия и калия титруют в присутствии этанола, концентрация которого в конце титрования должна быть не менее 55%, т.к. ртути йодид мало растворим в воде и имеет ярко-красную окраску осадка, что затрудняет фиксирование точки эквивалентности. Используется свойство ртути (II) йодида растворяться в спирте с образованием бесцветных растворов.
Титрант: ртути (II) перхлорат (0,01 моль/л) УЧ [1/2 Hg(ClO4)2]
2KI + Hg(ClO4)2 HgI2 + 2KClO4
Спирт : вода (1:1)
fэкв (ЛВ) = 1
3. Броматометрический метод. Используется в анализе йодидов калия и натрия.
Метод основан на восстановительных свойствах йодидов. Йодид-ионы окисляются калия броматом в среде кислоты хлороводородной до йодмонохлорида:
6KI + KBrO3 + 6HCI → 3I2 + 6KCI + KBr + 3H2O
3I2 + KBrO3 + 6HCI → 6ICI + KBr + 3H2O
Суммарное уравнение:
6KI + 2KBrO3 + 12HCI → 6ICI + 2KBr + 6KCI + 6H2O
Уравнение после сокращения коэффициентов:
3KI + KBrO3 + 6HCI → 3ICI + KBr + 3KCI + 3H2O
fэкв (MeI) = 1/2 (IЇ –2ē → I+)
