
УЧЕБНИК ВНУТРЕННИЕ БОЛЕЗНИ
.pdf5. Показания общих коагуляционных тестов (АПТВ, протромбиновый и тромбиновый тесты, содержание в плазме фибриногена).
Лечение ДВС-синдрома.
Выявление клинических и лабораторных признаков острого сепсиса (ознобы, лихорадка, потливость, лейкоцитоз и др.) требует немедленного проведения антибактериальной терапии:внутривенноевведениевысоких доз антибиотиков широкого спектра действия.
Устранениеявлений шока, нарушений гемодинамики и дыхания, в том числе раннее подключение аппаратов искусственной вентиляции легких (с повышением давления на выдохе).
Заместительно-коррекционнаятерапияраннее и достаточное по объему ежедневное введение свежезамороженной плазмы (СЗП) в сочетании с одновременным введением гепарина - по 15-20 тыс. ед в сутки на ранних этапах острого или подострого ДВС-синдрома и по 10-15 тыс. ед вместе с СЗП во IIи IIIфазах процесса. Объем переливаемой плазмы всегда должен быть не менее 10-15 мл/кг массы тела (для взрослых больных - 1 л в сутки, а в наиболее тяжелых случаях - 1,5 л и более).
Наряду с трансфузиями СЗП, при лечении острого ДВС-синдрома используются внутривенные вливания кровезаменителей - препаратов крахмала и др., что имеет значение как для купирования явлений шока, так и для обеспечения гемодилюции и восстановления микроциркуляции в органах.
Сцелью восстановления антикоагулянтного потенциала крови полученныеиз плазмы или рекомбинантныеконцентратыантитромбина III, протеина С (цепротин) и тромбомодулина.
В комплексной терапии ДВС-синдрома вместо гепарина могут применяться также низкомолекулярные гепарины(в умеренных дозах), надропарин (фраксипарин).
При острой почечной недостаточности капельное внутривенное введение допамина (0,05% раствор на 5% глюкозе) со скоростью 5-10 кап./мин (суточная доза 200-400 мг) с одновременной стимуляцией диуреза
лазиксом (40-80)мг. При недостаточном |
эффекте -этапныйплазмаферез |
|||
(при |
синдромесдавления, |
остром |
внутрисосудистом |
гемолизе, |
гангренизацией тканей при укусах змей и при развитии гепаторенального синдрома), при продолжающейся анурии - гемодиализ.
Принципиально важно при лечении ДВС-синдрома - не начинать трансфузионную терапию с введений эритромассы и, тем более, нативной донорской крови, поскольку при этом усиливается тромботический процесс и блокада микроциркуляции в органах, что ведет к усилению, а не ослаблению гипо ксических явлений в тканях. Поэтому общим правилом при оказании помощи больным с ДВС – синдромом является первоначальное применение СЗП и гемодилюции, а затем при необходимости - возмещение кровопотери эритромассой.
421
На поздних этапах - замещение тромбоцитов трансфузиями по 4-5 доз концентрата этих клеток в сутки, а также внутривенное введение больших доз антипротеаз – контрикала по 50-100 тыс. ед. и более (суточная доза до 500 тыс.ед.) (с целью выведения больного из синдрома реинфузии, который может возникнуть в процессе деблокады микроциркуляции в органах).
С целью предупреждения вторичного сепсиса: антибиотики локального действия внутрь и лактозу, которая способствует преобладанию молочнокислой микрофлоры в кишечнике.
Больные с ДВС-синдромом нуждаются в интенсивном круглосуточном наблюдении гемастезиологов и реаниматологов.
422
РАЗДЕЛ IV. НЕФРОЛОГИЯ
ГЛАВА 1. ОСТРЫЙ И ХРОНИЧЕСКИЙ ГЛОМЕРУЛОНЕФРИТЫ. Острый гломерулонефрит (ГН) – ГН, характеризующийся
внезапным развитием гематурии, протеинурии, артериальной гипертензии (АГ) и отеков, в части случаев с переходящим нарушением функции почек, которые сочетаются с морфологической картиной острого диффузного пролиферативного ГН.
Острый ГН часто связан с инфекционными заболеваниями. Одним из таких постинфекционных нефритов является острый постстрептококковый гломерулонефрит (ОПСГН), который отличается от других острых ГН типичными серологическими и гистологическими признаками.
Морфологическая картина ОПСГН включает:
oпризнаки воспаления:
-в начале заболевания – полиморфно-ядерные нейтрофилы, эозинофилы, макрофаги (фаза экссудации);
-в разгаре заболевания – макрофаги;
oпролиферацию:
-внутриклубочковую (часто);
-полулуния: очаговые (часто), распространенные (редко);
oиммунные депозиты:
-IgG (иммуноглобулин G), С3, пропердин – диффузный гранулярный тип отложения («звездное небо» на ранних этапах, «гирлянды» - на поздних);
-субэпителиальные («горбы»), субэндотелиальные и мезангиальные. В случаях преобладания пролиферации мезангиальных и
эндотелиальных клеток используется термин «пролиферативный нефрит»; в случаях, когда преобладает инфильтрация полиморфно–ядерными лейкоцитами – применяют термин «экссудативный ГН».
Клинические и лабораторные особенности ОПСГН включают:
- предшествующую стрептококковую инфекцию (латентный период ОПСГН составляет 1-2 недели после фарингита, 3-6 недель после кожной инфекции; в течение латентного периода иногда выявляется микрогематурия);
-возможное субклиническое течение;
-неспецифические симптомы (общее недомогание, слабость, тошнота, иногда с рвотой); у 5-10 больных также возможны тупые боли в пояснице, которые объясняют растяжением капсулы почек в результате
отека перенхимы;
- развернутый остронефритический синдром – у 40 больных (отеки,
гематурия, АГ, олигурия); у 96 больных отмечают как минимум два из этих симптомов;
- отеки – главная жалоба большинства больных (для подростков характерны отеки на лице и лодыжках, для детей младшего возраста – генерализованные отеки);
423
- АГ (развивается более чем у 80 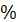 больных, но только у половины из них требует назначения антигипертензивных ЛС; редко осложняется развитием энцефалопатии);
больных, но только у половины из них требует назначения антигипертензивных ЛС; редко осложняется развитием энцефалопатии);
-иногда застойная сердечная недостаточность в результате задержки жидкости и АГ;
-гематурию, которая служит обязательным симптомом ОПСГН;
при этом у 2/3 больных обнаруживают микрогематурию, у 1/3 – макрогематурию, которая после увеличения диуреза обычно исчезает.
Микрогематурия может служить единственным проявлением острого эндокапиллярного пролиферативного ГН и сохранятся в течение многих месяцев после острого периода. С помощью фазово – контрастной микроскопии выявляют дисморфные (измененные) эритроциты, указывающие на клубочковое происхождение гематурии;
- протеинурию (выраженная протеинурия - ≥ 3 г/сут – наблюдается только у 4 % детей с клиникой ОПСГН, у взрослых – значительно чаще). Иногда транзиторное нарастание протеинурии отмечается через 1-2 недели болезни по мере восстановления СКФ;
детей с клиникой ОПСГН, у взрослых – значительно чаще). Иногда транзиторное нарастание протеинурии отмечается через 1-2 недели болезни по мере восстановления СКФ;
- цилиндрурию (эритроцитарные, гранулярные и пигментные цилиндры наблюдаются часто; при тяжелом экссудативном гломерулонефрите возможно обнаружение лейкоцитарных цилиндров);
-лейкоцитурию (нередко);
-снижение СКФ – у 25%больных в начале заболевания (при этом
уровень креатинина в сыворотке крови может повышаться до 2 мг/дл и более);
-выявление антистрептококковых антител:
-у больных с фарингитом более чем в 95% случаев;
-у больных с инфекцией кожи в 80% случаев;
-ложноположительные результаты – 5%.
-ранняя антибактериальная терапия подавляет антительный ответ – возможность получения нормальных титров антител на фоне приема
антибиотиков;
-снижение уровня комплемента (гемолитической активности) СН5 и/или С3, С4 - более чем в 90% случаев;
-гипергаммаглобулинемию – в 90%случаев;
-поликлональную криоглобулинемию – в 75% случаев.
Общие принципы лечения (Н. А. Мухин, Л. В. Козловская, Е. М. Шилов и др., 2008) включают:
-режим и диету:
-постельный режим в первые 3-4 недели болезни при значительных отеках, макрогематурии, выраженной АГ и СН;
-значительное ограничение потребления натрия (до 1-2 г/сут)
и воды в острый период болезни, особенно при выраженных признаках нефрита (быстром начале с отеками, олигурией и АГ). В первые 24 ч рекомендуют полностью прекратить прием жидкости, что само по себе может привести к уменьшению
424
отеков. В дальнейшем прием жидкости не должен превышать диуреза;
- ограничение приема белка до 0,5 г/кг в сутки в случае значительного снижения СКФ и развития олигурии; - лечение стрептококковой инфекции (больные и их родствен ники).
Такая терапия прежде всего показана, если ОПСГН возникает после перенесенного фарингита, тонзиллита, гнойничкового поражения кожи, особенно при положительных результатах посевов с кожи, зева, а также при высоких титрах антистрептококковых антител в крови;
-нормализацию АД, уменьшение отеков;
-поддержание водно-электролитного баланса;
-лечение осложнений (энцефалопатия, гиперкалиемия, отек легких,
ОПН);
-иммунодепрессивную терапию – при нефротическом синдроме и затянувшемся течении ГН.
Лечение стрептококковой инфекции.
В первые дни ОПСГН назначают:
-Феноксиметилпенициллин в/м 125 мг 4 р/сут, 7-10 сут.
Вслучае развития аллергической реакции на пенициллины
назначают:
-Эритромицин внутрь 250 мг 4 р/сут, 7-10 сут.
Терапия при отеках.
При периферических отеках назначают:
-Гидрохлоротиазид внутрь 50-100 мг 1 р/сут, утром натощак, до исчезновения отеков (только при СКФ>30 мл/с) или
-Фуросемидид внутрь 80-120 мг 1 р/сут утром натощак, до исчезновения отеков (при любой СКФ).
В случае отека легких назначают:
-Фуросемид 40-1000 мг в/в струйно, до 4-6 р/сут (в зависимости от диуреза и клинических проявлений)
±
-Морфин 5-10 мг в/в струйно, однократно.
Гипотензивная терапия При АГ назначают:
-Нифедипин внутрь 10 мг 3-6 р/сут под контролем АД, длительно
±
-Каптоприл внутрь 6,25-25 мг 2-3 р/сут под контролем АД, длительно или
-Лизиноприл внутрь 2,5-10 мг 1 р/сут под контролем АД, длительно или
-Периндоприл внутрь 2-4 мг 1 р/сут под контролем АД, длительно
или
-Рамиприл внутрь 1,25-5 мг 1 р/сут под контролем АД, длительно или
-Фозиноприл внутрь 10 мг 1-2 р/сут под контролем АД, длительно
425
или
-Эналаприл внутрь 2,5-10 мг 2 р/сут под контролем АД, длительно.
Лечение энцефалопатии, судорожного синдрома В случае гипертонической энцефалопатии применяют:
-Фуросемид в/в струйно 40-200 мг под контролем АД, однократно (при недостаточности диуретическом эффекте возможно повторное введение ЛС)
±
- Нитроглицерин, р-р с концентрацией 100 мкг/мл, в/в капельно с начальной скоростью 5 мкг/мин под контрол ем АД (каждые 3-5 мин возможно увеличение скорости инфузии максимально до 100 -200 мкг/мин), длительность лечения определяют индивидуально или - Нитропруссид натрия, р-р, в/в капельно 1-1,5 мкг/кг/мин под
контролем АД (при необходимости скорость введения постепенно увеличивают до 8 мкг/кг/мин), длительность лечения определяют индивидуально (р-р готовят непосредственно перед применением: сначала растворяют содержимое 1 ампулы в 5 мл 5 р-ра декстрозы, затем разводят дополнительно в 1000, 500 или 250 мл 5% р-ра декстрозы). Применение неразведенного р-ранитропруссида натрия недопустимо.
±
-Магния сульфат, 20-25 р-р, в/м или в/в струйно медленно 5-20 мл, кратность введения определяется клинической ситуацией.
При наличии судорожного синдрома к терапии добавляют:
-Диазепам в/в струйно 10-30 мг, однократно (при необходимости введение ЛС повторяют через 1 ч, затем через 4 ч).
Терапия ГКС.
Больным с развившимся и длительно (более 2 недель) сохраняющимся нефротическим синдромом, стабильно повышенным уровнем креатинина без тенденции к дальнейшему нарастанию и возвращению к норме в случае невозможности проведения биопсии почки показано:
- Преднизолон внутрь 1 мг/кг/сут (2 -3 дозы в утренний прием, после еды, 1/3 дозы в дневной прием, после еды), 1-2 мес.
В случае быстро прогрессирующей почечной недостаточности и выявления полулуний при биопсии почек рекомендовано:
- Метилпреднизолон в/в капельно 500-1000 мг 1 р/сут ежедневно, 3-5 сут.
Хронический гломерулонефрит (ХГН) – это воспалительное заболевание почек иммунного генеза с преимущественным исходным поражением клубочков и вовлечением в патологический процесс всех почечных структур, клинически проявляющееся почечными и/или внепочечными симптомами с неуклонно прогрессирующим течением и исходом в почечную недостаточность.
426
Этиология.
Причинные факторы большинства форм ХГН неизвестны. Установлена роль инфекции – бактериальной, особенно нефритогенных штаммов β-гемолитического стрептококка группы А, вирусов гепатита В и С, ВИЧ – инфекции; лекарственных препаратов (D-пеницилламин и др.); опухолей и других факторов экзо- и эндогенного происхождения.
В патогенезе ХГН выделяют ряд основных механизмов, которые можно разделить на две группы:
1.Иммунные, или иммуновоспалительные (иммунный ответ, иммунное воспаление, склеротические изменения).
2.Неиммунные (гемодинамические, метаболические).
Иммунные механизмысвязаны с образованием иммунных комплексов (ИК) "антиген-антитело" в присутствии комплемента. При этом происходит пассивный занос ИК в клубочек и их осаждение на гломерулярной базальной мембране (ГБМ) и в мезангии.
Начало иммунного воспалительного процесса связано с активацией медиаторов тканевого повреждения, обусловленный комплементемией, активацией хемотаксических факторов, способствующих миграции лейкоцитов.
Активное образование и выброс факторов роста и цитокинов соровождается ответной реакцией со стороны гломерулярных клеток. В результате взаимодействия их с этими медиаторами возникает клеточная пролиферация с выделением активных радикалов и ферментов, накопление и расширение мезангиальной мембраны, что приводит к снижению функции почек и фиброзно-склеротическими изменениями.
Особенно важны эффекторные реакции клеточного иммунитета, в которых участвуют сенсибилизированные лимфоциты и моноциты - макрофаги. В местах отложения иммунных комплексов или в местах их образования происходит активация системы комплемента, вероятно, по альтернативному пути - без участия факторов С2 и С4. Это приводит к образованию мембраноатакующего комплекса: С5b-C9 или полиС9, встраивающегося в базальные мембраны клеток и ГБМ и нарушающего их проницаемость. У нейтрофилов и моноцитов имеются рецепторы к С 3b, которые могут активировать эти клетки с последующим повреждением окружающих тканей. С5a и C3a, являющиеся анафилотоксинами, способствуют запуску местных процессов воспаления и влияют на микроциркуляцию в сосудистой системе клубочков.
Под влиянием разнообразных патологических стимулов (антигены, ЦИК, продукты тромбоцитов, компоненты комплемента и др.) моноциты активируются и выделяют в кровь широкий спектр биологически активных веществ: ИЛ-1, ФНОα, фибронектин и др. У больных ХГН отмечено нарушение грануломоноцитопоэза в костном мозге, приводящее к образованию функционально неполноценных моноцитов (макрофагов), т.о. страдает антигенпредставляющая, фагоцитарная, метаболическая функции моноцитов и развивается гиперпродукция медиаторов воспаления.
427
Основная часть ИЛ-1 выводится через почки, где его концентрация в 4 - 8 раз выше, чем в других тканях. Следовательно, независимо от места образования в организме, ИЛ-1 может концентрироваться в почечной ткани и вызывать целый комплекс реакций острого воспаления, активную пролиферацию мезангиальных клеток и продукцию мезангиального матрикса.
Нарушенные процессы взаимодействия клеток системы мононуклеарных фагоцитов (СМФ) с клетками сосудистого эндотелия, тромбоцитами, фибробластами, лимфоцитами запускают каскад процессов вторичной альтерации, в частности, через активацию кининовой системы. Это приводит к нарушениям почечной гемодинамики, развитию гиперкоагуляции на фоне сниженной активности системы фибринолиза и активации фибропластических процессов с развитием склерозирования нефронов.
Механизмы прогрессирования ХГН связаны не только с непосредственным поражением гломерулярного аппарата, но и интерстициального пространства. Дополнительным фактором аутоагрессии является повреждение канальцев почек вследствие длительной протеинурии.
Неиммуновоспалительные механизмы прогрессирования ХГН.
В соответствии с гипотезой Бреннера, по мере прогрессирования поражения почек функцию склерозированных нефронов берут на себя оставшиеся, что приводит к гипертрофии клубочкового аппарата почек, системной гипертензии и другим изменениям. В свою очередь, гиперфильтрация, выступая в роли дополнительного фактора вторичной альтерации, повреждает клубочки, способствуя их склерозированию.
Системная артериальная гипертензия также ведет к прогрессированию склеротических процессов в почечной ткани.
В патогенезе гиперлипидемии при ХГН рассматривается роль гипоальбуминемии, которая приводит к активизации синтеза липопротеидов в печени (преимущественно богатых триглицеридами - низкой и очень низкой плотности). Мезангиальные клетки, аккумулирующие значительное количество липидов, превращаются в так называемые "пенистые клетки", формирующие атероматозные бляшки в ткани почек. Существует прямая связь между переполнением мезангия липидами и гломерулярным склерозом, а также между концентрацией сывороточного холестерина и частотой гломерулярных повреждений. Гиперлипопротеидемия вызывает патологич ескую активацию мезангиальных макрофагов, что приводит к запуску иммунных механизмов гломерулонефрита, замыкая порочный круг.
Размеры повреждений ГБМ даже при самых активных вариантах ХГН намного меньше диаметра эритроцита с учетом его конформационных возможностей. Поэтому основное место проникновения эритроцитов в мочу - перитубулярные капилляры, т.е. гематурия имеет капиллярно-канальцевое происхождение. Это подтверждается наличием
428
ранних воспалительно-дистрофических изменений перитубулярных капилляров при ХГН. Исключение составляют случаи некротических изменений в клубочках почки.
При изучении протеинурии важным является качественный состав белков в моче. В нормальной почке свободно фильтруются и реабсорбируются около 4 г/сут низкомолекулярных белков: альбумины, фрагменты легких цепей Ig, микроглобулины, гормоны - вазопрессин, инсулин, глюкагон, АКТГ, паратгормон, гормон роста), лизоцим, некоторые ферменты. Появление в моче высокомолекулярных белков (глобулинов, трансферринов и т.п.) свидетельствует о грубой мембранной патологии. Исключение составляет белок Тамма - Хорсвалла, секретируемый эпителием восходящей части петли Генле. В моче здоровых людей обнаруживается 30-60 мг/сут этого белка. Увеличение концентрации протеина и закисление мочи при воспалении приводят к его агрегации с образованием геля, являющегося матриксом почечных цилиндров.
Все перечисленные механизмы, в конечном счете, приводят к развитию нефросклероза.
Морфологические варианты ХГН:
1.Мембранозная нефропатия.
2.Мембранопролиферативный (мезангиокапиллярный).
3.Мезангиопролиферативный.
4.Минимальные изменения (липоидный нефроз).
5.Фокально-сегментарный гломерулосклероз (ФСГС).
6.Фибропластический (стадия нефросклероза).
Первичный идиопатический ГН–заболевание с первичным поражением почек.
Вторичный ГН – поражение почек в рамках системного или иных заболеваний, а также вследствие лечебных вмешательств.
Выделяют пролиферативные формы (характеризуются увеличением числа клеток в клубочке):
-мезангиопролиферативный;
-мембранознопролиферативный (мезангиокапиллярный) инепролиферативные формы (при которых поражаются слои
клубочкового фильтра, образующие основной барьер для белков, а именно подоциты и базальная мембрана) –
-мембранозная нефропатия;
-болезнь минимальных изменений;
-фокально-сегментарный гломерулосклероз.
Метод верификации диагноза- пункционная нефробиопсия.
Показаниями к нефробиопсии являются:
-уточнение морфологической формы;
-оценка активности;
-дифференциальная диагностика с системными заболеваниями соединительной ткани, быстропрогрессирующим ГН, амилоидозом.
429
В нефробиоптате при ХГН выявляются следующие морфологические изменения:
- мембранозный ГН– диффузное утолщение базальной мембраны клубочков с формированием субэпителиальных выступов, окружающих отложения иммунных комплексов (зубчатый вид базальной мембраны);
- мембранопролиферативный (мезангиокапиллярный) ГН–
диффузная пролиферация мезангиальных клеток и инфильтрация клубочков макрофагами, увеличение мезангиального матрикса, утолщение
иудвоение базальной мембраны;
-мезангиопролиферативныйГН – диффузная пролиферация
мезангиальных клеток и инфильтрация клубочков макрофагами; увеличение площади мезангиального матрикса.
-ХГН с минимальными изменениями световая микроскопия не позволяет выявить какие-либо изменения, при электронной микроскопии – «слияние» (сглаживание) ножек подоцитов;
-фокально-сегментарныйгломерулосклероз (ФСГС)–
сегментарное спадение капилляров менее чем в 50% клубочков с отложением аморфного гиалинового материала;
- фибропластический ГН – исход всех гломерулопатий, характеризуется выраженностью фибротических процессов.
Клиническая классификация ХГН.
По формам:
1.Гипертоническая форма.
2.Нефротическая форма.
3.Смешанная форма.
4.Латентная форма.
5.Гематурическая форма.
По фазам:
1.Обострение (активная фаза, рецидив) - появление нефритического синдрома, снижение функции почек.
2.Ремиссия (неактивная фаза) - улучшение или нормализация (реже) лабораторных и экстраренальных проявлений (отеков, АГ).
По патогенезу:
1.Первичный (идиопатический).
2.Вторичный – ассоциированный с общим или системным
заболеванием.
Клиническая картина.
Гипертоническая форма.
Составляет примерно 1/5 всех случаев хронического гломерулонефрита. При этой форме изменения в моче обычно минимальны, протеинурия не превышает 1 г/сут., иногда микрогематурия, цилиндрурия. Ведущее клиническое проявление этой формы — артериальная гипертензия, которая вполне удовлетворительно переносится больными, в связи с чем они нередко поздно обращаются к врачу.
430
