
Часть 2
.PDF
598 ГЛАВА 13. Легкие
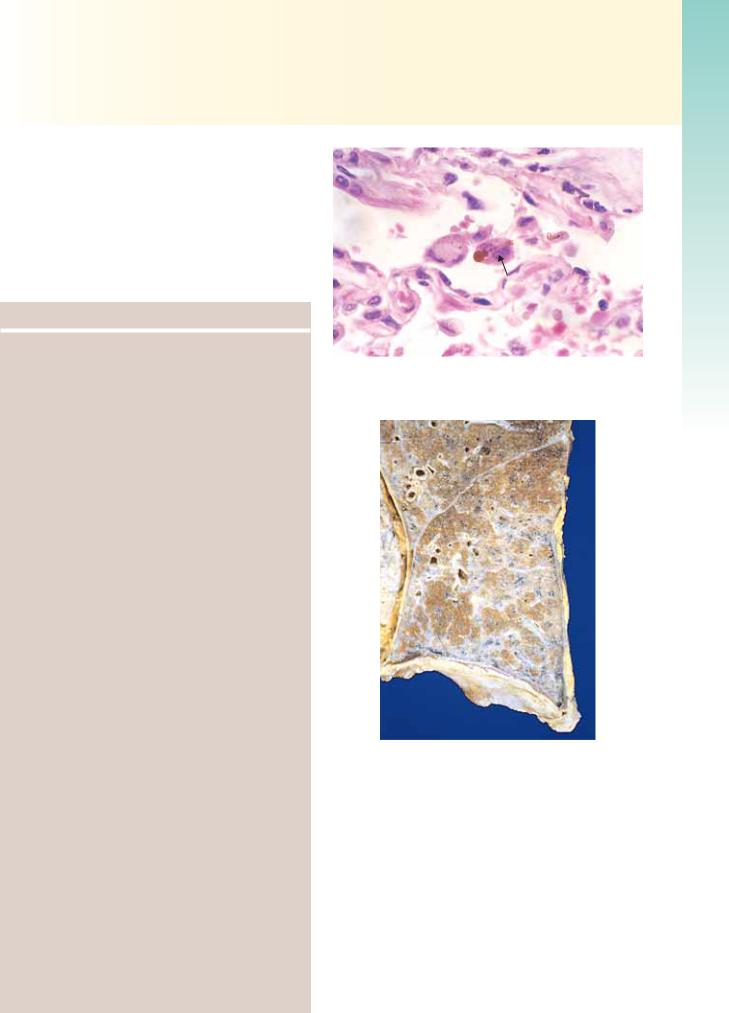
Рис. 13.19. Поверхность разреза легкого с распространенным силикозом. Фиброз привел к сморщиванию верхней доли легкого — имеет вид небольшой массы черного цвета (стрелка). Отмечается уплотнение и утолщение плевры. [С благодарностью Dr. John Godleski, Бригхэм и женский госпиталь, Бостон, Массачусетс.]
Рис. 13.20. Слияние силикотических узелков. [С благодарностью Dr. John Godleski, Бригхэм и женский госпиталь, Бостон, Массачусетс.]
лишь на поздних стадиях заболевания при развитии ПМФ. В это время болезнь может прогрессировать, даже если человек больше не контактирует с кварцем. У многих пациентов с ПМФ развивается легочная гипертензия и легочное сердце, возникающие вследствие хронической гипоксической вазоконстрикции и паренхиматозной дисфункции. Заболевание протекает длительно, но сниженная легочная функция может значительно ограничить активность больного.
При силикозе отмечают увеличение восприимчивости к туберкулезу. Постулируют, что силикоз приводит
к депрессии клеточного иммунитета, и кристаллы кварца могут подавлять способность легочных макрофагов фагоцитировать и нейтрализовать микобактерии. В силикотуберкулезных узелках часто выявляют центрально расположенную зону казеозного некроза. Взаимосвязь между кварцем и раком легкого ранее считали спорной, но в Международном агентстве исследования рака (1997) кристаллический кварц определили как один из самых канцерогенных профессиональных факторов для человека; и хотя этот факт подтвердили в нескольких эпидемиологических исследованиях, данный вопрос в настоящее время считают открытым.
Асбестоз и болезни, связанные с асбестом
Асбест — семейство кристаллических гидратировавших силикатов с волокнистой геометрией. По данным эпидемиологических исследований, профессиональное воздействие асбеста связано с развитием интерстициального фиброза паренхимы легких (асбестоз), ограниченных фиброзных бляшек или, реже, диффузного фиброза плевры, плевральных выпотов, бронхогенной карциномы, злокачественной мезотелиомы плевры и брюшины, карциномы гортани. Увеличенный риск раковых образований, связанных с асбестом, у членов семей рабочих, имеющих контакт с асбестом, доказывает потенциальную опасность асбеста в окружающей среде.
Патогенез. Концентрация, размер, форма и растворимость различных видов асбеста определяют возможность развития болезни. Существуют два различных типа асбеста: серпентин (с вьющимся и гибким волокном) и амфибол (имеющий прямое, жесткое и ломкое волокно). Существует несколько подтипов вьющихся и прямых волокон асбеста. Серпентин хризотил составляет большую часть асбеста, используемого в промышленности. Амфиболы, даже при их меньшей распространенности, представляют большую опасность, чем хризотил; однако оба типа могут стать причиной асбестоза, рака легкого и мезотелиомы. Большая патогенность прямых и жестких амфиболов, очевидно, связана с их структурой. Серпентиновые хризотилы, имеющие более гибкую, завитую структуру, вероятно, оседают в верхних дыхательных путях
иудаляются при помощи мукоцилиарного клиренса. Частицы, оседающие в легких, постепенно выщелачиваются из тканей, так как являются более растворимыми, чем амфиболы. Напротив, прямые и жесткие амфиболы попадают в глубжележащую ткань легких, где они могут проникнуть через эпителиальный пласт клеток в интерстиций. Несмотря на эти различия, обе формы асбеста считают фиброгенными, а увеличение экспозиции любого из них связывают с более высоким уровнем заболеваемости любыми связанными с асбестом болезнями. Асбестоз, как и другие пневмокониозы, вызывает фиброз, взаимодействуя с макрофагами легкого.
В дополнение к клеточным и фиброзным реакциям легкого, асбест, вероятно, также функционирует
икак инициатор, и как промотор опухолевого роста.
Некоторые из канцерогенных эффектов асбеста на мезотелий осуществляются реактивными свобод-
ными радикалами, генерируемыми волокнами асбеста (локализуются преимущественно в отдаленных от центра участках легкого, ближе к мезотелиальному покрову). Определенный вклад вносят и потенциально токсичные химикаты, адсорбированные на волокнах асбеста. Например, адсорбция канцерогенных веществ табачного дыма на волокнах асбеста имеет значение для известного синергичного эффекта курения на развитие бронхогенной карциномы у рабочих, контактирующих с асбестом.
Морфология
Асбестоз характеризуется развитием диффузного интерстициального фиброза легких. Эти изменения неотличимы от возникающих вследствие других причин, за исключением наличия асбестовых телец (имеют вид золотисто-коричневых, веретенообразных структур или «украшенных бусами» прутиков с прозрачным центром). Они состоят из волокон асбеста, покрытых содержащим железо белковым материалом (рис. 13.21). Асбестовые тельца, очевидно, образуются при попытке макрофагов фагоцитировать волокна асбеста; железо на тельцах представлено ферритином макрофагального происхождения. Асбестовые тельца иногда обнаруживают в легких здоровых людей (их обычно намного меньше), но без сопутствующего интерстициального фиброза.
В отличие от ПУРШ и силикоза, асбестоз начинается в нижних долях легких и в субплевральных отделах, средняя и верхние доли легких вовлекаются в патологический процесс при прогрессировании фиброза. Контракция фиброзной ткани нарушает нормальную архитектуру, приводит к возникновению сотового легкого с расширенными, заполненными воздухом структурами с утолщенными фиброзными стенками. Одновременно висцеральная плевра подвергается фиброзированию и утолщению, что может приводить иногда к сращению со стенкой грудной клетки. Фиброзирование иногда приводит к замуровыванию мелких веточек легочной артерии и артериол, вызывая легочную гипертензию и легочное сердце.
Плевральные бляшки — самый распространенный признак поражения плевры при контакте с асбестом — представлены хорошо отграниченными образованиями из грубого коллагена (рис. 13.22), часто содержащими кальций. Они образуются наиболее часто на передней и заднебоковой поверхности париетальной плевры и в области купола диафрагмы, не содержат асбестовых телец (только в редких случаях их обнаруживают у людей, не имевших контакта с асбестом). Редко экспозиция асбеста вызывает плевральные выпоты, которые обычно носят серозный характер (иногда диагностируют геморрагические выпоты). Редко возникает распространенный диффузный фиброз плевры, в запущенных случаях иногда приводящий к припаиванию легкого к стенке грудной клетки.
ГЛАВА 13. Легкие 599
Рис. 13.21. Асбестовое тельце (при большом увеличении). Имеет вид типичной структуры, напоминающей бусину, с головками на концах (стрелка)
Рис. 13.22. Асбестоз. Значительно утолщенная висцеральная плевра в области латеральной и диафрагмальной поверхности легкого. Обратите внимание на диффузный интерстициальный фиброз нижней доли легкого
Клинические проявления. Клинические симптомы при в асбестозе неотличимы от таковых при любом другом диффузном интерстициальном заболевании легкого. Как правило, прогрессирует одышка (возникает спустя 10–20 лет после экспозиции асбеста). Одышка обычно сопровождается продуктивным кашлем. Болезнь может протекать в легкой форме или прогрессировать до развития хронической сердечной недостаточности и легочного сердца, а также приводить к гибели пациента. Плевральные бляшки обычно бессимптомны; их обнаруживают на рентгенограммах (имеют вид ограниченных уплотнений). Как бронхогенные карциномы, так и злокачественные мезотелиомы

600 ГЛАВА 13. Легкие
развиваются у рабочих, контактировавших с асбестом.
Риск бронхогенной карциномы увеличен в 5 раз у рабочих, имевших контакт с асбестом; относительный риск развития мезотелиомы — очень редкой опухоли (заболеваемость составляет 2–17 случаев на 1 млн человек) — повышен более чем в 1000 раз. Мезотелиомы плевры и брюшины ассоциированы с экспозицией асбеста. Сопутствующее курение сигарет значительно увеличивает риск бронхогенной карциномы, но не влияет на частоту развития мезотелиом. Злокачественные опухоли легкого или плевры, связанные с асбестом, характеризуются крайне плохим прогнозом.
ЗАКЛЮЧЕНИЕ
•Пневмокониозы — группа хронических фиброзирующих заболеваний легкого, возникающих
врезультате контакта с органическими и неорганическими макрочастицами, обычно пыли минерального происхождения.
•Альвеолярные макрофаги легкого играют центральную роль в патогенезе повреждения легкого, поддерживая воспаление и генерируя реактивные кислородные радикалы и фиброгенные цитокины.
•Болезни, вызванные угольной пылью, включают бессимптомно протекающий антракоз, простой пневмокониоз (угольные пятна или узелки и центрилобулярная эмфизема), прогрессирующий массивный фиброз (проявляется растущей легочной дисфункцией, легочной гипертензией и легочным сердцем).
•Силикоз — самый распространенный пневмокониоз в мире — развивается при контакте с кристаллическим кремнием (например, кварцем).
•Проявления силикоза варьируют от бессимптомных силикотических узелков до массивного
легочного цирроза; у людей с силикозом существует также повышенная восприимчивость к туберкулезу. Отношения между экспозицией кварца и развитием рака легкого спорны.
•Волокна асбеста существуют в виде двух форм: амфиболы обладают более выраженным фиброгенным и канцерогенным воздействием, чем серпентины.
•Экспозиция асбеста связана с развитием следующих шести видов патологических процессов
влегких: парехиматозно-интерстициального фиброза в легких (асбестоза), фиброза плевры
(имеющего вид фиброзных бляшек или, реже, диффузного фиброза плевры), плевральных выпотов, рака легкого, злокачественных мезотелиом плевры и брюшины, рака гортани.
•Курение сигарет увеличивает риск развития рака легкого при экспозиции асбеста; кроме того, даже члены семей рабочих, контактирующих с асбестом, имеют повышенный риск развития рака.
Болезни легких, вызванные лекарственными препарата-
ми и радиацией
Лекарственные средства могут вызывать множественные острые и хронические изменения структуры
ифункций дыхательной системы. Например, блеомицин (противораковый препарат) вызывает пневмонит
иинтерстициальный фиброз в результате прямой токсичности и путем стимуляции притока воспалительных клеток в альвеолы. Точно так же амидарон (антиаритмический препарат) индуцирует пневмонит и легочный фиброз. Радиационный пневмонит — известное
ираспространенное осложнение лучевой терапии рака легкого и других опухолей грудной клетки. Острый радиационный пневмонит развивается обычно спустя 1–6 мес после лучевой терапии в среднем у 20% пациентов
ипроявляется лихорадкой, одышкой (выраженность ее пропорциональна объему облученного легкого), экссудативным плевритом и легочными инфильтратами в зонах радиационного воздействия. Данные симптомы могут исчезать при назначении глюкокортикоидов или прогрессировать в хронический радиационный пневмонит с развитием легочного фиброза.
Гранулематозные болезни
Саркоидоз
Хотя в настоящей главе саркоидоз рассмотрен как пример рестриктивного заболевания легких, следует помнить, что это мультисистемная болезнь неизвестной этиологии, характеризующаяся неказеифицирующимися гранулемами во многих тканях и органах. Другие заболевания, включая микобактериальные или грибковые инфекции и бериллиоз, также иногда приводят к развитию неказеифицирующихся гранулем; поэтому гистологический диагноз саркоидоза ставят путем исключения другой патологии. Хотя мультисистемные проявления саркоидоза нередко представлены разнообразными клиническими симптомами, однако двустороннее увеличение лимфатических узлов ворот легкого или поражение легкого (или обоих легких), видимое на рентгенограммах грудной клетки, служит главным диагностическим признаком в большинстве случаев. Изменения глаз и кожи отмечают приблизительно в 2% случаев (иногда представляют основные симптомы болезни).
Эпидемиология. Саркоидоз распространен во всем мире среди людей обоего пола, всех рас и возрастов. Однако выявляют определенные интересные эпидемиологические тенденции.
• Как правило, болеют взрослые не старше 40 лет.
• Высокий уровень заболеваемости регистрируют
вДании и Швеции, а также у афроамериканцев
вСША (распространенность саркоидоза в 10 раз превышает таковую у белокожих американцев).
•Саркоидоз — одно из немногих легочных заболеваний, имеющих более высокую распространенность среди некурящих лиц.
Этиология и патогенез. Хотя этиология саркоидоза в настоящее время неизвестна, однако существуют некоторые факты, позволяющие предположить, что эта болезнь служит признаком нарушенной регуляции иммунного ответа у людей, имеющих генетическую

предрасположенность и подвергнутых воздействию определенных агентов окружающей среды. Роль каждого из трех перечисленных составляющих рассмотрена ниже.
Для саркоидоза характерен целый ряд иммунных нарушений, позволяющих думать о развитии клеточноопосредованного иммунного ответа на неустановленный антиген с участием CD4+ T-хелперов. Характерны следующие изменения.
•Внутриальвеолярное и интерстициальное накопление CD4+ TH1-лимфоцитов.
•Моноклональная экспансия T-клеток (определена при анализе реаранжирования T-клеточных рецепторов).
•Увеличение содержания цитокинов TH1-клеточного происхождения, таких как ИЛ-2 и IFN-γ, вызывающих экспансию T-лимфоцитов и активацию макрофагов соответственно.
•Увеличение содержания ряда цитокинов в тканях (ИЛ-8, ФНО, воспалительного белка макрофагов 1α), усиливающих миграцию дополнительных T-клеток и моноцитов и способствующих формированию гранулем.
•Анэргия при обычных кожных тестах на такие антигены, как Candida или дериват очищенного протеина (возможно, из-за накопления CD4+ T-клеток в легочной ткани и возникающего впоследствии периферического истощения).
•Поликлоновая гипергаммаглобулинемия (другое
проявление TH-клеточной дисрегуляции).
• Генетическая предрасположенность у пациентов
ссаркоидозом подтверждается развитием заболевания в семейных и расовых группах, а также связью
сопределенным человеческим лейкоцитарным антигеном (HLA) и генотипами (например, класс I HLAA1 и HLA-B8).
Наконец, несколько предполагаемых антигенов считают провоцирующими саркоидоз (например, вирусы, микобактерии, боррелии, пыльца), но до сих пор
не существует никакого точного свидетельства инфекционной природы саркоидоза.
Морфология
Непременным морфологическим признаком саркоидоза считают наличие неказеифицирующейся эпителиоидно-клеточной гранулемы, независимо от вовлеченного органа (рис. 13.23). Гранулема представляет дискретное скопление эпителиоидных клеток, окруженных зоной, состоящей в значительной степени из CD4+ T-клеток. Эпителиоидные клетки имеют макрофагальное происхождение и характеризуются наличием развитой эозинофильной цитоплазмы и везикулярными ядрами. Нередко в гранулемах обнаруживают многоядерные гигантские клетки, образованные в результате слияния макрофагов. По периферии гранулемы визуализируют узкий слой фибробластов; со временем фибробласты пролиферируют, а откладывающийся коллаген
ГЛАВА 13. Легкие 601
Рис. 13.23. Типичные неказеифицирующиеся саркоидные гранулемы в легком с множеством гигантских клеток. [Любезно предоставлен Dr. Ramon Blanco, Department of Pathology, Brigham and Women's Hospital, Boston, Massachusetts.]
замещает гранулемы с формированием гиалинизированного рубчика. В гранулемах иногда обнаруживают две другие структуры: тельца Шумана (слоистые образования, состоящие из кальция и белков)
иастероидные тельца (звездообразные включения цитоплазмы гигантских клеток). Наличие их не требуется для постановки диагноза саркоидоза; их иногда выявляют в гранулемах другого происхождения. Редко в саркоидных гранулемах могут присутствовать очаги центрального некроза, что позволяет предположить инфекционный характер процесса. Типичный для туберкулеза казеозный некроз отсутствует.
На определенных стадиях болезни легкие поражаются у 90% пациентов. Гранулемы чаще располагаются в интерстиции, нежели в воздухоносных путях. Характерна тенденция к локализации в соединительной ткани вокруг бронхиол, легочных венул
ив плевре (распределение обусловлено развивающимся лимфангитом). В бронхиолоальвеолярной лаважной жидкости содержится большое количество CD4+ T-клеток. У 5–15% пациентов гранулематозные изменения в конечном счете заканчиваются развитием диффузного интерстициального фиброза
исотового легкого.
Внутригрудные лимфатические узлы ворот легкого и паратрахеальные лимфатические узлы вовлекаются в патологический процесс в 75–90% случаев, в то время как у трети пациентов диагностируют периферическую лимфаденопатию. Характерно отсутствие болезненности лимфатических узлов; они имеют плотноэластическую консистенцию. В отличие от туберкулеза, при саркоидозе лимфатические узлы не спаяны между собой и не содержат очагов некроза.
Поражение кожи выявляют приблизительно у 25% больных. Узловая эритема — признак острого саркоидоза — представлена возвышающимися красными

602 ГЛАВА 13. Легкие
мягкими узелками на коже передней поверхности ног. Саркоидные гранулемы не характерны для этих узелков. Напротив, дискретные безболезненные подкожные узлы (также могут возникать при саркоидозе) содержат множество неказеифицирующихся саркоидных гранулем. Другим характерным поражением кожи при саркоидозе служат плотные бляшковидные очаги с фиолетовым оттенком в области носа, щек и губ (lupus pernio — ознобленная волчанка). Поражение глаз и слезных желез возникает приблизительно у 20–50% пациентов. Патология глаз выражается в воспалении радужной оболочки или в виде иридоциклита (и может быть односторонней или двусторонней). Как следствие происходит помутнение роговицы, развивается глаукома
и(реже) полная потеря зрения. Поражается также
изадний увеальный тракт, в результате возникают
хориоидит, ретинит и неврит зрительного нерва. Зачастую данные патологические процессы сопровождаются воспалением слезных желез с подавлением слезообразования и развитием сухого синдрома. Односторонний или двусторонний паротит с увеличением и болезненностью околоушных желез диагностируют менее чем у 10% больных саркоидозом; в некоторых случаях развивается ксеростомия (сухость во рту). Сочетанное поражение глаз и околоушной слюнной железы (увеопаротит) называют
синдромом Mикулича.
Селезенка не всегда вовлекается в патологический процесс, но содержит гранулемы приблизительно в 70–75% случаев. Приблизительно у 10% больных отмечают увеличение селезенки. В печени при микроскопическом исследовании обнаруживают гранулемы (так же часто, как и в селезенке), локализованные обычно в портальных трактах, но только приблизительно у трети пациентов диагностируют гепатомегалию или нарушение функций печени. Поражение костного мозга (редко вызывает серьезную симпоматику) при саркоидозе обнаруживают примерно у 40% больных. Иногда регистрируют гиперкальциемию и гиперкальциурию, которые не связаны с разрушением с костей, а скорее вызваны увеличенным поглощением кальция вследствие образования активной формы витамина D мононуклеарными фагоцитами гранулем.
Клинические проявления. У многих людей заболевание протекает бессимптомно; его обнаруживают случайно как двустороннюю лимфаденопатию ворот легкого при обычном радиологическом обследовании или на аутопсии. В других случаях периферическая лимфаденопатия, поражения кожи и глаз, а также спленомегалия и гепатомегалия могут иметь клинические симптомы. Приблизительно в 60–70% симптомных случаях отмечают постепенное развитие респираторной симптоматики (одышка, сухой кашель и/или неопределенный дискомфорт за грудиной) или общих проявлений (лихорадка, утомляемость, потеря веса, анорексия, вечерние поты). Из-за отсут-
ствия характерных диагностических клинических признаков прибегают к биопсии легкого или лимфатических узлов. Выявление неказеифицирующейся гранулемы служит признаком, позволяющим заподозрить саркоидоз, но для постановки диагноза необходимо исключить другие причины гранулематозного воспаления.
Саркоидоз отличается непредсказуемым течением, характеризуется или прогрессирующим хроническим течением, или чередованием периодов активности
иремиссии. Ремиссии происходят постоянно и возникают самопроизвольно или при приеме глюкокортикоидов. В целом от 65 до 70% заболевших выздоравливают с минимальными остаточными проявлениями или без них. У 20% пациентов развивается постоянная дисфункция легких или происходит клиническое ухудшение. У большинства остальных 10–15% пациентов возникает прогрессивный легочный фиброз
илегочное сердце.
ЗАКЛЮЧЕНИЕ
•Саркоидоз — системное заболевание неустановленной этиологии; характерным морфологическим проявлением служат неказеифицирующиеся гранулемы, расположенные в различных тканях.
•Иммунопатология включает высокое содержание в легочной ткани CD4+ T-лимфоцитов,
которые локально секретируют TH1-зависимые цитокины (например, IFN-γ и ИЛ-2).
•Клинические симптомы включают увеличение лимфатических узлов, патологию глаз (синдром сухого глаза, воспаление радужной оболочки — иридоциклит), повреждения кожи (узловая эритема, ознобленная волчанка), висцеральные нарушения (в печени, селезенке, костном мозге). Поражение легких диагностируют в 90% случаев, при этом формируются гранулемы и интерстициальный фиброз.
Пневмонит гиперчувствительности
Пневмонит гиперчувствительности — воспалительное заболевание легкого с иммунным патогенезом; в патологический процесс, прежде всего, вовлекаются альвеолы. Именно поэтому болезнь часто называют аллергическим альвеолитом. Как правило, эта профессиональная болезнь развивается вследствие повышенной чувствительности к вдыхаемым антигенам, таким как заплесневелое сено (табл. 13.5). В отличие от бронхиальной астмы, при которой бронхи представляют основную мишень иммунного повреждения ткани, для пневмонита гиперчувствительности характерно иммунное повреждение на уровне альвеол.
Следовательно, пневмонит относят к рестриктивным заболеваниям легкого со снижением диффузионной способности и эластичности и уменьшением жизненной емкости легкого. Профессиональные агенты разнообразны, но синдромы имеют общие клинические и патологические проявления и, вероятно, сходный патогенез. Существуют доказательства, свидетельству-

|
|
|
ГЛАВА 13. Легкие 603 |
|
|
|
|
Таблица 13.5. |
Избранные причины пневмонита гиперчувствительности |
|
|
|
|
|
|
Синдром |
Причинный фактор |
Антигены |
|
Грибковые и бактериальные антигены |
|
|
|
|
|
|
|
Легкое фермера |
Заплесневелое сено |
Micropolyspora faeni |
|
Багассоз |
Заплесневелая выжатая сахарная |
Теплолюбивые актиномицеты |
|
|
|
свекла (выжимки) |
|
Легкое производителей кленового |
Заплесневелая кора клена |
Cryptostroma corticale |
|
сиропа |
|
|
|
Легкое работника, работающего |
Увлажнитель воздуха, |
Теплолюбивые актиномицеты, |
|
в условиях повышенной влажности |
прохладный туман |
Aureobasidium pullulans |
|
Легкое производителя солода |
Заплесневелый ячмень |
Aspergillus clavatus |
|
Легкое производителей сыра |
Заплесневелый сыр |
Penicillium casei |
|
Антигены насекомых |
|
|
|
Легкое мельника |
Загрязненное пылью зерно |
Sitophilus granarius (долгоносик |
|
|
|
|
пшеницы) |
Животные антигены |
|
|
|
Болезнь любителя голубей |
Голуби |
Белки сыворотки голубя в составе |
|
|
|
|
помета |
Химикаты |
|
|
|
Легкие работников химической |
Химическая промышленность |
Тримеиллированный ангидрид, |
|
промышленности |
|
изоцианаты |
|
ющие об иммунных механизмах развития пневмонита гиперчувствительности.
•При исследовании бронхиолоальвеолярного лаважа постоянно отмечают увеличенное количество CD4+ и CD8+ T-лимфоцитов.
•У большинства людей с пневмонитом гиперчувствительности обнаруживают преципитирующие специфические антитела в сыворотке крови; кроме того, с помощью метода иммунофлуоресценции выявляют комплемент и иммуноглобулины в стенках сосудов (это указывает на развитие процесса по механизмам гиперчувствительности III типа). Наличие неказеифицирующихся гранулем у 60–70% больных сви-
детельствует о развитии гиперчувствительности IV типа против соответствующего антигена.
Резюмируя вышеизложенное, следует заключить, что пневмонит гиперчувствительности возникает в результате иммунного ответа на внешний антиген с развитием реакций гиперчувствительности иммунокомплексного и замедленного типов.
Морфология
Морфология острых и хронических форм пневмонита гиперчувствительности характеризуется развитием очаговых неоднородных клеточных инфильтратов в легочном интерстиции, преимущественно в перибронхиальной ткани. Лимфоциты преобладают, но присутствуют также плазматические и эпителиоидные клетки. При острых формах болез-
ни также иногда выявляют примесь нейтрофилов. Неказеифицирующиеся гранулемы обычно образуются в интерстициальной перибронхиальной ткани более чем 65–70% больных. В распространенных, хронических, случаях развивается интерстициальный фиброз.
Клинические проявления. Пневмонит гиперчувствительности может иметь симптомы как острого заболевания (с лихорадкой, кашлем, одышкой и общими жалобами, возникающими спустя 4–8 ч после воздействия причинного фактора), так и хронической болезни (с постепенно прогрессирующими кашлем, одышкой, слабостью и снижением массы тела). Диагноз острой формы пневмонита, как правило, очевиден из-за короткого временного интервала между экспозицией антигена и развитием заболевания. В случае полного прекращения контакта с антигеном после развития острого заболевания легочные симптомы исчезают в течение нескольких дней. Неудачные попытки прекратить контакт с антигеном в конечном счете приводят к развитию хронического интерстициального заболевания легких, протекающего без видимых обострений при повторной экспозиции антигена.
Легочная эозинофилия
Легочная эозинофилия — группа легочных заболеваний, характеризующихся определенными клиническими и морфологическими проявлениями, включающими образование эозинофильных инфильтратов и активацию эозинофилов с увеличением уровня аль-

604 ГЛАВА 13. Легкие
веолярного ИЛ-5. Данные заболевания в целом имеют иммунный патогенез и полностью неустановленную этиологию. Легочные эозинофилии классифицируют на следующие группы.
•Острая эозинофильная пневмония с дыхательной недостаточностью — характеризуется быстрым развитием лихорадки, одышки, гипоксии и образованием разбросанных легочных инфильтратов (выявляемых при рентгенографии грудной клетки). В бронхиолоальвеолярной лаважной жидкости обнаруживают более 25% эозинофилов. Характерен быстрый ответ на применение глюкокортикоидов.
•Простая легочная эозинофилия (синдром Леффлера) — характеризуется «летучими» легочными инфильтратами, эозинофилией крови и благоприятным клиническим течением. Альвеолярные перегородки утолщены за счет инфильтрации эозинофилами
иединичными гигантскими клетками.
•Тропическая эозинофилия — вызывается филляриями
ипаразитами.
•Вторичная эозинофилия — развивается вторично при других аллергических заболеваниях, таких как бронхиальная астма, лекарственные аллергии, некоторые формы васкулитов.
•Идиопатическая хроническая эозинофильная пневмония — характеризуется образованием интерстициальных инфильтратов (из лимфоцитов и эозинофилов) и экссудата в просвете альвеол (обычно в периферических областях легкого). Заболевание сопровождается высокой лихорадкой, вечерними потами и одышкой. Диагноз устанавливают методом исключения (при отсутствии других форм легочных эозинофилий).
Интерстициальные болезни легких, связанные с курением
Роль курения сигарет в развитии обструктивных заболеваний легкого (эмфиземы и хронического бронхита) обсуждалась ранее. Курение также связано с возникновением рестриктивных или интерстициальных болезней легкого. Десквамативная интерстициальная пневмония (ДИП) и респираторный бронхиолит служат примерами двух интерстициальных заболеваний, связанных с курением. Самая поразительная гистологическая особенность ДИП — накопление в воздухоносных путях большого количества макрофагов (рис. 13.24) с развитой цитоплазмой, содержащей коричневый пигмент (макрофаги курильщика). Альвеолярные перегородки утолщены за счет редких воспалительных инфильтратов (обычно лимфоцитарных) и незначительно выраженного интерстициального фиброза. Легочные функции обычно свидетельствуют об умеренной рестрикции, для больных ДИП типичен хороший прогноз с превосходным ответом на терапию глюкокортикоидами и при прекращении курения.
Респираторный бронхиолит — распространенная патология легких, выявляемая морфологически у курильщиков, — характеризуется скоплением пигментированных макрофагов (аналогичных выявляемым при ДИП клеткам) с преимущественно бронхиолоцентрической
Рис. 13.24. Десквамативная интерстициальная пневмония (ДИП). При среднем увеличении в просветах альвеол визуализируются скопления большого количества альвеолярных макрофагов и небольшой фиброз альвеолярных перегородок
локализацией (в бронхиолах 1-го и 2-го порядка). Обнаруживают также умеренный перибронхиальный фиброз. Как и при ДИП, у пациентов отмечают постепенное начало одышки и сухого кашля, но симптомы прекращаются при отказе от курения.
БОЛЕЗНИ СОСУДИСТОГО ПРОИСХОЖДЕНИЯ
Легочная эмболия, кровоизлияния и инфаркт
Сгустки крови, обтурирующие крупные ветви легочной артерии, почти всегда представляют собой эмболы. Более чем в 95% случаев легочная эмболия возникает в результате тромбоза глубоких вен нижних конечностей, наиболее часто подколенных и расположенных выше крупных вен. Ежегодно в США тромбоэмболия становится причиной смерти приблизительно 50 000 людей. Даже когда нефатальная эмболия утяжеляет течение основного заболевания. Истинная частота нефатальной легочной эмболии неизвестна. Некоторые эмболии, несомненно, развиваются вне больницы у амбулаторных пациентов (и не имеют клинических проявлений). Даже среди госпитализированных пациентов легочную эмболию как причину смерти диагностируют в клинике только у 30–35% больных. По данным аутопсий, частота легочной эмболии варьирует в широких пределах от 1% в общем стационаре до 30% среди умерших после серьезных ожогов, травм или переломов. Факторы, предрасполагающие к развитию тромбоза вен нижних конечностей, представлены в главе 4; тем не менее следует еще раз вспомнить о таких факторах риска, как длительный постельный режим (особенно с иммобилизацией ног), хирургические операции (особенно ортопедические в области колена и бедра), серьезные травмы (включая ожоги и множественные переломы), застойная сердечная

недостаточность, предродовой или послеродовой период у женщин, а также прием противозачаточных таблеток с высоким содержанием эстрогенов, распространенный рак и первичные гиперкоагуляции (например, связанные с фактором V Лейдена) (см. главу 4).
Последствия легочной тромбоэмболии зависят в значительной степени от размера эмбола (который, в свою очередь, определяет размер обтурируемой ветви легочной артерии), а также от сердечно-легочного статуса пациента. Существуют два важных последствия эмболии легочной артерии: увеличение давления в легочной артерии в результате механической блокировки кровотока (возможно, из-за вазоспазма, возникающего за счет нейрогенных и /или цитокиновых механизмов, например, с участием тромбоксана A2 и серотонина) и ишемия легочной паренхимы, расположенной дистальнее места окклюзии. Таким образом, окклюзия крупных ветвей приводит к внезапному повышению давления в легочной артерии, уменьшению сердечного выброса, правосторонней сердечной недостаточности (острому легочному сердцу) или даже смерти. Следующие механизмы лежат в основе развития гипоксемии.
•Перфузия зоны ателектаза легких. Альвеолярный коллапс в зоне ишемии развивается в связи со снижением продукции сурфактанта и уменьшением движения грудной клетки из-за связанной с эмболией боли; кроме того, часть легочного кровотока минует гиповентилируемые области легкого.
•Уменьшение сердечного выброса вызывает усиление различий артериально-венозного насыщения кислородом.
•Шунтирование крови через незаращенное овальное окно (наблюдают у 30% здоровых людей).
•При окклюзии мелких веточек легочной артерии
последствия менее катастрофичны и протекают без клинической симптоматики.
Вспомните, что легкое оксигенируется не только легочными артериями, но также и бронхиальными артериями, и непосредственно из воздуха в альвеолах. При нормальной циркуляции по бронхиальным артериям и поддержании адекватной вентиляции прекращение кровотока в мелкой веточке легочной артерии не приводит к некрозу ткани. Действительно, ишемический некроз (инфаркт), вызванный легочной тромбоэмболией, является исключением, а не правилом (регистрируют только в 10% случаев при наличии сердечной недостаточности, нарушений циркуляции по бронхиальным артериям или при гиповентиляции части легкого в результате основной легочной болезни).
Морфология
Последствия легочной тромбоэмболии зависят от размера эмбола и общего состояния кровообращения. Большие крупные тромбоэмболы задерживаются и воздействуют на стенку ствола легочной артерии или ее главных ветвей, а также «садятся верхом» на область бифуркации как «эмбол-наездник» (рис. 13.25). Обычно смерть от гипоксии или острой
ГЛАВА 13. Легкие 605
Рис. 13.25. Крупный «тромбоэмбол-наездник» (расположенный в области бифуркации ствола легочной артерии), возникший вследствие тромбоза бедренной вены. [Любезно предоставлен д-р Linda Margraf, отдел патологии, Университет Техаса, Югозападная Военно-медицинская школа, Даллас, Техас.]
правожелудочковой недостаточности (острое легочное сердце) наступает так внезапно, что в легких не успевают развиться какие либо морфологические изменения.
Эмболы меньших размеров закупоривают просветы ветвей легочной артерии среднего и мелкого калибра. При достаточном кровообращении и хорошем кровотоке по бронхиальным артериям жизнеспособность легочной ткани сохраняется, однако в некоторых областях возникают легочные геморрагии с внутриальвеолярными скоплениями крови в результате ишемического повреждения эндотелиальных клеток. При наличии патологии сердечно-сосудистой системы, сопровождающейся сердечной недостаточностью с застойным венозным полнокровием легкого, эмболия мелких и средних ветвей легочной артерии приводит к развитию геморрагического инфаркта легкого. Чем большая территория легкого ишемизирована в результате окклюзии, тем более вероятно развитие инфаркта. Около 75% всех инфарктов локализуются в нижних долях легкого (более половины из них — множественные). Они имеют клиновидную форму с основанием, обращенным к плевре, и вершиной — к воротам легкого. Легочные инфаркты — типично геморрагические, на ранних стадиях имеют вид участков красно-синюшного цвета, выбухающих над поверхностью (рис. 13.26). Прилегающая плевра часто покрывается фибри-

606 ГЛАВА 13. Легкие
Рис. 13.26. Свежий маленький геморрагический инфаркт легкого клиновидной формы
нозными наложениями. Если удается обнаружить обтурированный тромбоэмболом сосуд, то он локализуется в области вершины инфаркта. Эритроциты в зоне инфаркта начинают разрушаться в течение 48 ч, и инфаркт бледнеет, в конечном счете приобретая красно-коричневую окраску за счет синтезируемого гемосидерина. Со временем по краям инфаркта происходит замещение некротических масс фиброзной тканью серо-белого цвета, что в итоге приводит к формированию постинфарктного рубца, который макроскопически имеет вид втяжения легочной ткани. Гистологическим признаком новых инфарктов служит наличие коагуляционного некроза альвеолярных перегородок в области кровоизлияния.
Клинические проявления. Легочная тромбоэмболия может иметь следующие клинические симптомы.
•В большинстве случаев (60–80%) легочная эмболия клинически бессимптомна, потому что тромбоэмболы малых размеров быстро деградируются путем фибринолиза, а бронхиальное кровообращение в этот период поддерживает жизнеспособность пораженной паренхимы легкого.
•В 5% случаев может произойти внезапная смерть, развиться острая правожелудочковая недостаточность (острое легочное сердце) или сердечнососудистый коллапс (шок) при обтурации более 60% всего легочного кровотока крупным эмболом или множественными, одновременно возникшими, мелкими эмболами. Массивная легочная эмболия — одна из немногих причин мгновенной смерти, зачастую наступающей прежде, чем у человека возникает боль в груди или одышка.
•Закупорка веточек легочной артерии относительно мелкого и среднего калибра (10–15% случаев), представляющих артерии концевого типа, приводит к развитию легочного инфаркта при наличии некоторой степени недостаточности кровообращения. Типичным клиническим симптомом инфаркта служит неожиданно возникшая, необъяснимая и кажущаяся беспричинной одышка.
•У некоторых людей (менее 3% случаев) рецидивирующая, многократно повторяющаяся тромбоэмболия приводит к легочной гипертензии, хронической правосторонней сердечной недостаточности (хроническому легочному сердцу) и со временем к легочному
сосудистому склерозу с тяжелой прогрессирующей одышкой.
Эмболы обычно резорбируются после начального острого периода. Они уменьшаются в размерах и в результате эндогенной фибринолитической активности могут лизироваться целиком. Однако при наличии предрасполагающих факторов маленький безобидный эмбол может превращаться в крупный, кроме того, у 30% пациентов, однажды испытавших однократную легочную эмболию, существует вероятность развития рецидива. Таким образом, диагностика и соответствующая профилактика тромбоэмболии имеют большое значение. Профилактическая терапия включает раннее вставание с постели после оперативных вмешательств и родов, ношение эластических чулок, использование интермиттирующей пневматической компрессии и выполнение изометрических упражнений для ног (для прикованных к постели пациентов). Антикоагулянтная терапия показана всем людям, входящим в состав группы высокого риска. Пациентам с легочной эмболией также назначают антикоагулянты. Пациенты с массивной легочной эмболией — кандидаты на тромболитическую терапию.
Кроме того, следует упомянуть нетромбические формы легочной эмболии, которые включают редкие, но потенциально смертельные формы: кессонную болезнь, жировую эмболию и эмболию околоплодными водами (см. главу 4). Внутривенное введение наркотиков часто сопровождается эмболией легочных микрососудов инородными телами; присутствие силиката магния (талька) во внутривенной смеси вызывает гранулематозный ответ в легочном интерстиции и в стенках легочной артерии. Вовлечение интерстиция может привести к легочному фиброзу, в то время как последний обусловливает возникновение легочной гипертензии. Кристаллы талька иногда обнаруживают в гранулемах (при помощи поляризационной микроскопии). Костномозговая эмболия (наличие гемопоэтических клеток и жировых включений в просвете сосудов малого круга кровообращения) может произойти в результате массивной травматизации, а также у пациентов с инфарктом кости, страдающих серповидно-клеточной анемией.
ЗАКЛЮЧЕНИЕ
Легочная эмболия
•Крупные тромботические массы в просветах легочной артерии имеют эмболическое происхождение (из тромбов, образованных в глубоких венах нижних конечностей).
•Факторы риска тромбоэмболии включают длительный постельный режим, хирургические операции (особенно ортопедические), серьезную травму, хроническую сердечную недо-

статочность, пероральные противозачаточные средства (особенно содержащие высокий уровень эстрогенов), распространенный рак и генетические болезни, сопровождающиеся гиперкоагуляцией.
•Большинство (60–80% случаев) эмболий протекают бессимптомно, приблизительно в 5% случаев служат причиной острого легочного сердца,
шока или смерти (типично наличие большого «тромбоэмбола-наездника»). В остальных случаях эмболии развивается инфаркт легкого.
•У пациентов, однажды испытавших легочную эмболию, существует вероятность развития
рецидива.
Легочная гипертензия
Малый круг кровообращения обладает низкой резистентностью, давление в легочной артерии составляет 1/8 системного. Легочная гипертензия (состояние, при котором давление в легочной артерии увеличивается и достигает 1/4 системного давления или более) чаще развивается вторично в связи с уменьшением общей площади поперечного сечения сосудов малого круга кровообращения или вследствие увеличения сопротивления легочному сосудистому кровотоку. Существует несколько причин вторичной легочной гипертензии.
•Хронические обструктивные или интерстициальные болезни легкого, которые сопровождаются деструкцией паренхимы легкого и возникающей в результате редукцией альвеолярных капилляров. Это вызывает
увеличение легочного артериального сопротивления и вторичное повышение артериального давления.
• Рецидивирующие легочные эмболии, приводящие к уменьшению общей площади поперечного сечения сосудов малого круга кровообращения, что, в свою очередь, вызывает увеличение сосудистого сопротивления.
•Болезни сердца, например митральный стеноз, при котором увеличивается давление в левом предсердии, приводя к повышению давления в легочных венах и, в конечном итоге, к развитию легочной артериальной гипертензии. Врожденный порок с шунтированием крови слева направо — другая причина
вторичной легочной гипертензии.
В редких случаях, когда легочная гипертензия не связана ни с одной из перечисленных причин, ее называют первичной или идиопатической. Подавляющее большинство таких случаев носят спорадический характер, и только у 6% пациентов диагностируют семейную форму с аутосомно-доминантным типом наследования.
Патогенез. Согласно современным представлениям,
дисфункция легочного эндотелия и/или гладкомышечных клеток служит вероятной причиной большинства форм легочной гипертензии.
•При вторичной легочной гипертензии эндотелиальная дисфункция развивается как результат основ-
ГЛАВА 13. Легкие 607
ного заболевания (например, слущивание и механическое повреждение клеток из-за увеличенного кровотока, возникшего из-за шунтирования кровотока слева направо, или биохимического повреждения, вызванного фибрином при рецидивирующей тромбоэмболии). Дисфункция эндотелия приводит
куменьшению синтеза вазодилатирующих агентов (например, оксида азота, простациклина), увеличению продукции вазоконстрикторных медиаторов (таких как эндотелин). Кроме того, происходит увеличение образования факторов роста и цитокинов, которые вызывают миграцию и репликацию сосудистых гладкомышечных клеток и выработку внеклеточного матрикса.
•При первичной легочной гипертензии, особенно редкой
семейной ее форме, ТФР-β-сигнальный путь активируется как ключевой посредник между эндотелиальной и гладкомышечной дисфункцией. В 50% случаев семейной легочной гипертензии обнаруживают специфические мутации рецептора белка морфогенеза костного мозга 2-го типа (BMPR2), выявляемые на уровне герминативных клеток. BMPR2 (относят
кповерхностным клеточным молекулам) взаимодействует со многими лигандами TGF-β-сигнального пути. Продукт гена BMPR2 — ингибитор пролиферации, следовательно, мутации приводят к потере функции этого гена и патологической пролиферации эндотелия и гладкомышечных клеток сосудов. Пролиферация эндотелия в этих случаях — моноклональная, что подтверждает генетическое происхождение заболевания. Не у всех людей с мутациями BMPR2 развивается первичная легочная гипертензия; этот факт позволяет предположить наличие генов-модификаторов, вероятно, затрагивающих пенетрацию данного специфического фенотипа.
•Исследования спорадических форм первичной легочной гипертензии свидетельствуют также о возможной роли гена транспорта серотонина (5-HTT). При добавлении серотонина или сыворотки к гладкомышечным клеткам легкого некоторых больных с первичной легочной гипертензией усиливается пролиферация этих клеток. Как предполагают, генетические полиморфизмы 5-HTT приводят к усилению его экспрессии, что стимулирует пролиферацию гладкомышечных клеток. Нарушение функции 5-HTT может также служить причиной легочной
гипертензии, диагностируемой у людей, принимающих фенфлюрамин (препарат против ожирения) или его производные.
Морфология
Сосудистые изменения при всех формах легочной гипертензии (первичной и вторичной) распространяютсянавсеартериальноедерево(рис.13.27)ивключают развитие атером в крупных ветвях (эластического типа) легочной артерии (подобных возникающим при системном атеросклерозе); пролиферацию гладкомышечных клеток интимы в артериях мышечного
