
хирургия 5 курс / книги / Savel'ev V.S. (red.) 80 lekcij po hirurgii (Litterra, 2008)(ru)(T)(K)(910s)(ISBN 9785982161190)
.pdfКритическая ишемия нижних конечностей
стопы у опытных специалистов в последние годы ста новится во многих случаях достаточным для принятия решений о методе реконструкции.
Вместе с тем рентгеноконтрастная ангиография остается золотым стандартом обследования больных с поражениями периферических артерий. В последние годы компьютерная и магнитно-резонансная томо графия существенно улучшили качество получаемого изображения сосудистого русла и могут быть полез ными при принятии решения о реваскуляризационной стратегии не только в отношении магистральных артерий конечности, но и артерий голени и стопы. Исследования, проводимые на диагностических аппа ратах последних поколений, дают результаты, конкури рующие с ангиографией.
Лечение
Лечение включает консервативную терапию, хирур гическую реваскуляризацию и эндоваскулярные вме шательства и, к сожалению, часто ампутацию. Главные задачи лечения КИНК— сохранение конечности, улучшение качества жизни и сокращение количества сердечно-сосудистых осложнений от атеросклероза — приходится решать в срочном порядке.
Все пациенты должны получать комплексное лече ние, включая антитромбоцитарную терапию, особенно в группе с высоким риском тромбоза стенозированных артерий. Ингибиторы АПФ следует применять для лече ния артериальной гипертензии и для уменьшения риска кардиоваскулярных осложнений. Интенсивная тера пия, направленная на понижение показателей липидов и контроль содержания глюкозы в крови, также очень важны. Дополнительное лечение трофической язвы, антибиотики и анальгетики служат непременными компонентами терапии КИНК. Если нарастает угроза ампутации, то необходима немедленная госпитализа ция, требуется назначение фракционированного или нефракционированного гепарина. В принятии решения о характере лечения больного с КИНК кроме сосудис того хирурга должны принимать участие терапевты, кардиологи, эндокринологи, врачи функциональной диагностики, анестезиологи-реаниматологи и другие специалисты.
Лечение пациента следует начинать сразу при пос туплении в хирургическое отделение. Если в процессе обследования выявляются гемодинамически значимые поражения других артериальных бассейнов— сон ных или коронарных артерий, необходимо предпри нять попытку первичной коронарной реваскуляризации или эндартерэктомии из сонной артерии. Возраст, как
правило, не может быть причиной отказа пациенту в операции.
Определение этапности выполнения оперативных вмешательств, а также наиболее оптимальный объем реваскуляризации конечности при генерализованном поражении артериальных бассейнов являются главны ми задачами современной реконструктивной хирургии сосудов. Все это определяет актуальность поиска мето дов, улучшающих результаты хирургического лечения.
При вмешательствах на артериях нижних конеч ностей чаще всего используется проводниковая анес тезия, втом числе эпидуральная, либо комбинация с общей анестезией. Предоперационная подготовка, помимо коррекции основных факторов риска, заключа ется в проведении внутривенной инфузионной терапии сопутствующей патологии и имеющихся обменных рас стройств.
При аорто-бедренных реконструкциях использу ют синтетические протезы. Выбор вида операции зави сит от одноили двухстороннего характера поражения подвздошных артерий. При двухсторонней протяжен ной окклюзии обеих подвздошных артерий выполня ется бифуркационное аорто-бедренное шунтирование. В случаях тяжелого состояния пациентов при КИНК воз можно и одностороннее шунтирование: в этих ситуа циях мы выполняем вмешательство из параректального внебрюшинного доступа под эпидуральной анестезией. Больных активизируем в тот же или на следующий день.
При противопоказаниях к аорто-бедренной реконст рукции выполняется и перекрестное подвздошно-бед- ренное, бедренно-бедренное или подключично-бед- ренное шунтирование. В случаях сочетанного пораже ния аорты, подвздошной и бедренной артерий пред почтительно выполнять одновременно шунтирование аорто-бедренно-подколенных сегментов.
При реконструктивных операциях на артериях ниже паховой складки в бедренно-подколенном, под- коленно-тибиальном сегментах вмешательство может включать профундопластику, бедренно-подколенное шунтирование и различные виды бедренно-тибиаль- ных вмешательств с использованием собственной вены больного, как в положении инверсии, так и in situ. Как правило, четкого контрастирования дистального арте риального русла достичь не удается, поэтому выпол няется интраоперационная ангиография или ревизия состояния сосудов во время вмешательства. Во всех случаях бедренно-подколенных реконструкций ниже щели коленного сустава, бедренно-берцовых и бедрен- но-стопных мы используем вену in situ. При заверше нии операции, как правило, проходимость дистального анастомоза проверяется выполнением интраопераци-
121
Сердечно-сосудистая хирургия
онной ангиографии, ангиоскопии или ультразвуковых методов исследования.
У больных с высоким риском осложнений или ухуд шением состояния из-за тяжести сопутствующей пато логии при наличии участка сосуда с ограниченной окклюзией или выраженным стенозом применяется щадящая методика эндартерэктомии.
Реконструктивные сосудистые операции — метод выбора в лечении больных с критической ишеми ей конечностей. У них возникает необходимость в «срочном» шунтировании окклюзированного сегмен та магистрального сосуда. Основной проблемой для хирурга служит определение достаточных путей оттока в зоне предполагаемой реконструктивной операции. Также следует отметить существенное влияние на успех подобных вмешательств квалификации и опыта сосудистого хирурга. По нашему мнению, их сложность соизмерима с операциями на коронарных или сонных артериях.
При невозможности выполнения реконструктивных операций на окклюзированных подколенной и берцо вых артериях возможно восстановление кровоснаб жения путем артериализации венозного русла стопы. При этом используется два вида вмешательства: артериализация поверхностной и артериализация глубокой венозных систем.
Принципиально новый вид операций при дистальном поражении артерий голени в условиях критической ишемии нижних конечностей был разработан и при менен в клинической практике сосудистым отделени ем Института хирургии им. А.В. Вишневского РАМН. Принцип операции заключается во включении в арте риальное русло венозной системы ишемизированной стопы через большую подкожную вену. Эффективность подобного вмешательства оказалась очень высокой, положительный результатдостигнуту 79% больныхтромбангиитом и 93% атеросклерозом. Лишь в 20% случаев пришлось выполнить «экономную» ампутацию на уровне стопы или пальцев. При явлениях гангрены либо разви тии тромбофлебита эта методика невыполнима.
Известно также много других способов прямых реконструкций с реверсированной веной, по мето дике in situ, с использованием разгрузочных артериовенозных фистул в зоне дистального анастомоза. Одновременно используются способы непрямых реваскуляризаций — реваскуляризирующая остеотрепанация, пересадка пряди большого сальника на ножке, различные другие виды артериализации.
В клиническую практику внедрен способ хирурги ческого лечения критической ишемии нижних конеч ностей при окклюзирующих поражениях артерий голе
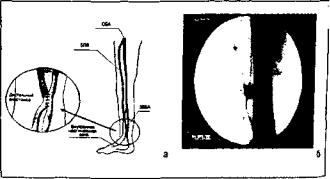
ни, когда дистальный анастомоз вены in situ накладыва ется с одной из артерий голени и одновременно сохра няется венозный сброс. Использование такого способа позволяет выполнять реконструктивные операции при полной окклюзии одной из артерий голени, а также при проксимальных окклюзиях обеих артерий голени и высоком периферическом сосудистом сопротивле нии. Наличие дополнительного сброса крови в вену за счет анастомоза «бок в бок» значительно снижает риск тромбоза реконструкции, существенно продлевает срок функционирования шунта (рис. 1). Исключаются ранние тромботические осложнения.
Восстановление кровоснабжения в дистальном артериальном русле при критической ишемии нижних конечностей подобным способом позволяет восстано вить артериальный кровоток у больных при неболь шой емкости дистального русла и высоком перифери ческом сопротивлении. Способ позволяет выполнить реконструктивную операцию с хорошим эффектом у подавляющего большинства больных в случаях неудов летворительных путей оттока, при окклюзиях артерий голени, несостоятельности дистального русла. При этом у больных восстанавливается кровообращение в ниж ней конечности, регрессируют ишемия и трофические расстройства. Использование данного способа позво ляет расширить контингент пациентов, подвергающихся сосудистой реконструкции, которые ранее считались бесперспективными.
К сожалению, применение различных способов реваскуляризации не всегда позволяет восстановить кровообращение в конечности. Это обстоятельство диктует поиск новых способов реконструктивных вме шательств у пациентов с дистальными окклюзиями артерий голени. У этой категории больных особо остро
Рис. 1. Способ хирургического лечения критической ише мии нижних конечностей: а — схема оперативного нхнчиательстна; б — ангпограмма, выполненная спустя IS месяцев мосле операции. Контрастнроиан дистальный артернот'- Hoam.in анастомоз с сохраненным сбросом в пену
Критическая ишемия нижних конечностей
стоит вопрос об окклюзии шунтов. Случаи тромбозов трансплантатов следует делить на ранние (до 1 месяца) и поздние (более 1 месяца) после хирургического вме шательства. Причины их самые разнообразные: во-пер вых, технические ошибки и погрешности выполнения операций, неадекватная оценка состояния дистального артериального русла, неправильный подбор шунта и прочее. При раннем тромбозе шунта целесообразно предпринять попытку ревизии анастомозов, тромбэктомии и исправления реконструкции.
Адекватное систематическое наблюдение больных после выполненных реконструктивных операций, конт роль функционирования шунта и состояния конечности, подбор препаратов для консервативной терапии — задачи ангиологов поликлиник. Обычно эти пациенты наблюдаются постоянно, посещая хирурга-ангиолога 3—4 раза в год, а при необходимости и чаще.
Консервативная терапия. Лечение с использова нием различных фармацевтических средств у больных с критической ишемией начинают с первых дней пре бывания больного в стационаре, независимо от того, будет выполняться хирургическая реконструкция или эндоваскулярное пособие.
К принятой схеме относится назначение дезагрегантных препаратов (иногда больные уже принимают эти препараты пожизненно по поводу церебральной или кардиальной ишемии), низкомолекулярных декстранов и пентоксифилина (трентала). При сахарном диабете и синдроме диабетической стопы эффективно назначе ние сулодексида (Вессел Дуэ Ф). К сожалению, следует констатировать, что сама по себе консервативная тера пия недостаточно эффективна при лечении критичес кой ишемии нижних конечностей в ближайшем и тем более отдаленном периоде. В этом плане определен ные надежды дает лечение вазапростаном, которое у больных с критической ишемией также целесообразно проводить в сочетании с хирургической реконструк цией. Обычно этот препарат начинают использовать в качестве предоперационной меры подготовки, а затем продолжают после выполнения оперативной реваскуляризации. Препарат наиболее эффективен при пора жении артерий голени. Длительность лечения — от 10 до 20 и более дней в дозе от 20 мкг до 80 мкг в сутки, которую вводят внутривенно разведенной в 200 мл физиологического раствора. Под влиянием лечения вазопростаном больные отмечают уменьшение болей, ускорение заживления трофических язв. Препарат при меняют и в случаях отказа больных от оперативного лечения при тромбозе трансплантата.
Консервативная терапия крайне важна после выпис ки больного из стационара: показан постоянный прием
препаратов ацетилсалициловой кислоты в дозе 50— 100 мг в сутки, пентоксифилин в дозе 1200 мг (может быть использован трентал-400 или вазонит-600 в такой же суммарной дозе) курсами в течение 2—3 месяцев 2 раза в год.
Ампутация конечности является необходимой при невозможности реваскуляризации, а также в случае обширного некроза тканей конечности. Она выпол няется только после осмотра больного сосудистым хирургом, в тех случаях, когда исчерпаны все воз можности спасения конечности. Вместе с тем ампута ция конечности — очень тяжелое вмешательство для пациентов преклонного возраста. Смертность в раннем послеоперационном периоде после ампутации нижней конечности до настоящего времени высокая — от 5 до 17%. До 10% больных после ампутаций, выполняемых выше коленного сустава и до 20%— ниже колена, нуждаются в дополнительном хирургическом лечении длительно незаживающих ран. Ампутация дает более высокую смертность у диабетиков. Последующая, как правило, в течение года после первой, ампутация про тивоположной нижней конечности наблюдается очень часто, более чем в 50% случаев.
Хирургическая реваскуляризация, как метод сохра нения конечности, — эффективная стратегия, она спо собна улучшить качество жизни у большинства паци ентов с КИНК. Такая операция очень часто связана с длительным восстановлением кровоснабжения конеч ности, потенциальной потерей подкожной вены (кото рая могла бы быть необходима в будущем для аортокоронарного шунтирования (АКШ)), хроническим отеком нижних конечностей и еще более худшей ситуацией, когда хирург терпит неудачу.
Осложнения, которые встречаются при выполнении шунтирования ниже паховой складки, могут иметь сле дующие возможные результаты: смертность — от 1,3 до 6%, острый инфаркт миокарда — от 1,9 до 3,4%, ране вые осложнения — от 10 до 30% и тромбоз вены — до 15%. Несмотря на успешный результат шунтирующих операций, ампутация все еще вынужденно выполняется в 10—40% случаев.
Новые технологии в лечении критической ишемии
Хроническая КИНК является результатом прогрес сирующего мультифокального атеросклероза сосудов нижних конечностей. Вовлечение большеберцовомалоберцовых сосудов встречается очень часто. КИНК приводит к ишемической боли покоя и прогрессирую щей потере тканей.
123
Сердечно-сосудистая хирургия
Золотым стандартом лечения КИНК на протяжении многих лет была хирургическая реваскуляризация, при чем протяженность шунтирования в последние годы достигла артерий голени и стопы. Между тем этот под ход возможен при условии хорошей проходимости дис тальном артериального русла конечности и отсутствии сопутствующей патологии. Недавнее рандомизирован ное исследование BASIL подвергло сомнению превос ходство хирургической реваскуляризации и подтверди ло преимущество лечебного эффекта тибио-перонеаль- ных интервенционных технологий у подобной группы больных. Эти результаты должны привести к техничес кому и технологическому прогрессу эндоваскулярных вмешательств на тибио-перонеальных сосудах.
Появление высококвалифицированных эндоваску лярных специалистов, которые способны лечить КИНК менее агрессивными способами, чем хирурги, позволяет надеяться на успех. Оптимальное использование малоинвазивного метода и мультидисциплинарный подход к лечению КИНК также существенно влияют на улучше ние результатов. Для клинического успеха необходимо восстановление «прямолинейного потока» в одной или более артерий голени. Улучшение проходимости лишь проксимального сегмента сосуда не всегда дает благо приятный результат, выраженное стенозирование в дис тальном сегменте артериального русла конечности или протяженная окклюзия не обеспечат адекватного кро воснабжения для заживления раны. Состояние артерий голени и дуги стопы очень важно, и для его оценки необ ходимо получение высококачественных ангиограмм.
Успех терапии оценивается облегчением боли в покое, заживлением язв и предотвращением ампута ции. Поскольку результат лечения КИНК в значитель ной степени связан с качеством жизни и, в частности, сохранением возможности ходьбы, являющейся наибо лее важным аспектом качества жизни, цель лечения КИНК— сохранение ноги. Увеличение потока крови в первую очередь необходимо для заживления ишемических язв и предотвращения прогрессирующего некроза тканей.
После реваскуляризации пациент должен иметь, по возможности, прямолинейный кровоток к стопе, и ЛПИ > 0,7 с давлением у лодыжек > 50 мм рт. ст. Комплексный, мультидисциплинарный подход к лечению пациента, включая сосудистого хирурга и кардиолога (вместе с эндоваскулярным специалистом), поможет в заживле нии раны. Эндоваскулярные подходы к лечению КИНК продемонстрировали успех в 92—96% случаев с трех летним сохранением конечности в 77—94%.
Результаты эндоваскулярного лечения, конечно, различны в зависимости от тяжести сопутствующей
патологии, протяженности стенозирующего пораже ния, сложности восстановительных манипуляций и т.д. Инновационные технологии, в настоящее время исполь зуемые для спасения конечности, включают лазерную атерэктомию, эксцизионную атерэктомию, криопластику, сокращающуюся баллонную ангиопластику, стентирование (стенты из «голого» металла, баллон-рас ширяющиеся, саморасширяющиеся и с лекарственным покрытием). Частота спасения конечности с использо ванием лазерной и дополнительной медикаментозной терапии многообещающие. Покрытые гепарином малого диаметра баллон-расширяющиеся стенты используются для лечения тибиальных окклюзии с хорошими резуль татами. Многочисленные результаты исследования продемонстрировали, что в сравнении с традицион ным шунтированием эндоваскулярный подход к лече нию КИНК имеет сопоставимые результаты и немалую надежду на успех лечения.
Показания. Недавно опубликованное исследование BASIL продемонстрировало б-месячное выживание без ампутации у пациентов с КИНК, пролеченных реваскуляризацией ниже щели коленного сустава. Начальная стратегия — попытки эндоваскулярной реваскуляри зации с тем, чтобы избавить пациента от хирургичес кой реваскуляризации. Возможно, интервенционные технологии тибио-перонеальных сосудов должны быть методом выбора лечения КИНК, особенно на начальных этапах лечения ишемии, вызванной окклюзией сосу дов ниже подколенной артерии. Особенно это важно, если предполагаемая продолжительность жизни паци ента меньше чем 1—2 года и у него выявлены тяжелые сопутствующие заболевания. После того как заживет рана, возникающий рестеноз не приводит к рецидиву некроза или язв из-за достаточного притока крови.
Результаты: повышение дистанции ходьбы и увели чение ЛПИ. Частота осложнений— 5,8%, без случаев ампутации и хирургического вмешательства. Первичная проходимость (по данным УЗДГ и ангиографии) через 1 год после выполнения ангиопластики регистрируется у 2/3 больных.
Технические особенности выполнения эндовас кулярных манипуляций. Доступ. Правильно выбран ный доступ — важная часть процедуры. При выполне нии дистальной ангиопластики различают следующие доступы:
•контралатеральный;
•ипсилатеральный антеградный;
•ретроградный большеберцовый;
•ретроградный большеберцовый/стопный.
Внастоящее время первые два используются наибо лее часто, существенно реже — ретроградный больше-
124
Критическая ишемия нижних конечностей
берцовый доступ. Последний доступ — альтернативный подход, используемый тогда, когда обычные антеградный или контралатеральный ретроградный закончи лись неудачей. Этот тип доступа требует достаточного калибра передней и задней большеберцовых артерий ниже лодыжки, чтобы попытаться их пунктировать.
Адекватная антикоагулянтная терапия во время инфраподколенной интервенции является решающей в предотвращении тромботических осложнений. Кроме того, сосуды ниже щели коленного сустава чувствитель ны к манипуляции, часто спазмируются и во время про цедуры рекомендуется внутриартериальное использо вание вазодилататоров.
Проводник и методы предупреждения поврежде ний сосудов. Основная причина технических неудач — неспособность предупредить повреждение сосуда про водником. Вообще в большеберцовых артериях исполь зуются 0,14-дюймовые или 0,18-дюймовые проводные системы, хотя стандартный проводник может быть полезен при стенотических повреждениях и окклюзиях, особенно протяженных, требующих более агрессивного подхода. Если первоначально произошла неудача со стандартным проводником, то дополнительную провод никовую поддержку может обеспечить также баллон или катетер. В пошаговом подходе используются гидрофиль ные проводники. Они имеют более высокий риск перфо рации артериальной стенки и должны использоваться с осторожностью. Для более распространенных окклю зии может быть предпринята методика субинтимальной реканализации и ангиопластики.
Баллонная ангиопластика. Первоначально баллон ная ангиопластика принялась в качестве главного метода реваскуляризации при КИНК. Вообще длинные баллоны диаметром 2,5—4 мм используются с продолжительны ми (5-минутными) раздуваниями. Различают короткие и протяженные стенотические поражения, диффузные стенотические повреждения и окклюзию протяженностью менее 10 см в большеберцовых и малоберцовых сосудах. В сравнении с хирургическими восстановительными опе рациями эта эндоваскулярная техника отличается лучшей реваскуляризацией с существенным улучшением дистальной перфузии конечности, непосредственным облег чением боли покоя и ускорением заживления язвы.
Использование сокращающегося баллона в инфраподколенных артериях в 20% случаев приводило к интимальной диссекции и неадекватным гемодинамическим результатам, что требовало в большинстве слу чаев использования добавочного стентирования. Тем не менее сокращающиеся баллоны могут применяться с целью лечения остиальных поражений или неоинтимальной гиперплазии.
В1987 году A. Bolia в Великобритании была раз работана методика субинтимальной ангиопластики при протяженных окклюзиях бедренных и берцовых сосудов. Она заключается в намеренном создании субинтимальной диссекции, которая начинается проксимальнее окклюзионного поражения артерии. Диссекция продлевается
всубинтимальном пространстве до повторного входа
впросвет сосуда в точке, расположенной дистальнее окклюзии (рис. 2). Субинтимальный канал теоретически свободен от эндотелия и атеросклеротических бляшек, вто время как при обычной ангиопластике поврежден ный эндотелий и атероматозные массы могут служить источником агрегации тромбоцитов в ближайшем перио де и неоинтимальной гиперплазии — в отдаленном.
Взависимости от локализации и типа поражения,
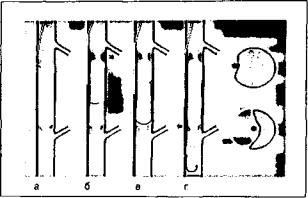
атакже от предпочтения оператора субинтимальная ангиопластика может быть выполнена антеградным ипсилатеральным или ретроградным контралатераль ный бедренным доступом. Проводник с изогнутым кон чиком в начале окклюзии направляется с помощью кате тера в стенку артерии {рис. 2 а), свободную от контрла теральных ветвей. Дальнейшее продвижение проводни ка обычно вызывает начало диссекции (рис. 2 6), затем катетер вводится в зону окклюзии. Как правило, при продвижении в субинтимальном пространстве провод ник складывается в петлю большого диаметра (рис. 2 в). Последовательно проводя петлю проводника и катетер, обычно несложно преодолеть всю длину окклюзированного сегмента. Выход в свободный просвет сосуда после прохождения участка окклюзии (рис. 2 г) облег чается тем, что непораженная интима прочно связана с
Рис. 2. Техника субинтимальной ангиопластики: а — провод ник с изогнутым кончиком в начале окклюзии направляется с помощью катетера в стенку артерии; 6 — катетер вводится в
зону окклюзии; в — проводник складывается в петлю боль шого диаметра; г — выход в свободный просвет сосуда после прохождения участка окклюзии
125
Сердечно-сосудистая хирургия
медией, тогда как пораженная интима утрачивает такую связь. Поэтому, когда петля проводника продвигается по пораженному участку, она встречает минимальное сопротивление, достигая же границы между поражен ной и менее пораженной интимой, проводник входит в истинный просвет артерии. Как только кончик катетера выходит за пределы окклюзии, проводник извлекается, и путем введения небольшого количества контрастного вещества подтверждается факт реентри, а также оцени вается состояние дистального русла.
При наличии остаточного, лимитирующего поток, поражения целесообразно имплантировать стент. В то же время не рекомендуется рутинное стентирование зоны субинтимальной ангиопластики, т.к. она не дает преимуществ в отношении проходимости артерии в отдаленные сроки. Особенностью вмешательств на артериях голени является то, что во избежание спазма каждому этапу предшествует внутриартериальное вве дение нитроглицерина в дозе ОД—0,2 мкг.
Цель процедуры считается достигнутой, если вос станавливается магистральный кровоток до стопы хотя бы по одной артерии голени. Все пациенты должны получать аспирин в дозе 100 мг в сутки пожизненно.
В качестве примера на рис. 3 представлено клини ческое наблюдение пациентки П., 79 лет, с критической ишемией обеих нижних конечностей и тяжелой сопутст вующей патологией (ИБС, хронический обструктивный
|
|
|
|
|
|
4L |
|
Г |
|
|
|
F |
^f"1 |
|
|
|
у - |
|
|
|
|
|
|
PJ |
IMP |
I/ |
|
|
1 |
|
|||||
$ |
/ |
|
|
||
щ |
п |
7 |
|
|
|
щ |
Ц' |
• г |
1, |
||
н |
р: |
it Л |
|||
• |
!1J |
К mm1 |
*4 |
||
а |
б |
В |
г |
||
|
|
|
|
|
|
Рис. 3. Ашиограммы пациентки П., 79 лет, до (а, 6) и | (в, г) субинтимальной ангиопластики
бронхит, гипертоническая болезнь, цереброваскулярная болезнь). Выполнена двухсторонняя субинтимальная ангиопластика бедренно-подколенного сегмента и артерий голени с интервалом в 2 недели. В результате был восстановлен магистральный кровоток до стопы по всем большеберцовым артериям. Критическая ишемия разрешилась. Язвенные поражения зажили.
Вероятность технического успеха процедуры высо ка и составляет 80—90%. Перфорации, как правило, не имеют клинических последствий и корригируются дилатацией альтернативного субинтимального канала.
Несмотря на положительные результаты авторов, методика до недавнего времени не получала большого распространения в сосудистых центрах. Наши резуль таты превзошли ожидания: частота сохранения конеч ности высока и достигает 88 и 68% в течение 1 и 3 лет, соответственно. Причем речь идет о больных высокого хирургического риска, часто без материала для аутовенозного шунтирования, а также с пораженным дистальным руслом. Принимая во внимание преимущества данной техники, включающей местную анестезию, мини мальную инвазивность, малые сроки госпитализации и низкую стоимость,— субинтимальная ангиопластика заняла достойное место в лечении пациентов с крити ческой ишемией нижних конечностей.
Стентирование берцовых артерий. Данные отно сительно использования стентов в инфраподколенных артериях ограничены. Общие причины редкого использования стентов в этой области — ограниченные возможности дилатации и малый диаметр артерий (до 4 мм). Будущие технологии могут разрешить проблему внутристентовых рестенозов в артериях малого диамет ра нижней конечности.
Лазер. Лазерный свет (308 nm) удаляет бляшку путем фотоакустической аблации. Лазер поставляет через гиб кий оптоволоконный катетер ультрафиолетовую энергию короткими пульсами. Эта технология предполагает уда ление бляшки, что уменьшает возможность эмболичес ких осложнений. Недавно опубликованные результаты показали процедурный успех в 86% случаев с исполь зованием эксимерного лазера у пациентов с высоким риском для хирургического вмешательства из-за наличия противопоказаний или непригодными для шунтирования подкожными венами. Это исследование продемонстри ровало возможности спасения конечности до 6 месяцев в 93% случаях. Преимущество лазера состоит в том, что он может облегчать реканализацию трудных для про хождения проводником хронических окклюзии. Кроме того, при полных окклюзиях можно использовать «поша говый» подход лазера, и затем специалист работает проводником до успешной реканализации. Добавочная
126

Критической ишемия нижних конечностей
баллонная ангиопластика обычно выполняется после использования лазерного воздействия.
Осложнения транслюминальной ангиопластики.
По результатам многочисленных исследований смерт ность после транслюминальной ангиопластики состав ляет 1,7%. Это ниже интраоперационной смертности (от 1,8 до 6%) при дистальном шунтировании. Ранняя пос леоперационная смертность была в 2,9% случаях после эндоваскулярных манипуляций и 5,6%— после хирур гического вмешательства. Частота перфорации артерий может достигать 3,7% и чаще встречается у диабетиков и пожилых пациентов. Это осложнение может быть купировано баллонной тампонадой с или без отмены антикоагулянтов. Другие главные осложнения проис ходят от 2 до 6% случаев и включают гематому участка доступа, острую артериальную непроходимость, свя занную с эмболией. Ятрогенная артериальная окклюзия может быть вторичной из-за спазма, диссекции или дистальной эмболизации. Антиспазматические препа раты, стенты и тромболитики с или без аспирационной атерэктомии могут использоваться как помощь для раз решения патологического состояния.
Инфраподколенные интервенционные техноло гии. В последние годы возрос энтузиазм в отношении эндоваскулярного подхода клечению инфраподколенных
стенозирующих поражений артерий. Существует много причин для этого сдвига. Поскольку сосудистые хирурги предпочитают передавать пациентов специалистам по эндоваскулярным вмешательствам, дистальное шунтиро вание часто переходит в разряд вмешательств «второй линии». Оборудование для ангиопластики стало гораздо лучше, и методы инфраподколенной интервенции стали более качественными и надежными. Низкопрофильные баллоны с большой длиной стали более доступными и для наших лечебных учреждений. Задача для практикую щего интервенциониста — знать, какое устройство более соответствует в данной обстановке. Стентирование также выполняется для лечения стенозов берцовых артерий, что позволяет предотвратить ампутацию у пациентов с КИНК. Наблюдаются низкая частота рестенозов и сни жение потребности в дополнительных этапах лечения. Вот почему хирурги также поддерживают использование эндоваскулярных методов в качестве начального подхо да в лечении пациентов с критической ишемией конеч ностей. Приводим алгоритм действий специалистов при поступлении больного с КИНК (рис. 4).
В конечном счете успех выполненного хирургического вмешательства или совместно с эндовазальными мани пуляциями обычно ведет к клиническим результатам — заживлению язвы и возможности комфортной ходьбы.
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| |
Приемный покой |
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
i |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| |
Осмотр хирурга |
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
Сосудистая*патология |
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
Нет |
|
|
|
|
Осмотр сосудистого |
|
|
|
Критическая ишемия |
|
|||||
|
|
критической |
|
|
|
|
|
|
|
|
|
|
|||||
|
|
ишемии |
|
|
|
|
хирурга |
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Плановая |
|
|
|
|
|
|
Оценка тяжести состояния и |
|
|
||||||
|
|
консервативная |
|
|
|
|
|
|
осмотр специалистов и др. |
|
|
||||||
|
|
терапия |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
^ ^ \ _ |
|
|
||
|
|
Крайне тяжелое |
|
| |
Тяжелое |
| |
|
| |
Средней тяжести | |
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
1 |
|
|
|
|
i |
|
|
|
|
|
1 |
|
|
||
|
|
Ампутация по жиз |
|
|
|
УЗДГ, консерва |
|
|
|
/- |
|
УЗДГ, консерва |
|
||||
|
|
ненным показаниям |
|
|
|
тивная терапия |
|
|
|
|
тивная терапия |
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
Х ^ |
|
|
|
|
|
|
|
|
|
|
|
|
___^— |
|
|
|
|
|
|
—— |
|
||
|
|
Положительная |
|
|
|
|
|
|
Попытка |
|
|
|
|||||
|
|
|
Отрицательная |
|
|
|
|
|
Дооперационная |
|
|||||||
|
|
динамика |
|
линамика |
|
|
реконструкции |
|
|
ангиогоаФия |
|
||||||
|
|
1 |
|
|
1 |
|
|
(ангиография,' |
|
|
1 |
|
|||||
|
|
|
1 |
|
|
ангиопластика, |
|
|
|
||||||||
|
| |
Наблюдение |
Ампутация |
|
|
стентирование) |
|
|
Консервативная |
|
|||||||
|
|
|
|
по жизненным |
|
|
|
|
|
|
|
терапия |
|
||||
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
показаниям |
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
Положительная |
|
|
Отрицательная |
|
|||
|
|
|
|
|
|
|
|
|
|
|
динамика |
|
|
динамика |
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
||
|
|
|
|
|
|
|
|
|
|
1 |
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
Ампутация по жиз |
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
Наблюдение |
|
|
ненным показаниям |
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Рис. 4. Алгоритм действий хирурга при поступлении больного с критической ишемией нижних конечностей
127
Сердечно-сосудистая хирургия
|
|
Литература |
|
тяжелой ишемии. Актуальные вопросы сердечно-сосудис |
||||||||
|
|
|
|
|||||||||
|
|
|
|
той хирургии. Вильнюс, 1980, с. |
170—172. |
|
|
|
||||
1. |
Белов Ю.В., Косенков А.Н., Баяндин Н.Л. и др. Тактика хирур |
14. Казаков |
Ю.И., |
Евтихов |
P.M. Хирургические |
заболевания |
||||||
|
гического лечения больных с диффузными поражениями арте |
|
аорты и периферических артерий. Тверь—Иваново, 2003, |
|||||||||
|
рий нижних конечностей / Хирургия, 1999, № 4, с. 4—9. |
|
с. 17—18. |
|
|
|
|
|
|
|
||
2. |
Белов Ю.В., Остапенко А.Б. Хирургическое лечение больных с |
15. |
Капутин М.Ю., Овчаренко Д.В., Сорока В.В. |
и др. |
||||||||
|
множественным поражением артерий нижних конечностей / |
|
Субинтимальная ангиопластика в лечении больных с |
|||||||||
|
Ангиология и сосудистая хирургия, 2002, № 8, с. 72—79. |
|
критической ишемией нижних конечностей. Медицинаий |
|||||||||
3. |
Бокерия Л.А., Гудкова Р.Г. Сердечно-сосудистая хирургия — |
|
академический журнал. Т. 6, № 3, 2006, с. 103—109. |
|
||||||||
|
2005. Болезни и врожденные аномалии системы кровообра |
16. |
Кротовский Г.С., Зудин A.M. Тактика лечения пациентов с |
|||||||||
|
щения. М., НЦССХим. А.Н. Бакулева РАМН, 2006,114 с. |
|
критической ишемией нижних конечностей. И.: Медицина, |
|||||||||
4. |
Гавриленко А.В., Скрылев СИ. Хирургическое лечение боль |
|
2005, с. 10—17. |
|
|
|
|
|
|
|||
|
ных с критической ишемией нижних конечностей. М.: |
17. |
Покровский А.В., Москаленко Ю.Д., Гульмурадов Т. и др. |
|||||||||
|
Медицина, 2005,174 с. |
|
Отдаленные результаты реваскуляризации ишемизиро- |
|||||||||
5. |
Диагностика и лечение пациентов с критической ишемией |
|
ванной конечности через систему глубокой |
артерии |
||||||||
|
нижних конечностей. Российский консенсус. М., 2002, 40 с. |
|
бедра / Хирургия, 1997, /V? |
5, с. 3—7. |
|
|
|
|||||
6. Дибиров |
М.Д., Дибиров А.А. Саркисян Ю.Г. и др. |
18. |
Покровский А.В., Дан В.Н., |
Чупин А.В. Хирургическое лече |
||||||||
|
Хирургическое лечение хронической ишемии при дисталь- |
|
ние критической ишемии нижних конечностей. Матер. |
|||||||||
|
ных окклюзиях у лиц пожилого и старческого возраста. |
|
Всеросс. |
науч.-практ. |
конф. |
хирургов, |
посвященной |
|||||
|
Традиционные и новые направления сосудистой хирургии |
|
50-летию науч. хирургического общества на Кавказских |
|||||||||
|
и ангиологии. Челябинск, 2004, с. 88—91. |
|
Минеральных Водах. Кисловодск, 1996, с. 92. |
|
|
|||||||
7. Дуданов И.П., Гуни П., Щеглов Э.А. и др. Дистальное шун |
19. |
Покровский А.В., Дан В.Н., Чупин А.В. Артериализация веноз |
||||||||||
|
тирование при критической ишемии нижних конечностей |
|
ного кровотока стопы в спасении конечности от ампута |
|||||||||
|
у больных моложе и старше 80 лет. Вестник хирургии, |
|
ции у больных облитерирующим |
тромбангиитом |
с окклю |
|||||||
|
1997, т. 156, N° 2, с. 47—51. |
|
зией артерий голени и стопы при критической ишемии / |
|||||||||
8. Дуданов |
И.П., Карпов А.В., Капутин М.Ю., Сорока В.В., |
|
Ангиология и сосудистая хирургия, 2000, № 6, с. 86—99. |
|||||||||
|
Ерофеев А.А. Комплексное лечение атеросклеротических |
20. |
Савельев B.C., Кошкин В.М. Критическая ишемия нижних |
|||||||||
|
поражений абдоминального сегмента аорты, периферичес |
|
конечностей. М.: Медицина, 1997, с. 29—49. |
|
|
|||||||
|
ких артерий с критической ишемией нижних конечностей у |
21. |
Ратнер Г.Л., Слуцкер Т.Е. Системный анализ и вопросы |
|||||||||
|
больных преклонного и старческого возраста. Медицинский |
|
тактики у больных облитерирующим атеросклерозом |
|||||||||
|
академический журнал. Т. 7, № 1,2007, с. 166—172. |
|
нижних конечностей / Ангиология |
и сосудистая хирургия. |
||||||||
9. Дуданов |
И.П., Петровский В.И., Субботина Н.С. Муль- |
|
1995, N° 3, с. 107—112. |
|
|
|
|
|
|
|||
|
тифокальный атеросклероз: клинико-патогенетические |
22. |
Чеботарев Д.Ф., Маньковский Н.Б. Руководство |
по гери |
||||||||
|
аспекты ишемических органных поражений. Петрозаводск, |
|
атрии. М.: Медицина, 1982, с. 544. |
|
|
|
||||||
|
2004, 240 с. |
23. |
Becguemin LP., Melliere D.G., Benhaiem N. Late occlusion of |
|||||||||
10. Думпе Э.П., Говорунов Г.В., Терещенко AS. и др. Изолиро |
|
aorto-bifemoral graft. J. Cardiovasc. Surg., 1987, v. 28, №1, |
||||||||||
|
ванная профундопластика при бедренно-подколенных |
|
p. 12—17. |
|
|
|
|
|
|
|
||
|
окклюзиях / Хирургия, 1980, N° 8, с. 23—27. |
24. |
Bolia A., |
Brennan J., |
Bell |
P.R. |
Recanalisation of femora- |
|||||
11. Дюжиков |
А.А., Шорлуян П.М. Отдаленные результаты |
|
popliteal occlusions: Improving success rate by subintimat |
|||||||||
|
восстановительных сосудистых операций при облите- |
|
recanalisation. Clin. Radiol. 1989, v. 40, p. 325. |
|
|
|||||||
|
рирующем атеросклерозе сосудов нижних конечностей / |
25. |
Horstmann /?., Nielsen H.3., Erkens £., Kern M., HolhbachG. |
|||||||||
|
Хирургия, 1980, №- 8, с. 27—30. |
|
Aortofemoral bypass and extensive profundaplasty in combined |
|||||||||
12. Затевахин И.И., Говорунов Г.В., Сухарев И.И. Реконст |
|
arterial occlusive |
disease |
of the pelvic-femoral |
type |
—a stage |
||||||
|
руктивная хирургия поздней реокклюзии аорты и перифе |
|
oriented analysis. Vasa. 1993, v. 22, p. 157—168. |
|
|
|||||||
|
рических артерий. М.: Медицина, 1993. |
26. |
Rutherford R. Vascular surgery. 2005, v. 2, p. 830—842. |
|||||||||
13. |
Марцинкявичус A.M., Трипонис В.И., Баркаускас Э.И. и др. |
27. |
Satiani В., Liapis CD., Evans W.E. Prediction |
of |
distal |
|||||||
|
Техника обеспечения оттока во время реконструктивных |
|
reconstruction |
following |
aortofemoral bypass |
for |
limb |
|||||
|
операций на аорте и магистральных ее ветвях в стадии |
|
salvage. Surg.Gynecot.Obstet. 1980, v. 151, p. 500—502. |
|||||||||
128
ХИРУРГИЧЕСКОЕ ЛЕЧЕНИЕ НАРУШЕНИИ МОЗГОВОГО КРОВООБРАЩЕНИЯ
/7.0. Казанчян
Для большинства стран мира сосудисто-мозговая недостаточность — патология медико-социальной значимости. По данным ВОЗ, от церебро-васкулярных заболеваний ежегодно умирает около 5 млн человек. Инсульт занимает 3-е место в структуре причин леталь ности, второе — среди сердечно-сосудистых заболева ний и первое среди инвалидизирующих заболеваний.
Смертность от инсульта составляет в среднем 139 на 100 000 населения. В Российской Федерации этот пока затель равен 309. Крайне неблагоприятны результаты инсультов: почти 1/3 больных умирает в ближайшие дни, большинство становятся стойкими инвалидами, часто нуждаясь в посторонней помощи и лишь 17—20% возвращаются к трудовой деятельности. Частота разви тия повторных инсультов составляет ежегодно в сред нем 9—10% с летальностью, достигающей 62—65%.
Почти в 80% случаев инсульты имеют ишемический генез и лишь в 20% — геморрагический. Причиной ише мии головного мозга может быть как постепенно нарас тающая редукция мозгового кровотока и развивающие ся на этом фоне гемодинамические расстройства, так и эмболия в сосуды головного мозга. В 15—20% случаев причиной эмболии служат заболевания сердца (веге тации на створках аортального клапана, мерцательная аритмия, постинфарктная аневризма левого желудочка с тромбом, миксома, дилатационная или ишемическая кардиомиопатия, тромбообразование после протезиро вания клапанов сердца и др.). В 50% случаев причиной нарушения мозгового кровообращения и развития сосу дисто-мозговой недостаточности являются поражения брахиоцефальных ветвей аорты.
Предположения о причинной связи между пора жениями сонных артерий и инсультом высказывались давно. Основывались они на данных аутопсийных иссле дований. Внедрение в клиническую практику рентгеноконтрастной ангиографии Egos Monig в 1927 году позволило прижизненно выявить эти поражения и под твердить правомочность этих предположений. В начале 50-х годов XX столетия начались попытки лечения ангиографически верифицированных окклюзирующих пора жений сонных артерий хирургическим путем. Приоритет отдается Н. Eastcott, G.W. Pickering и G.S. Rob, которые в мае 1954 года успешно оперировали 66-летнюю пациен
тку со стенозом левой ВСА и транзиторными ишемическими атаками. Больная поправилась, исчезли симптомы ишемии головного мозга, что явилось еще одним под тверждением значимости сонной артерии в развитии расстройств мозгового кровообращения. Появившиеся вскоре аналогичные сообщения явились толчком для стремительного роста операций на сонных артериях. Расширялся и диапазон хирургических вмешательств. Начались операции по поводу окклюзирующих пора жений других брахиоцефальных ветвей. В 1956 году З.В. Davis с соавт. сообщили об эндартерэктомии из брахиоцефального ствола. В 1961 г. B.C. Савельев впервые в мире при протезировании брахиоцефального ствола для наложения проксимального анастомоза использовал восходящую аорту. Данная методика стала и по насто ящее время остается операцией выбора при необходи мости протезирования брахиоцефального ствола.
В1964 году J.C. Parrot впервые произвел операцию транспозиции подключичной артерии в общую сонную
вцелях коррекции кровотока по подключичной арте рии. С аналогичной целью M.D. Bakey с соавт. в 1965 году выполнили операцию сонно-подключичного шун тирования. Первые операции по поводу окклюзирую щих поражений подключичных артерий у нас в стране выполнил А.В. Покровский.
Вконце 70-х годов XX столетия были разработа ны эндоваскулярные методы лечения окклюзирующих поражений брахиоцефальных артерий. Появились пер вые сообщения об эндоваскулярной дилатации внут ренних сонных, подключичных артерий, а также общей сонной артерии и брахиоцефального ствола.
Следует отметить, что, несмотря на многочислен ные публикации о высокой эффективности каротидной эндартерэктомии (КЭАЭ), о значении ее в предотвра щении острых нарушений мозгового кровообращения, в конце 1970-х, начале 1980-х годов появились сообще ния, в которых эти результаты оспаривались и стави лась под сомнение целесообразность выполнения такой операции. Указывалось на несоблюдение при оценке результатов правил рандомизированных исследований и на то, что хирургическому вмешательству подвергают ся заведомо более легкие пациенты, в то время как кон сервативная терапия проводится у тяжелого континген-
129
Сердечно-сосудистая хирургия
та больных. Проведенные в конце 80-х годов XX столе тия многоцентровые исследования в Северной Америке и Европе (ACST— Asymptovatic Carotid Surgery Trial; CASANOVA — Carotid Artery Asymptomatic Narrowing Operation Versus Aspirin; NASCET— North American Symptomatic Carotid Endarterektomy Trial) с участи ем ведущих медицинских центров доказали неправо мочность таких заявлений и окончательно доказали преимущества каротидной эндартерэктомиии перед консервативными методами, значение ее в снижении частоты острых ишемических инсультов.
Изучалосьтечениеокклюзирующего процесса в зави симости от степени стеноза, клинической его манифес тации и характера и морфологии атеросклеротической бляшки. Полученные данные сравнивались с результата ми каротидных эндартерэктомий. Естественное течение гемодинамически значимых асимптомных поражений было неблагоприятным: частота ежегодного инсульта составляла от 2 до 5,7%. Более неблагоприятным было течение симптомных поражений при транзиторных ише мических атаках (ТИА): риск развития инсульта в тече ние первого года после появления симптомов составлял 12—13%, а к концу 5-го года наблюдения 35%. Частота же ежегодного инсульта при окклюзии внутренней сон ной артерии достигала 40% с последующей частотой 7% в год. Ежегодная летальность после перенесенного инсульта составляла 10%, а к концу 5-летнего срока возрастала до 50%. Было доказано неблагоприятное течение гетерогенных бляшек с изъязвленной поверх ностью: частота ежегодных инсультов при наличии язв поверхностью более 40 мм2 достигала 7,5%.
В отличие от этих данных летальность после КЭАЭ не превышала 2,3%, неврологические осложнения наблю дались в 0,5—3,0% случаев, а частота инсультов в пяти летний срок наблюдения не превышала 9%. И вполне закономерно каротидная эндартерэктомия в настоящее время является наиболее часто проводимой реконс труктивной сосудистой операцией, уступая лишь аортокоронарному шунтированию.
Основные черты патологии
Причинами нарушения кровотока по брахиоцефальным ветвям могут быть системные окклюзирующие заболевания сосудов, врожденные аномалии их разви тия, экстравазальная компрессия опухолями или раз вившимся после перенесенных операций спаечным процессом, спонтанное или посттравматическое рас слоение.
Основной причиной нарушений кровообращения и развития сосудисто-мозговой недостаточности служат атеросклероз и патологические извитости. Характерным для атеросклероза является частая (более чем в 2 раза) экстракраниальная локализация поражения, при этом «излюбленным местом» является бифуркация сонных артерий. Поражения проксимальных отрезков наблю дается реже. При подобных локализациях часто пора жаются подключичные артерии, реже брахиоцефальный ствол и еще реже общие сонные артерии. Процесс начинается с образования холестеринового «ядра» в толще стенки с постепенным его ростом и превраще нием в атероматозную бляшку. Увеличивающаяся в размерах бляшка приводит к сужению просвета артерии, затем повреждению интимы и проникновению в просвет сосуда атеросклеротической бляшки. Образующиеся на изъязвленной поверхности тромбы и внутрибляшечные кровоизлияния становятся реальной угрозой эмболи ческих осложнений. Постепенно происходит фиброзная трансформация и кальцификация бляшек.
Патологические деформации занимают второе место среди причин нарушений мозгового кровообра щения. При скрининговых УЗ-исследованиях патоло гические извитости сонных артерий выявляются в 25% случаев. Значительно чаще они встречаются при целе направленных УЗ-исследованиях у больных с различны ми проявлениями сосудисто-мозговой недостаточнос ти. Этиология патологических извитостей окончательно не установлена. Чаще указывается на их врожденный генез, связанный с нарушением эмбриогенеза. В пользу врожденного генеза патологии говорит частое их выяв ление у детей и подростков, при этом нередко у ближай ших родственников и родных, двусторонний характер патологии, сочетание извитостей с различными врож денными пороками сердца.
Вместе с тем нельзя исключить и приобретенный характер извитостей с учетом корреляции их с возрас том и более частого их развития при наличии сопутс твующей артериальной гипертензии. Образование изви тостей у больных с высокой артериальной гипертензией представляется защитным функциональным приобрете нием для уменьшения энергии пульсовой волны и обес печения равномерного мозгового кровотока.
Многообразие форм патологических извитос тей затрудняет выделение единой классификации. Различают (по классификации Weibel 3., Fields S., 1965) С- и S-образные извитости, перегибы под острым углом (kinking) и петлеобразования (coiling). Наш опыт 175 наблюдений патологических извитостей показыва ет, что встречаются также двойные перегибы или соче тание различных форм извитостей.
130
