
AA_2012_04-045-050
.pdf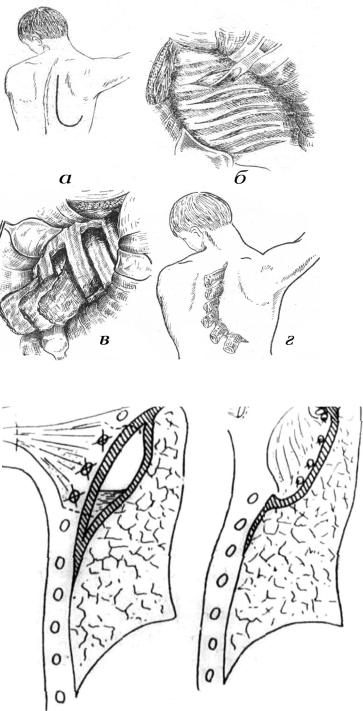
3. Хирургические заболевания легких и плевры
Рис. 118. Торакопластика по Линбергу
Рис. 119. Схема лечения эмпиемы мышечной пластикой
181
Клиническая хирургия
остеомиелит ребер и др.). Фибрин стимулирует репаративные процессы, антибиотики должны быть избирательными для инфекции.
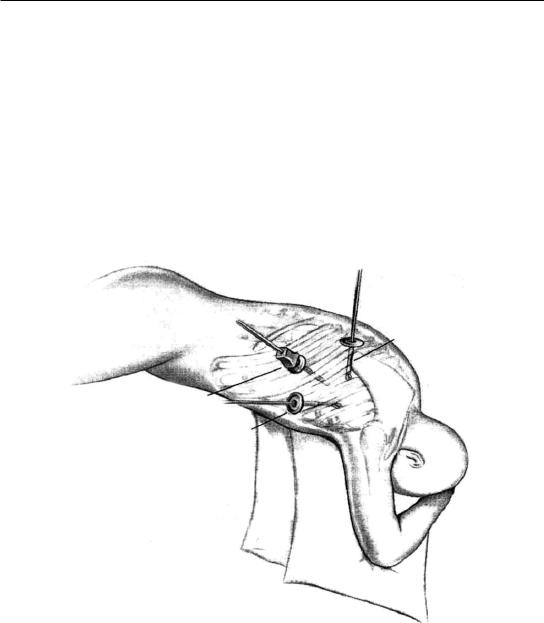
Для лечения хронических эмпием плевры перспективными являются и малоинвазивные методики. Применяются торакоскопические декортикация и плеврэктомия, санация, ликвидация свищей и т.д. Используя методику торакоскопического промывания и отсасывания плеврального содержимого, разделения сращений, кюретаж плевры, можно прервать развитие эмпиемы на ранней стадии. Плотные наложения на плевре при эмпиеме поддаются удалению с помощью торакоскопической техники. Порты для введения торакоскопа и инструментов создаются так же, как и при других торакоскопи- ческих операциях (рис. 120). Целью декортикации является как можно более полное удаление ограничивающих подвижность легких фибринозных пленок, расправление легкого (Франтзайдес, 2000).
Рис. 120. Расположение портов при торакоскопических операциях
Таким образом, острая и хроническая эмпиемы плевры являются тяжелыми заболеваниями, как правило, это осложнения заболеваний легких и грудной клетки. Важны их профилактика, своевременная диагностика и адекватное лечение, что зависит от знаний и умений врача.
182

4.Гнойные заболевания костей, суставов и околосуставных тканей
4.ГНОЙНЫЕ ЗАБОЛЕВАНИЯ КОСТЕЙ, СУСТАВОВ
ÈОКЛОСУСТАВНЫХ ТКАНЕЙ
4.1. Острый гематогенный остеомиелит
Остеомиелит – воспаление всех морфологических структур кости и окружающих е¸ мягких тканей, которое сопровождается остеонекрозом.
По смыслу «остеомиелит» – воспаление костного мозга, хотя с самого начала под этим термином подразумевалось воспаление всей кости. В 1831 г. М. Рейно ввел в литературу этот термин для обозначения воспалительного осложнения перелома костей. Попытки некоторых авторов заменить термин «остеомиелит» такими, как «паностит», «остеит», не увенчались успехом.
Воспаление кости было известно давно. О нем упоминается в трудах Гиппократа, Абу Али Ибн Сины, А. Цельса, К. Галена и др. Однако классическое описание клини- ческой картины острого остеомиелита в 1853 г. дал французский хирург Ш. Шассеньяк.
Возникновение остеомиелита связано с попаданием в костный мозг микробной флоры, чаще всего золотистого стафилококка, реже – стрептококка, диплококка, синегнойной палочки, протея и смешанной флоры. В зависимости от путей попадания микроорганизмов в кость остеомиелиты подразделяют на травматические и гематогенные. При травмати- ческих остеомиелитах инфицирование кости происходит через костную рану, возникающую в результате открытого ранения, ранения с повреждением кости или операции на костной ткани. При гематогенном остеомиелите микробная флора заносится в кость с кровью из какого-либо гнойного очага. Эти две формы различаются и по клинико-морфологичес- ким признакам.
Современная классификация разработана с учетом необходимости составления отчета, основанного на принципах количественной оценки различных сторон заболевания. Это развернутая рабочая классификация остеомиелита, которая учитывает этиологию, стадийность, фазность, локализацию патологического процесса и особенности клинического течения заболевания.
Классификация остеомиелита
1.Этиология.
1.1.Монокультура.
1.2.Смешанная, или ассоциированная, культура:
1.2.1.Двойная ассоциация.
1.2.2.Тройная ассоциация.
183

Клиническая хирургия
1.3.Возбудитель не выделен.
2.Клинические формы.
2.1.Острый гематогенный остеомиелит:
2.1.1.Генерализованная форма:
2.1.1.1.Септикотоксическая (молниеносная).
2.1.1.2.Септикопиемическая.
2.1.2.Местная (очаговая).
2.2.Посттравматический остеомиелит:
2.2.1.Развившийся после перелома кости.
2.2.2.Развившийся после огнестрельной раны.
2.2.3.Послеоперационный (включая спицевой).
2.2.4.Пострадиационный.
2.3.Атипичные формы:
2.3.1.Абсцесс Броди (вялотекущий внутрикостный процесс).
2.3.2.Альбуминозный остеомиелит Оллье-Понсе.
2.3.3.Склерозирующий остеомиелит Гарре.
2.3.4.Опухолевидный остеомиелит (остеоидостеома).
2.3.5.Послетифозный остеомиелит.
2.3.6.Антибиотический.
3.Стадии и фазы гематогенного остеомиелита.
3.1.Острая стадия:
3.1.1.Интрамедуллярная фаза.
3.1.2.Экстрамедуллярная фаза.
3.2.Подострая стадия:
3.2.1.Фаза выздоровления.
3.2.2.Фаза продолжающегося процесса.
3.3.Хроническая стадия:
3.3.1.Фаза обострения.
3.3.2.Фаза ремиссии.
3.3.3.Фаза выздоровления.
4.Локализация процесса и клинические формы.
4.1.Остеомиелит трубчатых костей.
4.2.Остеомиелит плоских костей.
4.3.Морфологические формы:
4.3.1.Диффузная.
4.3.2.Очаговая.
4.3.3.Диффузно-очаговая.
5.Осложнения.
5.1.Местные:
5.1.1.Патологический перелом.
5.1.2.Патологический вывих.
5.1.3.Ложный сустав.
184

4. Гнойные заболевания костей, суставов и околосуставных тканей
5.1.4.Другие местные осложнения.
5.2.Общие.
Âобщей структуре заболеваний органов опоры и движения доля остеомиелита составляет 6,5–7% (Амирасланов и др., 1998; Кутин 2000; Абаев и др., 2005; Каравелло и др., 2004). Среди всех гнойных процессов на долю гематогенного остеомиелита приходится от 6 до 10%, но по тяжести клинического течения, трудности диагностики, большому проценту осложнений, приводящих к инвалидности, и сложности лечения эту патологию следует отнести к очень тяж¸лым гнойным заболеваниям. Трудно найти равное остеомиелиту заболевание по длительности клинического течения. Срок заболевания во многих случаях ис- числяется не годами, а десятилетиями, что приводит к тяж¸лым осложнениям со стороны внутренних органов и нередко заканчивается ампутацией конечности. Исследования многих отечественных уч¸ных (Т.Я. Арефьев, Я.М. Брусникин, В.Я. Брайцев, И.С. Венгеровский, М.В. Гринев, И.В. Давыдовский, П.Г. Корнев, Т.П. Краснобаев, В.И. Москвин и др.) посвящены изучению этого заболевания, однако до настоящего времени оста¸тся не вполне ясной причина нарушения кровоснабжения кости, приводящая к некрозу. Одно несомненно: гематогенный остеомиелит развивается на фоне септицемии.
Этиология, патогенез, патоморфология
В 1880 г. Луи Пастер из гноя больной остеомиелитом выделил микроб и назвал его стафилококком. Впоследствии было установлено, что любой микроб может вызывать остеомиелит, однако его основным возбудителем является золотистый стафилококк. Однако с середины 70-х гг. прошлого столетия возросла роль грамотрицательных бактерий как возбудителей остеомиелита, в частности вульгарного протея, синегнойной палочки, кишечной палочки и клебсиеллы, которые чаще высеваются в ассоциации со стафилококком. Важным этиологическим фактором могут быть и вирусные инфекции, на фоне которых в 40–50% случаев развивается остеомиелит.
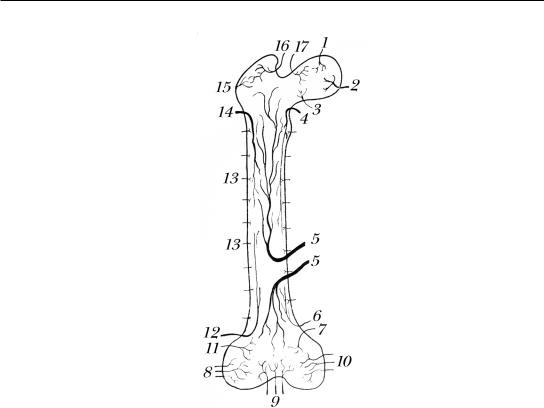
Существует множество теорий патогенеза остеомиелита. Основоположники сосудистой (эмболической) теории (А.А. Бобров, Лексер) указывали на особенности сосудов детей, способствующие возникновению остеомиелита. Они считали, что питающие кость артерии в метафизах разветвляются, образуя обширную сеть, в которой кровоток резко замедляется, способствуя оседанию в ней гноеродных микробов (рис. 121).
Однако последующие морфологические исследования установили, что концевые сосуды в метафизах длинных костей исчезают уже ко 2-му году жизни, в связи с чем идея А.А. Боброва оказалась односторонней. А. Виленский в 1934 г., не отрицая эмболической теории возникновения остеомиелита, дополнил е¸, полагая, что обструкция артериальной системы эпифиза обусловлена не пассивной закупоркой микробным эмболом, а развитием воспалительного тромбартериита или тромбофлебита. Однако последние патологии правильнее трактовать как возникающие вторично.
Значительным вкладом в развитие теории патогенеза остеомиелита явились эксперименты смоленского патологоанатома профессора С.М. Дерижанова (1937–1940 гг.), пред-
185
Клиническая хирургия
Рис. 121. Кровоснабжение длинных трубчатых костей человека (по М.Г. Привесу): 1, 2, 8, 9, 10 – эпифизарные сосуды; 3, 7, 11, 17 – метафизарные сосуды; 4, 6, 12, 14 –
добавочные диафизарные сосуды (aa. diaphyseos accessoriae); 5 – главные диафизарные сосуды (aa. nutriciae); 13 – сосуды надкостницы и кортикальные сосуды; 15, 16 – апофизарные сосуды
ложившего аллергическую теорию развития остеомиелита. Автор вызывал сенсибилизацию кроликов лошадиной сывороткой. Затем, вводя разрешающую дозу сыворотки в кост- но-мозговую полость, получал асептический аллергический остеомиелит. С.М. Дерижанов полагал, что бактериальные эмболы не играют роли в патогенезе остеомиелита. Заболевание развивается только на почве сенсибилизации организма и возникновения в кости асептического воспаления вследствие самых разных причин. В остеомиелитическом очаге пролиферативные изменения периоста, гаверсовых каналов сдавливают сосуды извне, а набухание стенок самих сосудов уменьшает их просвет изнутри. Все это затрудняет и нарушает кровообращение в кости, способствует возникновению остеомиелита.
Согласно нервно-рефлекторной теории (Н.Н. Еланский, Б.К. Осипов, В.В. Турбин, Д.Г. Рохлин) развитию остеомиелита предшествуют длительный рефлекторный спазм сосудов и нарушение кровообращения. Факторами, провоцирующими вазоспазм, могут быть любые раздражители внешней среды. При этом не отрицается роль сенсибилизации организма и наличия скрытой инфекции.
Кроме того, ряд авторов в этиопатогенезе остеомиелита придают значение и другим факторам, например травме (И.С. Венгеровский), которая сама по себе (без наличия виру-
186

4. Гнойные заболевания костей, суставов и околосуставных тканей
лентного агента) не может быть этиологическим фактором, но созда¸т участок кости с меньшей устойчивостью, так что при наличии эндогенной инфекции травма становится действующим этиологическим моментом (это имеет значение и для активации старых, латентных остеомиелитических очагов); внесосудистой окклюзии (М.В. Гринев), когда причиной сдавления питающих кровеносных сосудов является воспалительный инфильтрат; врожденной неполноценности сосудов кости (Ш. Шассеньяк).
Существуют и другие теории.
Процесс возникновения гематогенного остеомиелита очень сложен. Ни одна из существующих теорий не может объяснить всех особенностей возникновения и тече- ния этого заболевания. Каждая теория дополняет другие. Только совокупность выдвинутых положений может дать относительно правильное представление о патогенезе остеомиелита. Ясно одно: гематогенный остеомиелит – результат септикопиемии с локализацией воспалительного очага в кости.
В патогенезе острого остеомиелита большую роль играют аутогенные источники микрофлоры. Очаги скрытой или дремлющей инфекции в кариозных зубах, миндалинах, постоянно выделяя токсины и продукты распада, способствуют развитию аллергической реакции замедленного типа, создают предрасположенность организма к возникновению заболевания. В этой ситуации неспецифические раздражители (травма, переохлаждение, переутомление, болезни) играют роль разрешающего фактора и могут вызвать в кости асептическое воспаление. Последнее при попадании микробов в кровоток реализуется в острый гематогенный остеомиелит. В других случаях вследствие перенесенного заболевания или действия другого неспецифического раздражителя в преморбидном периоде организм может оказаться ослабленным; экзогенная инфекция, попав в ослабленный организм, может сыграть роль пускового механизма.
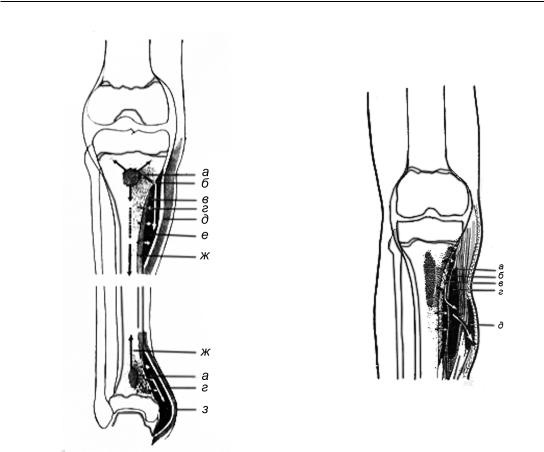
Патогенетически заболевание начинается как диффузный воспалительный процесс в костном мозге, распространяющийся на гаверсовы каналы и периост. Сдавление сосудов приводит к от¸ку костного мозга с последующей гнойной инфильтрацией, которая распространяется как вдоль по кости, так и к кортикальному слою, к надкостнице. Стенки гаверсовых канальцев подвергаются аутолизу. Гибнут клетки костного мозга и все слои костной структуры. Воспаление развивается по типу флегмоны. Давление в полости кости повышается до 300–400 мм вод. ст. (нормальное давление – до 50 мм вод. ст.), и по костным каналам поднадкостнично распространяется гнойное отделяемое, которое отслаивает надкостницу. Образуются субпериостальные абсцессы (рис. 122).
При разрыве надкостницы гной проникает в окружающие кость мягкие ткани, что сопровождается образованием флегмон мягких тканей, некрозов мышц, тромбофлебитов, тромбартериитов и невритов (рис. 123).
При эпифизарной локализации остеомиелита разрушается суставной хрящ и возникает артрит. Микробная флора из гнойного очага кости может попасть в сустав и лимфогенным пут¸м. У детей часто происходит эпифизиолиз – отделение эпифиза кости от диафиза по линии росткового хряща (метафиза).
Вокруг гнойного очага в кости развивается остеопороз – разрушение структуры кости, а на 3–4-й неделе от начала заболевания уже определяются очаги некроза.
187
Клиническая хирургия
Рис. 122. Морфология и распространение |
Рис. 123. Распространение гнойного процесса при |
гнойного процесса при остром остеомиелите (схе- |
остром остеомиелите в мягкие ткани: |
ма): а – абсцедировавшая флегмона |
а – абсцедировавшая флегмона миелона; |
в миелоне метафиза; б – прорыв гноя через |
б – поднадкостничный абсцесс; в – некроз |
тончайшую пористую пластинку кортекса; |
с начавшейся секвестрацией кортекса; |
в – поражение компактной костной ткани; |
г – внутримышечный абсцесс; |
г – прорыв гноя через гаверсовы каналы; |
д – подкожный абсцесс |
д – поднадкостничный абсцесс; е – отслойка над- |
|
костницы; ж – распространение гноя |
|
в направлении костно-мозгового канала; |
|
з – поднадкостничный и околосуставной |
|
абсцесс |
|
В дальнейшем образуются секвестры и секвестральные полости. Секвестры препятствуют заживлению очага. Рассасывание их затруднено из-за наличия в них микробов, подавляющих действие тканевых ферментов.
Некроз костной ткани сопровождается репаративными процессами, которые способствуют развитию остеосклероза. Остеобласты участвуют в формировании молодой костной ткани. При некупирующемся воспалительном процессе в секвестральной полости образуются свищи, что говорит о переходе острого воспалительного процесса в хронический.
188

4. Гнойные заболевания костей, суставов и околосуставных тканей
Патоморфологические изменения при остеомиелите в настоящее время изучены достаточно хорошо. В 1-е сутки заболевания в костном мозге отмечаются явления реактивного воспаления: гиперемия, расширение кровеносных сосудов, стаз крови с выхождением через измененную сосудистую стенку лейкоцитов и эритроцитов, межклеточная инфильтрация и серозное пропитывание. На 3–5-е сутки костно-мозговая полость заполняется красным и желтым костным мозгом; на отдельных участках обнаруживаются скопления эозинофилов и сегментоядерных нейтрофилов, единичные плазматические клетки. Скопление сегментоядерных нейтрофилов отмечается и в расширенных гаверсовых каналах коркового вещества кости.
На 10–15-е сутки гнойная инфильтрация прогрессирует с развитием выраженного некроза костного мозга по протяжению; выявляются резко расширенные сосуды с очагами кровоизлияний между костными перекладинами, множественные скопления экссудата с огромным количеством распадающихся лейкоцитов. Отмечено разрастание грануляционной ткани в элементах, окружающих костный мозг.
На 20–30-е сутки явления острого воспаления сохраняются. В костном мозге видны поля, заполненные некротическими массами, детритом и окруженные большими скоплениями сегментоядерных нейтрофилов и лимфоцитов. Намечаются отдельные участки эндостального костеобразования в виде примитивных костных перекладин. В корковом веществе гаверсовы каналы расширены, изъедены, костные перекладины истончены.
На 35–45-е сутки заболевания некроз распространяется почти на все элементы костной ткани, корковое вещество истончается. Кость продолжает разрушаться, эндостальное костеобразование отсутствует, полости заполнены гомогенными массами, в которых обнаруживаются секвестры в окружении гнойного экссудата. Секвестры прилежат к некротизированной ткани, которая без резких границ переходит в волокнистую соединительную ткань. Вблизи эндоста появляется грануляционная ткань, в которой видны массивные очаги некроза с участками костного мозга и резко расширенными сосудами, густо инфильтрированными миелоидными элементами различной степени зрелости.
Сроки образования секвестров различны. В одних случаях они определяются на рентгенограммах к концу 4-й недели, в других, особенно при обширных деструкциях, для окончательного отторжения омертвевших участков требуется 3–4 месяца (рис. 124).
Наличие отделившихся секвестров свидетельствует о переходе воспалительного процесса в хроническую стадию. После перехода острого воспалительного процесса в хронический сосуды вновь образовавшейся костной ткани постепенно запустевают, в межклеточном веществе откладываются соли кальция, придающие особую плотность костной ткани. Чем дольше существует очаг деструкции, тем больше выражены склеротические изменения в кости. Из вновь образовавшейся кости вокруг секвестра оформляется секвестральный «гроб». Отверстие кости, ведущее к центрально расположенному секвестру («клоаке»), сообщается со свищевым ходом (рис. 125).
Через несколько лет процесса эбурнеации (уплотнения губчатой структуры) кость приобретает исключительную плотность. В ней почти не определяются сосуды, при обра-
189
Клиническая хирургия
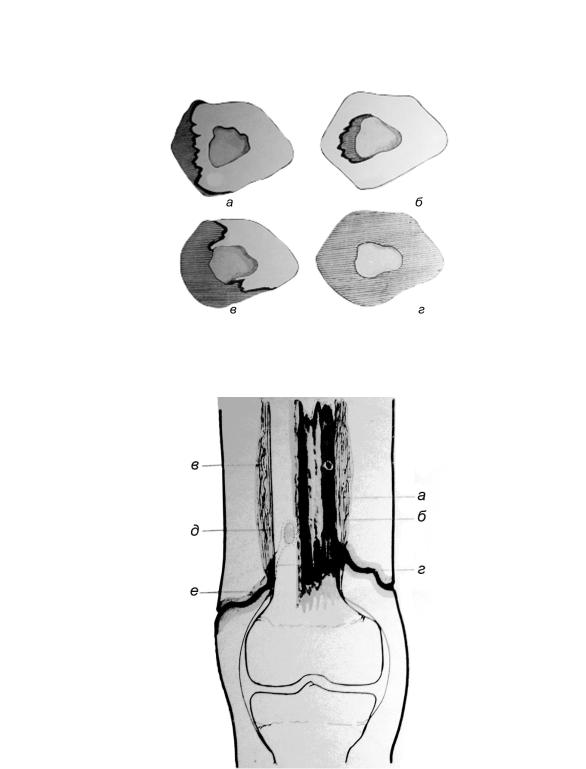
Рис. 124. Различные виды секвестрации: а – сегментарный кортикальный секвестр;
á– сегментарный центральный секвестр; в – сегментарный проникающий внутрь секвестр;
ã– тотальный секвестр
Рис. 125. Секвестральный «гроб»: a – секвестр;
á– секвестральный «гроб»; в – оссифицирующие периостальные наслоения;
ã– свищевой канал; д – клоака
190
