
- •Практикум
- •Модуль 1. Вуглеводні та їх похідні, що містять атоми галогенів, гідроксильні та карбонільні групи практичні заняття
- •Лабораторні заняття
- •Самостійна робота студента
- •Література Основна
- •Змістовий модуль 1. Вуглеводні та їх галогенопохідні практична робота №1
- •I. Тестові завдання
- •Завдання для самостійного розв’язання:
- •III. Вправи за темою "Добування та властивості алканів" Приклад розв’язання:
- •Завдання для самостійного розв’язання:
- •Метан а в с бутан.
- •IV. Розв’язання задач" Приклади розв’язання:
- •Кількість речовини Карбону, що міститься в спаленому зразку вуглеводню, дорівнює:
- •Відповідь:масова частка виходу продукту нітрометану дорівнює 85%.
- •Особливості конспектування і вимоги до конспекту
- •I. Тестові питання
- •I. Тестові завдання
- •Завдання для самостійного розв’язання:
- •III. Вправи за темою "Добування та властивості алкенів" Приклад розв’язання:
- •Ця реакція використовується для якісного і кількісного визначення сполук, які містять подвійний зв’язок між атомами Карбону.
- •Завдання для самостійного розв’язання:
- •Хлорометанетан а етен 1,2-дибромоетан.
- •IV. "Розв’язання задач" Приклади розв’язання:
- •Самостійна робота №2. Алкадієни. Загальна характеристика. 1,3-Бутадієн. Ізопрен. Застосування 1,3-бутадієну та ізопрену
- •I. Тестові завдання
- •Завдання для самостійного розв’язання:
- •III. Вправи за темою “Добування та властивості алкінів” Приклад розв’язання:
- •Завдання для самостійного розв’язання:
- •IV. “Розв’язання задач” Приклади розв’язання:
- •Згідно рівнянням (I) і (II):
- •Практична робота №4
- •I. Тестові завдання
- •Завдання для самостійного розв’язання:
- •III. Вправи за темою “Добування та властивості аренів” Приклад розв’язання:
- •Завдання для самостійного розв’язання:
- •IV. “Розв’язання задач” Приклади розв’язання:
- •Самостійна робота №3. Окиснення гомологів бензену. Багатоядерні арени.
- •Лабораторна робота № 1
- •Дослід 1. Добування хлороформу з хлоралгідрату
- •Дослід 2. Добування йодоформу
- •Дослід 3. Якісне визначення галогенів (проба Бейльштейна)
- •Література
- •Змістовий модуль 2. Гідроксильні похідні вуглеводнів та карбонільні сполуки лабораторна робота № 2
- •Дослід 1. Взасмодія етанолу з металічним натрієм
- •Література
- •Самостійна робота №4. Багатоатомні спирти. Загальна характеристика. Окремі представники: етиленгліколь та гліцерин, їх ідентифікація в медицині.
- •Лабораторна робота № 3
- •Дослід 1. Дія ферум (III) хлориду на одно- та багатоатомні феноли
- •Дослід 2. Реакція конденсації фенола з реактивом Маркі
- •Дослід 3. Осадження білка фенолом
- •Література
- •Самостійна робота №6.Багатоатомні феноли. Пірокатехін. Резорцин. Гідрохінон. Пірогалол
- •Лабораторна робота № 4
- •Дослід 1
- •Дослід 4 Окиснення формальдегіду купрум (II) гідроксидом в лужному середовищі (проба Троммера)
- •Дослід 5
- •Модуль 2. Органічні сполуки, що містять карбоксильні групи, атоми Нітрогену; гетерофункціональні та гетероциклічні сполуки лабораторні заняття
- •Самостійна робота студента
- •Література Основна
- •Додаткова
- •Змістовий модуль 3 лабораторна робота № 5
- •Дослід 1. Відношення карбонових кислот до дії окисників
- •Дослід 2. Підтвердження наявності альдегідної групи в молекулі форміатної кислоти
- •Дослід 3. Розчинність бензенової кислоти у лугах
- •Дослід 4. Якісні реакції на ацетат- та бензоат-іони
- •Дослід 5. Возгонка бензенової кислоти (“зимовий сад”)
- •Література
- •Лабораторна робота № 6
- •Дослід 1. Доказ наявності двох карбоксильних груп у молекулі оксалатної кислоти (одержання калієвих солей)
- •Дослід 2. Якісна реакція на оксалат-іон
- •Лабораторна робота № 7
- •Дослід 1. Утворення нітрату сечовини
- •Дослід 2. Гідроліз сечовини
- •Дослід 3. Утворення та виявлення біурету
- •Література
- •Дикарбонові кислоти. Щавлева кислота
- •Дослід 2. Лігнінова проба
- •Дослід 3. Окиснення аніліну
- •Література
- •Завдання для котролю знань
- •Лабораторна робота № 9
- •Дослід 1. Доказ будови тартратної кислоти
- •Дослід 2. Розкладання цитратної кислоти під дією концентрованої сульфатної кислоти
- •Дослід 3. Визначення лактатної кислоти в молочній сироватці
- •Література
- •Завдання для котролю знань
- •Лабораторна робота № 10
- •Дослід 1. Розчинність саліцилової кислоти у воді, спирті, лугах
- •Дослід 2. Доведення наявності фенольного гідроксилу в саліциловій кислоті
- •Дослід 3. Гідроліз ацетилсаліцилової кислоти та фенілсаліцилату (салолу)
- •Література
- •Самостійна робота №10.Фенолокислоти. Будова фенолокислот. Саліцилова кислота: будова, хімічні властивості. Фізіологічний вплив на організм людини. Ацетилсаліцилова кислота. Фенілсаліцилат
- •I. Тестові питання
- •II. Вправи для розв’язання
- •Самостійна робота №11.Поняття про пептиди та білки. Структури білків
- •Дослід 2. Відсутність відновлючої здатності у сахарози
- •Дослід 3. Кислотний гідроліз крохмалю
- •Література
- •Завдання для котролю знань
- •Самостійна робота №12.Вуглеводи.Поняття про полісахариди
- •I. Тестові питання
- •II. Вправи для розв’язання
- •II. Вправи для розв’язання
- •I. Тестові питання
- •II. Вправи для розв’язання
- •71. Укажіть структурну формулу малонової кислоти:
- •107. Укажіть назву органічної сполуки, яка належить до дисахаридів:
- •120. Укажіть назву органічної сполуки, яка належить до пятичленних гетероциклів з двома гетероатомами:
- •141. Установіть відповідність між хімічними формулами та класами органічних сполук:
- •161. Установіть послідовність розташування гомологів у гомологічному ряді одноосновних насичених карбонових кислот:
Завдання для самостійного розв’язання:
1. Як здійснити наступні перетворення:
етан
етиловий спирт етилен бромоетан 1,1-дибромоетан?
За допомогою структурних формул напишіть рівняння реакцій і зазначте умови, за яких відбуваються реакції.
2. Наведіть рівняння реакцій, за допомогою яких можна здійснити такі перетворення:
C2H6 C2H4 C2H5Cl
C2H4Cl2
Зазначте умови, за яких відбуваються реакції.
3. Наведіть рівняння реакцій, за допомогою яких можна здійснити такі перетворення:
Хлорометанетан а етен 1,2-дибромоетан.
Назвіть невідому речовину. Зазначте умови, за яких відбуваються реакції.
4. Напишіть рівняння реакцій полімеризації: а) 2-метилпропену; б) 1-бутену; в) 2-бутену.
5. У дві пробірки з бромною водою і розчином калій перманганату поклали шматочки поліетилену. Чи зміниться забарвлення розчинів? Порівняйте дію на етилен та поліетилен бромної води та калій перманганату. Чи можна вважати поліетилен ненасиченою сполукою?
IV. "Розв’язання задач" Приклади розв’язання:
Задача №1: Етиленовий вуглеводень масою 7,0 г приєднує 2,24 л (н.у.) гідроген броміду. Визначите формулу і будову цього вуглеводню, якщо відомо, що він є цис-ізомером.
Розв’язання: 1. Обчислюємо кількість речовини гідроген броміду:
(HBr) = V(HBr)/Vm = 2,24/22,4 = 0,1 моль.
2. Складаємо рівняння хімічної реакції приєднання гідроген броміду до етиленового вуглеводню в загальному вигляді:
![]()
Згідно рівнянню реакції: (CnН2n) = (HBr) = 0,1 моль.
3. Обчислюємо молярну масу етиленового вуглеводню:
M(CnН2n) = m(CnН2n)/(CnН2n) = 7,0/0,1 = 70 г/моль.
4. Молярну масу етиленового вуглеводню CnН2n можна визначити також інакше:
M(CnН2n) = n·M(C) + 2n·M(Н) = (12n + 2n) г/моль.
Отже, 12n + 2n = 70. Відповідно 14n = 70; n = 70/14 = 5.
Таким чином, етиленовим вуглеводням складу С5Н10 відповідають п’ять структурних ізомерів:
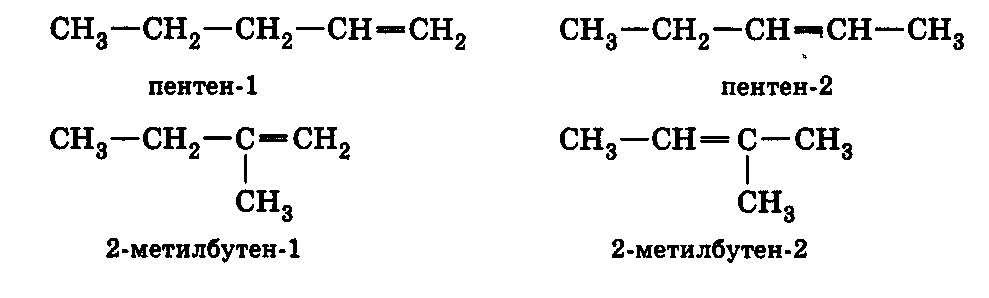

З цих речовин тільки 2-пентен має цис-транс-ізомери, тому що кожен з атомів Карбону, що зв’язаний подвійним зв’язком має два різних замісники:

Відповідь: цис-2-пентен.
Задача №2: Суміш етану та етилену об’ємом 200 мл (нормальні умови) знебарвила бромну воду масою 25 г. Розрахуйте об’ємну частку етилену в суміші, якщо масова частка брому в бромній воді дорівнює 3,2%.
Розв’язання: 1. Обчислюємо масу брому, що міститься в бромній воді:
m(Br2) = m(бром. води)·(Br2)/100% = 25·3,2%/100% = 0,8 г.
2. Обчислюємо кількість речовини брому:
(Br2) = m(Br2)/М(Br2) = 0,8/160 = 0,005 моль.
3. З бромною водою легко взаємодіє тільки етилен з утворенням 1,2-дибромоетану. Складаємо рівняння відповідної хімічної реакції:
С2Н4 + Br2 С2Н4Br2
Згідно рівнянню реакції: (С2Н4) = (Br2) = 0,005 моль.
4. Обчислюємо об’єм етилену за нормальних умов:
V(С2Н4) = (С2Н4)·Vm = 0,005·22,4 = 0,112 л = 112 мл.
5. Розраховуємо об’ємну частку етилену у вихідній газовій суміші:
(С2Н4) = V(С2Н4)/V(суміші) = 112/200 = 0,56 або 56%.
Відповідь: об’ємна частка етилену в суміші дорівнює 56%.
Завдання для самостійного розв’язання:
1. Масова частка Гідрогену в молекулі вуглеводню дорівнює 14,29 %. Густина речовини за повітрям 1,931. Визначте молекулярну формулу сполуки.
2. При спалюванні 2,45 г органічної речовини утворилось 7,7 г вуглекислого газу і 3,15 г води. Відносна густина пари цієї речовини за вуглекислим газом дорівнює 0,64. Визначте молекулярну формулу речовини.
3. 5,6 г етиленового вуглеводню приєднують 4,48 л гідроген хлориду (нормальні умови). Визначте молекулярну і структурну формули вуглеводню.
4. Визначте масову частку виходу продукту реакції (у % від теоретично можливого), якщо при взаємодії 5,6 л етилену (нормальні умови) з бромом було добуто 42,3 г 1,2-диброметану.
5. Суміш метану з етиленом об’ємом 800 мл (нормальні умови) знебарвила 200 г бромної води з масовою часткою брому 1,6%. Визначте об’ємну частку етилену в суміші.
