
- •Практикум
- •Модуль 1. Вуглеводні та їх похідні, що містять атоми галогенів, гідроксильні та карбонільні групи практичні заняття
- •Лабораторні заняття
- •Самостійна робота студента
- •Література Основна
- •Змістовий модуль 1. Вуглеводні та їх галогенопохідні практична робота №1
- •I. Тестові завдання
- •Завдання для самостійного розв’язання:
- •III. Вправи за темою "Добування та властивості алканів" Приклад розв’язання:
- •Завдання для самостійного розв’язання:
- •Метан а в с бутан.
- •IV. Розв’язання задач" Приклади розв’язання:
- •Кількість речовини Карбону, що міститься в спаленому зразку вуглеводню, дорівнює:
- •Відповідь:масова частка виходу продукту нітрометану дорівнює 85%.
- •Особливості конспектування і вимоги до конспекту
- •I. Тестові питання
- •I. Тестові завдання
- •Завдання для самостійного розв’язання:
- •III. Вправи за темою "Добування та властивості алкенів" Приклад розв’язання:
- •Ця реакція використовується для якісного і кількісного визначення сполук, які містять подвійний зв’язок між атомами Карбону.
- •Завдання для самостійного розв’язання:
- •Хлорометанетан а етен 1,2-дибромоетан.
- •IV. "Розв’язання задач" Приклади розв’язання:
- •Самостійна робота №2. Алкадієни. Загальна характеристика. 1,3-Бутадієн. Ізопрен. Застосування 1,3-бутадієну та ізопрену
- •I. Тестові завдання
- •Завдання для самостійного розв’язання:
- •III. Вправи за темою “Добування та властивості алкінів” Приклад розв’язання:
- •Завдання для самостійного розв’язання:
- •IV. “Розв’язання задач” Приклади розв’язання:
- •Згідно рівнянням (I) і (II):
- •Практична робота №4
- •I. Тестові завдання
- •Завдання для самостійного розв’язання:
- •III. Вправи за темою “Добування та властивості аренів” Приклад розв’язання:
- •Завдання для самостійного розв’язання:
- •IV. “Розв’язання задач” Приклади розв’язання:
- •Самостійна робота №3. Окиснення гомологів бензену. Багатоядерні арени.
- •Лабораторна робота № 1
- •Дослід 1. Добування хлороформу з хлоралгідрату
- •Дослід 2. Добування йодоформу
- •Дослід 3. Якісне визначення галогенів (проба Бейльштейна)
- •Література
- •Змістовий модуль 2. Гідроксильні похідні вуглеводнів та карбонільні сполуки лабораторна робота № 2
- •Дослід 1. Взасмодія етанолу з металічним натрієм
- •Література
- •Самостійна робота №4. Багатоатомні спирти. Загальна характеристика. Окремі представники: етиленгліколь та гліцерин, їх ідентифікація в медицині.
- •Лабораторна робота № 3
- •Дослід 1. Дія ферум (III) хлориду на одно- та багатоатомні феноли
- •Дослід 2. Реакція конденсації фенола з реактивом Маркі
- •Дослід 3. Осадження білка фенолом
- •Література
- •Самостійна робота №6.Багатоатомні феноли. Пірокатехін. Резорцин. Гідрохінон. Пірогалол
- •Лабораторна робота № 4
- •Дослід 1
- •Дослід 4 Окиснення формальдегіду купрум (II) гідроксидом в лужному середовищі (проба Троммера)
- •Дослід 5
- •Модуль 2. Органічні сполуки, що містять карбоксильні групи, атоми Нітрогену; гетерофункціональні та гетероциклічні сполуки лабораторні заняття
- •Самостійна робота студента
- •Література Основна
- •Додаткова
- •Змістовий модуль 3 лабораторна робота № 5
- •Дослід 1. Відношення карбонових кислот до дії окисників
- •Дослід 2. Підтвердження наявності альдегідної групи в молекулі форміатної кислоти
- •Дослід 3. Розчинність бензенової кислоти у лугах
- •Дослід 4. Якісні реакції на ацетат- та бензоат-іони
- •Дослід 5. Возгонка бензенової кислоти (“зимовий сад”)
- •Література
- •Лабораторна робота № 6
- •Дослід 1. Доказ наявності двох карбоксильних груп у молекулі оксалатної кислоти (одержання калієвих солей)
- •Дослід 2. Якісна реакція на оксалат-іон
- •Лабораторна робота № 7
- •Дослід 1. Утворення нітрату сечовини
- •Дослід 2. Гідроліз сечовини
- •Дослід 3. Утворення та виявлення біурету
- •Література
- •Дикарбонові кислоти. Щавлева кислота
- •Дослід 2. Лігнінова проба
- •Дослід 3. Окиснення аніліну
- •Література
- •Завдання для котролю знань
- •Лабораторна робота № 9
- •Дослід 1. Доказ будови тартратної кислоти
- •Дослід 2. Розкладання цитратної кислоти під дією концентрованої сульфатної кислоти
- •Дослід 3. Визначення лактатної кислоти в молочній сироватці
- •Література
- •Завдання для котролю знань
- •Лабораторна робота № 10
- •Дослід 1. Розчинність саліцилової кислоти у воді, спирті, лугах
- •Дослід 2. Доведення наявності фенольного гідроксилу в саліциловій кислоті
- •Дослід 3. Гідроліз ацетилсаліцилової кислоти та фенілсаліцилату (салолу)
- •Література
- •Самостійна робота №10.Фенолокислоти. Будова фенолокислот. Саліцилова кислота: будова, хімічні властивості. Фізіологічний вплив на організм людини. Ацетилсаліцилова кислота. Фенілсаліцилат
- •I. Тестові питання
- •II. Вправи для розв’язання
- •Самостійна робота №11.Поняття про пептиди та білки. Структури білків
- •Дослід 2. Відсутність відновлючої здатності у сахарози
- •Дослід 3. Кислотний гідроліз крохмалю
- •Література
- •Завдання для котролю знань
- •Самостійна робота №12.Вуглеводи.Поняття про полісахариди
- •I. Тестові питання
- •II. Вправи для розв’язання
- •II. Вправи для розв’язання
- •I. Тестові питання
- •II. Вправи для розв’язання
- •71. Укажіть структурну формулу малонової кислоти:
- •107. Укажіть назву органічної сполуки, яка належить до дисахаридів:
- •120. Укажіть назву органічної сполуки, яка належить до пятичленних гетероциклів з двома гетероатомами:
- •141. Установіть відповідність між хімічними формулами та класами органічних сполук:
- •161. Установіть послідовність розташування гомологів у гомологічному ряді одноосновних насичених карбонових кислот:
Лабораторна робота № 3
Тема роботи: Дія ферум (III) хлориду на одно- та багатоатомні феноли. Реакція конденсації фенола з реактивом Маркі. Осадження білка фенолом.
Мета роботи:
Дослід 1. Дія ферум (III) хлориду на одно- та багатоатомні феноли
Виконання:
1. В пробірку помістіть 3 краплі прозорої фенольної води і додати 1 краплю розчину ферум (III) хлориду. Спостерігається поява характерного кольору.
2. В чотири пробірки помістіть по 3 краплі розчинів: №1 – пірокатехіну; №2 – резорцину; №3 – гідрохінону; №4 – пірогалолу. В кожну пробірку додайте по 1 краплі розчину ферум (III) хлориду.
Кольорова реакція з ферум (III) хлоридом використовується для ідентифікації фенолів.
Завдання:
1. Складіть рівняння реакції взаємодії фенолу з ферум (III) хлоридом.
2. Свої спостереження внесіть в наступну таблицю:
|
Реагент |
Забарвлення фенолів | ||||
|
фенол |
пірокатехін |
резорцин |
гідрохінон |
пірогалол | |
|
ферум (III) хлорид |
|
|
|
|
|
Дослід 2. Реакція конденсації фенола з реактивом Маркі
Виконання:
1. Приготування реактиву Маркі (розчину формальдегіду в сульфатній кислоті): 0,2 мл формаліну розчиніть в 10 мл концентрованої сульфатної кислоти.
2. На предметне скло помістіть декілька кристалів фенолу та змочіть 1-2 краплями реактива Маркі. При стоянні утворюється вишнево-червоне забарвлення, зумовлене утворенням арилметанового барвника.
Дана реакція використовується для ідентифікації фенолів.
Завдання:
Складіть рівняння реакції конденсації фенолу з формальдегідом.
Дослід 3. Осадження білка фенолом
Виконання:
В пробірку помістіть 1 мл розчину яєчного білка та додайте по краплях насичений водний розчин фенолу. Спостерігається помутніння розчину та утворення згустків, що обумовлено денатурацією білка.
Завдання:
Поясніть, яке явище лежить в основі осадження білка фенолом.
Література
Черных В.П. и др. Общий практикум по органической химии: Учеб. пособ. для студ. вузов III-IV уровней аккредитации / В.П. Черных, И.С. Гриценко, М.О. Лозинский, З.И. Коваленко; Под общ. ред. В.П. Черных X.: Изд-во НФАУ; Золотые страницы, 2002. 592 с.: ил.
Завдання для котролю знань
1. Складіть структурні формули ізомерних ароматичних оксисполук складу С7Н8О та назвіть їх.
2. Складіть рівняння реакцій добування фенолу із хлорбензолу.
3. Складіть рівняння реакцій галогенування фенолу. Назвіть продукти реакції.
4. Складіть рівняння реакцій нітрування фенолу. Назвіть продукти реакції.
5. Визначте масу фенолу, необхідну для приготування 10 кг 2 %-го розчину (за масою) карболової кислоти.
Самостійна робота №6.Багатоатомні феноли. Пірокатехін. Резорцин. Гідрохінон. Пірогалол
I. Тестові питання
1. Укажіть клас органічних сполук, до якого відноситься пірокатехін:
а) спирти;
б) феноли;
в) етери;
г) альдегіди.
2. Укажіть клас органічних сполук, до якого відноситься пірогалол:
а) спирти;
б) феноли;
в) етери;
г) альдегіди.
3. Укажіть назву органічної речовини, яка відноситься до двохоатомних фенолів:
а) о-крезол;
б) м-ксилол;
в) резорцин;
г) пірогалол.
4. Укажіть назву органічної речовини, яка відноситься до трьохоатомних фенолів:
а) гідрохінон;
б) пірокатехін;
в) резорцин;
г) флюроглюцин.
5. Укажіть назву багатоатомного фенолу, який є вихідною речовиною в синтезі лікарського препарату адреналіну:
а) пірокатехін;
б) гідрохінон;
в) резорцин;
г) пірогалол.
II. Вправи для розв’язання
1. Назвати відповідну сполуку за номенклатурою ІЮПАК:
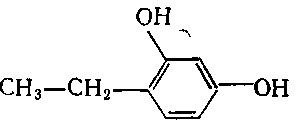
2. Напишіть схеми реакцій резорцину з такими реагентами:
а) NaOH;
б) (CH3CO)2O;
в) Br2 (H2O);
г) Br2(CCl4);
д) HNO3 (конц.);
е) HNO3 (разб.);
є) H2SO4(100ºС).
3. Які якісні реакції можна використати для виявлення:
а) фенолу;
б) резорцину;
в) пірокатехіну;
г) гідрохінону?
Відповідь підтвердіть рівняннями хімічних реакцій.
САМОСТІЙНА РОБОТА №7.Етери. Номенклатура. Фізичні та хімічні властивості. Діетиловий етер
I. Тестові питання
1. Укажіть клас органічних сполук, до якого відноситься етоксиетан:
а) спирти;
б) феноли;
в) естери;
г) етери.
2. Укажіть клас органічних сполук, до якого відноситься метоксибензен:
а) спирти;
б) етери;
в) естери;
г) феноли.
3. Укажіть назву органічної речовини, яка відноситься до етерів:
а) 2-гідроксипропан;
б) 2-етоксипропан;
в) 2-пропанол;
г) 1,2-пропандіол.
4. Укажіть, представники якого класу органічних сполук ізомерні етерам:
а) спирти;
б) феноли;
в) естери;
г) альдегіди.
5. Укажіть спосіб добування етерів:
а) внутрішньомолекулярна дегідратація спиртів;
б) міжмолекулярна дегідратація спиртів;
в) відновлення альдегідів;
г) гідратація алкінів.
II. Вправи для розв’язання
1. Чому етери мають нижчу температуру кипіння у порівнянні з відповідними спиртами? Відповідь пояснити.
2. Складіть структурні формули, що відповідають наступним речовинам. Наведіть назви цих речовин за номенклатурою ІЮПАК. Вкажіть класи органічних сполук, до яких ці речовини належать:
а) етилметиловий етер;
б) диетиловий етер.
3. Напишіть рівняння реакцій, за допомогою яких можна добути:
а) діетиловий етер з натрій етилату та йодетану;
б) диметиловий етер з натрій метилату та йодметану.
4. Напишіть рівняння диметилового етеру з такими реагентами:
а) HCl;
б) HJ;
в) H2SO4 (конц.);
г) O2.
