
- •Практикум
- •Модуль 1. Вуглеводні та їх похідні, що містять атоми галогенів, гідроксильні та карбонільні групи практичні заняття
- •Лабораторні заняття
- •Самостійна робота студента
- •Література Основна
- •Змістовий модуль 1. Вуглеводні та їх галогенопохідні практична робота №1
- •I. Тестові завдання
- •Завдання для самостійного розв’язання:
- •III. Вправи за темою "Добування та властивості алканів" Приклад розв’язання:
- •Завдання для самостійного розв’язання:
- •Метан а в с бутан.
- •IV. Розв’язання задач" Приклади розв’язання:
- •Кількість речовини Карбону, що міститься в спаленому зразку вуглеводню, дорівнює:
- •Відповідь:масова частка виходу продукту нітрометану дорівнює 85%.
- •Особливості конспектування і вимоги до конспекту
- •I. Тестові питання
- •I. Тестові завдання
- •Завдання для самостійного розв’язання:
- •III. Вправи за темою "Добування та властивості алкенів" Приклад розв’язання:
- •Ця реакція використовується для якісного і кількісного визначення сполук, які містять подвійний зв’язок між атомами Карбону.
- •Завдання для самостійного розв’язання:
- •Хлорометанетан а етен 1,2-дибромоетан.
- •IV. "Розв’язання задач" Приклади розв’язання:
- •Самостійна робота №2. Алкадієни. Загальна характеристика. 1,3-Бутадієн. Ізопрен. Застосування 1,3-бутадієну та ізопрену
- •I. Тестові завдання
- •Завдання для самостійного розв’язання:
- •III. Вправи за темою “Добування та властивості алкінів” Приклад розв’язання:
- •Завдання для самостійного розв’язання:
- •IV. “Розв’язання задач” Приклади розв’язання:
- •Згідно рівнянням (I) і (II):
- •Практична робота №4
- •I. Тестові завдання
- •Завдання для самостійного розв’язання:
- •III. Вправи за темою “Добування та властивості аренів” Приклад розв’язання:
- •Завдання для самостійного розв’язання:
- •IV. “Розв’язання задач” Приклади розв’язання:
- •Самостійна робота №3. Окиснення гомологів бензену. Багатоядерні арени.
- •Лабораторна робота № 1
- •Дослід 1. Добування хлороформу з хлоралгідрату
- •Дослід 2. Добування йодоформу
- •Дослід 3. Якісне визначення галогенів (проба Бейльштейна)
- •Література
- •Змістовий модуль 2. Гідроксильні похідні вуглеводнів та карбонільні сполуки лабораторна робота № 2
- •Дослід 1. Взасмодія етанолу з металічним натрієм
- •Література
- •Самостійна робота №4. Багатоатомні спирти. Загальна характеристика. Окремі представники: етиленгліколь та гліцерин, їх ідентифікація в медицині.
- •Лабораторна робота № 3
- •Дослід 1. Дія ферум (III) хлориду на одно- та багатоатомні феноли
- •Дослід 2. Реакція конденсації фенола з реактивом Маркі
- •Дослід 3. Осадження білка фенолом
- •Література
- •Самостійна робота №6.Багатоатомні феноли. Пірокатехін. Резорцин. Гідрохінон. Пірогалол
- •Лабораторна робота № 4
- •Дослід 1
- •Дослід 4 Окиснення формальдегіду купрум (II) гідроксидом в лужному середовищі (проба Троммера)
- •Дослід 5
- •Модуль 2. Органічні сполуки, що містять карбоксильні групи, атоми Нітрогену; гетерофункціональні та гетероциклічні сполуки лабораторні заняття
- •Самостійна робота студента
- •Література Основна
- •Додаткова
- •Змістовий модуль 3 лабораторна робота № 5
- •Дослід 1. Відношення карбонових кислот до дії окисників
- •Дослід 2. Підтвердження наявності альдегідної групи в молекулі форміатної кислоти
- •Дослід 3. Розчинність бензенової кислоти у лугах
- •Дослід 4. Якісні реакції на ацетат- та бензоат-іони
- •Дослід 5. Возгонка бензенової кислоти (“зимовий сад”)
- •Література
- •Лабораторна робота № 6
- •Дослід 1. Доказ наявності двох карбоксильних груп у молекулі оксалатної кислоти (одержання калієвих солей)
- •Дослід 2. Якісна реакція на оксалат-іон
- •Лабораторна робота № 7
- •Дослід 1. Утворення нітрату сечовини
- •Дослід 2. Гідроліз сечовини
- •Дослід 3. Утворення та виявлення біурету
- •Література
- •Дикарбонові кислоти. Щавлева кислота
- •Дослід 2. Лігнінова проба
- •Дослід 3. Окиснення аніліну
- •Література
- •Завдання для котролю знань
- •Лабораторна робота № 9
- •Дослід 1. Доказ будови тартратної кислоти
- •Дослід 2. Розкладання цитратної кислоти під дією концентрованої сульфатної кислоти
- •Дослід 3. Визначення лактатної кислоти в молочній сироватці
- •Література
- •Завдання для котролю знань
- •Лабораторна робота № 10
- •Дослід 1. Розчинність саліцилової кислоти у воді, спирті, лугах
- •Дослід 2. Доведення наявності фенольного гідроксилу в саліциловій кислоті
- •Дослід 3. Гідроліз ацетилсаліцилової кислоти та фенілсаліцилату (салолу)
- •Література
- •Самостійна робота №10.Фенолокислоти. Будова фенолокислот. Саліцилова кислота: будова, хімічні властивості. Фізіологічний вплив на організм людини. Ацетилсаліцилова кислота. Фенілсаліцилат
- •I. Тестові питання
- •II. Вправи для розв’язання
- •Самостійна робота №11.Поняття про пептиди та білки. Структури білків
- •Дослід 2. Відсутність відновлючої здатності у сахарози
- •Дослід 3. Кислотний гідроліз крохмалю
- •Література
- •Завдання для котролю знань
- •Самостійна робота №12.Вуглеводи.Поняття про полісахариди
- •I. Тестові питання
- •II. Вправи для розв’язання
- •II. Вправи для розв’язання
- •I. Тестові питання
- •II. Вправи для розв’язання
- •71. Укажіть структурну формулу малонової кислоти:
- •107. Укажіть назву органічної сполуки, яка належить до дисахаридів:
- •120. Укажіть назву органічної сполуки, яка належить до пятичленних гетероциклів з двома гетероатомами:
- •141. Установіть відповідність між хімічними формулами та класами органічних сполук:
- •161. Установіть послідовність розташування гомологів у гомологічному ряді одноосновних насичених карбонових кислот:
Лабораторна робота № 7
Тема роботи: Утворення нітрату сечовини. Гідроліз сечовини. Утворення та виявлення біурету.
Мета роботи: Експериментально здійснити зазначені досліди.
Дослід 1. Утворення нітрату сечовини
Виконання:
В пробірку внесіть 2-3 мл концентрованого розчину сечовини, додайте такий самий об'єм концентрованого розчину нітратної кислоти. Вміст пробірки збовтайте. Оскільки він нагрівається, його треба охолодити холодною водою або льодом. Після охолодження реакційної суміші випадає осад — нітрат сечовини. Якщо взяти невелику кількість осаду і помістити на предметне скло, то під мікроскопом можна побачити кристали цієї солі.
Завдання:
Складіть рівняння реакції одержання нітрату сечовини.
Дослід 2. Гідроліз сечовини
Виконання:
Вмістіть у пробірку 1 шпатель сечовини. Додайте 5-6 крапель баритової води. Треба наливати баритову воду так, щоб не замочити пробірку зверху (можна по скляній паличці). Закоркуйте пробірку, але не щільно, бо при нагріванні розчину корок вискочить із пробірки. Між корком та стінкою пробірки вставити вузьку смужку червоного лакмусового паперу. Поставте пробірку у нагріту до кипіння водяну баню. Через 15-20 хвилин зверніть увагу на посиніння червоного лакмусового паперу.
Завдання:
Складіть рівняння реакції гідролізу сечовини.
Дослід 3. Утворення та виявлення біурету
Виконання:
Помістіть у суху пробірку 1 шпатель сечовини. Нагрійте обережно над полум'ям пальника. Сечовина спочатку починає плавитись, спостерігається часткова сублімація ціанату амонію. Через кілька секунд починається виділення бульбашок газу ‑ амоніаку (легко розітнати за запахом).
Невдовзі виділення амоніаку припиняється і реакційна маса твердіє при нагріванні внаслідок утворення нових речовин: біурету та ціанурової кислоти. Охолодивши пробирку, додайте у неї 5-6 крапель води та прокип'ятити протягом 2-3 хв. При цьому біурет, що легше розчинюється, перейде у розчин. Дати відстоятися осаду ціанурової кислоти , що важко розчиняється. Обережно злитйте розчин біурету в іншу пробірку та додатйте до нього 2 краплини NaOH. При цьому незначна каламуть від слідів ціанурової кислоти пропаде. Додати 1 краплю розчину купрум (II) сульфату. З'являється рожево - фіолетове забарвлення комплексної солі біурету (біуретова реакція).
Біуретова реакція ‑ одна з кольорових реакцій на білок та поліпептиди. До осаду ціанурової кислоти, що залишився у пробірці, додайте 2-3 краплі розчину амоніаку, енергійно струсіть та додайте 1 краплю розчину купрум(II) сульфату. Утворюється осад бузкового кольору комплексної мідної солі ціанурової кислоти.
Завдання:
Складіть рівняння відповідних реакцій.
Література
Черных В.П. и др. Общий практикум по органической химии: Учеб. пособ. для студ. вузов III-IV уровней аккредитации / В.П. Черных, И.С. Гриценко, М.О. Лозинский, З.И. Коваленко; Под общ. ред. В.П. Черных X.: Изд-во НФАУ; Золотые страницы, 2002. 592 с.: ил.
Завдання для котролю знань
1. Записати хімізм процесу добування нітрату сечовини.
2. Записати хімізм процесу гідролізу сечовини.
3. Визначити рівняння хімічної реакції одержання біурету.
4. Записати хімізм процесу гідролізу сечовини.
САМОСТІЙНА РОБОТА №8.Монокарбонові кислоти. Окремі представники:
мурашина, оцтова, бензенова
I. Тестові питання
1. Укажіть продукти нагрівання мурашиної кислоти з концентрованою H2SO4:
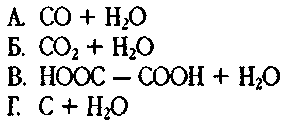
2. Укажіть продукти окиснення мурашиної кислоти:

3. Укажіть речовину, з якою реагує оцтова кислота:
а) метан;
б) натрій гідроксид;
в) мідь;
г) калій хлорид.
4. Укажіть назву карбонової кислоти, яка виявляє найсильніші кислотні властивості:
а) масляна;
б) мурашина;
в) оцтова;
г) пропіонова.
5. Особливістю метанової кислоти є взаємодія з:
а) лужними металами;
б) лугами;
в) основними оксидами;
г) реактивом Толленса.
II. Вправи для розв’язання
1. Напишіть структурні формули наступних сполук:
а) аміду мурашиної кислоти;
б) хлорангидриду оцтової кислоти;
в) п-амінобензенової кислоти.
2. Напишіть рівняння реакцій взаємодії:
а) оцтової кислоти з 2-пропанолом;
б) метилового естеру мурашиної кислоти з водним розчином натрій гідроксиду.
в) мурашиної кислоти з пентахлоридом фосфору;
г) бензенової кислоти з натрій гідроксидом.
Назвіть продукти реакцій та вкажіть класи органічних сполук, до яких вони належать.
3. У якому з рядів усі речовини реагуватимуть з етановою кислотою:
а) H2O, Cl2, HCl;
б) Cl2, C2H5OH, NaOH;
в) Ag2O, H2, Na2CO3.
Напишіть рівняння реакцій.
4. Напишіть рівняння реакції етерифікації оцтової кислоти метиловим, етиловим, ізопропіловим та втор-бутиловим спиртами. Наведіть механізм реакції. Назвіть добуті сполуки. Поясніть роль концентрованої сульфатної кислоти. Напишіть рівняння реакції кислотного гідролізу добутих естерів.
