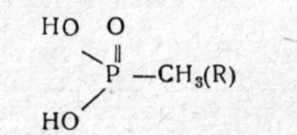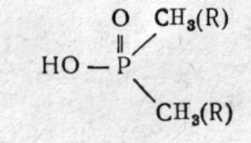- •Н.И.Каракчиев
- •© Издательство «Медицина, УзСср, 1988
- •Предисловие
- •Раздел I
- •1.2. Средства применения отравляющих веществ
- •1.3. Физико-химические свойства отравляющих веществ
- •1.4. Классификация отравляющих веществ
- •1.5. Боевые поражающие свойства химического оружия
- •1.6. Факторы, определяющие эффективность химического оружия
- •1.7. Медико-тактическая характеристика очага химического заражения
- •1.8. Предмет и задачи военной токсикологии
- •1.9. Пути поступления отравляющих веществ в организм
- •1.10. Механизм действия отравляющих веществ
- •1.11. Патогенез развития клиники поражения
- •1.12. Цитогенетическое, тератогенное и бластомогенное действие ядов
- •1.13. Методы токсикологических исследовании. Характеристика токсичности ов
- •1.14. Организация профилактики и лечения пораженных ов
- •1.15. Антидотное лечение
- •Глава 2. Фосфорорганические отравляющие вещества (ов нервно-паралитического действия)
- •2.1 Физико-химические и токсические свойства
- •2.2. Механизм действия и патогенез поражения
- •Анионный участок Эстерозный участок
- •Патофизиологические эффекты действия фов, связанные с накоплением ацетилхолина в синапсах и возбуждением холинорецепторов
- •2.3. Клиника поражения
- •2.4. Патологоанатомические изменения
- •2.5. Диагностика поражений фов
- •2.6. Антидоты фов
- •2.7. Симптоматические и патогенетические средства
- •2.8. Первая медицинская помощь
- •2.9. Помощь на этапах медицинской эвакуации
- •Глава 3. Отравляющие вещества общеядовитого действия
- •3.1. Синильная кислота и хлорциан
- •3.1.2. Механизм действия и патогенез поражения
- •3.1.3. Клиника поражения
Глава 2. Фосфорорганические отравляющие вещества (ов нервно-паралитического действия)
Фосфорорганические ОВ (ФОВ) являются в настоящее время самыми опасными веществами быстрого и смертельного действия в арсенале химического оружия зарубежных империалистических армий. Вот почему на их изучение обращается особое внимание.
Впервые они появились в фашистской Германии в годы второй мировой войны. Синтез их был осуществлен в лабораториях Фарбениндустри Шрадером. В 1937г. синтезирован табун, в 1938г.— зарин и в 1944г.— зоман. Был налажен массовый выпуск этих ОВ. В Англии в эти годы синтезирован диизопропилфторфосфат и введен на вооружение как штатное ОВ.
В 50-х годах шведский химик Таммелин синтезировал высокотоксичные аминотиоловые эфиры фосфоновых кислот, на основании которых в США с 1955г. на вооружении появились наиболее высоко токсичные ОВ под условным названием V-газы (вигазы). На вооружении стран НАТО состоят зарин, зоман, V-газы и др.
Фосфорные соединения являются жизненно необходимыми для организма веществами, в частности аденозинтрифосфорная кислота (АТФ) — одно из основных макроэргических соединений, обеспечивающих энергоресурсы организма. В то же время фосфорорганические эфиры являются высокотоксичными веществами нервно-парадитдщесдого действия. В настоящее время синтезировано около 12 тысяч фосфорорганических соединений (ФОС) типа эфиров различных фосфорсодержащих кислот. Многие из них нашли широкое применение в качестве инсектицидов для уничтожения насекомых-вредителей сельскохозяйственных культур и в системе санитарно-противоэпидемических станций; некоторые эфиры применяются в медицине в качестве лекарств, а ряд соединений состоят на вооружении как ОВ.
Особая опасность ФОВ объясняется следующими характерными свойствами этих соединений: 1) они являются наиболее токсичными среди всех ОВ; 2) могут проникать в организм всеми возможными путями, в том числе через кожу, что затрудняет защиту от них; 3) многие из них не имеют цвета и запаха, практически трудно обнаруживаются органами чувств (их можно обнаружить только химическими реакциями) и момент поражения может проходить незаметно; 4) обладают значительной стойкостью на местности; 5) могут вызывать так называемую молниеносную форму поражения, когда смерть наступает в первые 5—10 мин. на поле боя до получения необходимой медицинской помощи. Эти обстоятельства приводят к выводу, что ФОВ могут вызывать массовые потери войск и населения с высокой, смертностью пораженных.
2.1 Физико-химические и токсические свойства
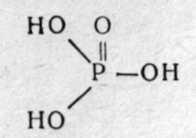
Фосфорорганические соединения (ФОС) по своей химической структуре могут быть производными фосфорной (фосфаты), алкилфосфоновой (фосфонаты), диалкилфосфиновой (фосфинаты), тиофосфорной кислот (тиофосфаты) и других производных фосфорных кислот:
|
|
|
|
|
Фосфорная кислота (эфиры называют фосфатами)
|
Алкилфосфоновая кислота (одна фосфоруглеродная связь; эфиры называют фосфонатами)
|
Диалкилфосфиновая кислота (две фосфоруглеродные связи, эфиры называют фосфинатами)
|
Зарин (gВ) — изопропиловый эфир метилфторфосфоновой кислоты:
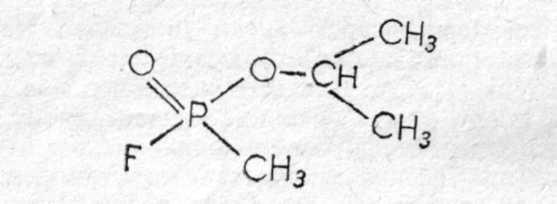
Физические свойства. Зарин — бесцветная жидкость, практически без запаха (некоторые отмечают слабый фруктовый запах). Температура кипения 158°С (при кипении разлагается), поэтому обладает значительной летучестью (при 20°—13,2 мг/л воздуха) и сравнительно небольшой стойкостью (летом на местности держится до 10 ч). Температура плавления (затвердевания) —56°С, может применяться в зимних условиях. Молекулярная масса 140,1; плотность 1,094 (тяжелее воды); плотность паров по воздуху 4,86. Зарин хорошо растворяется в жирах, липидах и органических растворителях (дихлорэтан, бензол, бензин, спирт и др.) и сравнительно хорошо растворяется в воде. Проникает через кожные покровы в капельно-жидком и парообразном состоянии.
Химические свойства. Наиболее подвижной и реакционно способной является фторфосфорная связь, поэтому по этой связи легче всего идут химические и биохимические реакции зарина. Зарин гидролизуется водой, но медленно (при комнатной температуре на 50% гидролизуется за 5 ч), при этом образуются значительно менее токсичная фтористоводородная кислота и нетоксичный остаток.

Гидролиз зарина резко ускоряется при добавлении щелочных веществ и кипячении. Зарин легко разрушается и дегазируется щелочными веществами, аммиаком:
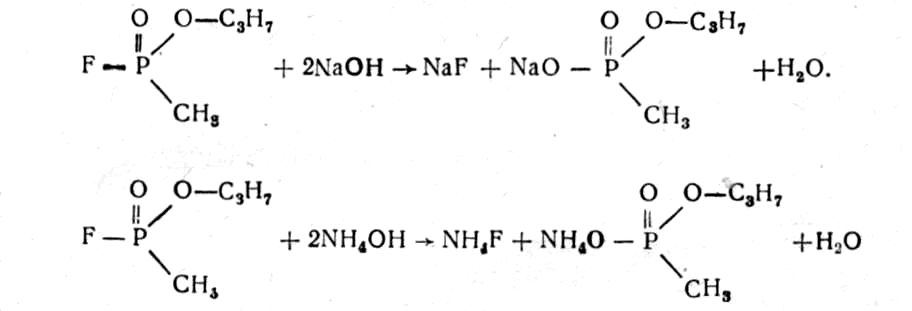
Для дегазации, предметов, зараженных зарином, применяются 5% растворы едких щелочей, 25% раствор аммиака, или аммиачно-щелочной раствор № 2-ащ и др.
3оман, (gD) — пинаколиновый эфир метилфторофосфоновой кислоты. Представляет собой бесцветную жидкость, практически без запаха (некоторые отмечают слабый камфорный запах).
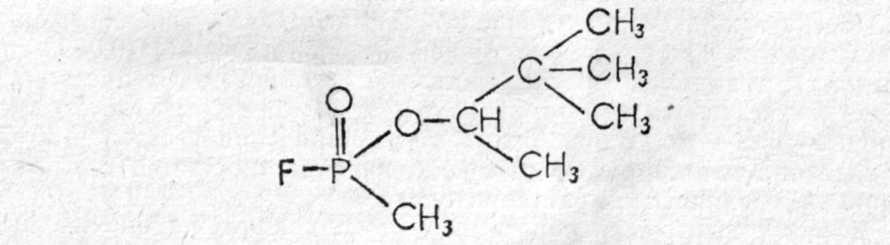
Физические свойства. Температура кипения зомана около 200°С (с разложением), относится к стойким ОВ (стойкость летом около суток). Температура затвердевания —80°С (по другим данным —42°С). Молекулярная масса 182; плотность, 1,013; плотность паров по воздуху 6,3. Хорошо растворяется в жирах, липидах, органических растворителях; в воде растворяется умеренно. Хорошо проникает через кожу человека и животных.
Химические свойства близки к свойствам зарина (реакции по Р—F связи), но в воде гидролизуется очень медленно (в холодной воде может держаться месяцами). Дегазируется также щелочными веществами.
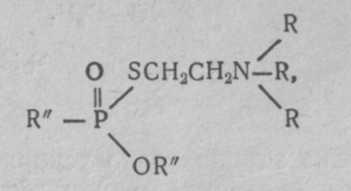
V-газы. Под этим названием объединяют различные соединения с общей формулой:
|
|
|
где R' —алкильный радикал, ОR" — алкильный эфир, R —два или три алкильных радикала. Известно около 15 таких соединений, отличающихся радикалами. Более токсичным и вероятным ОВ считается О-этил-S-диизопропиламиноэтил-метилфосфонотионат (Vх ):
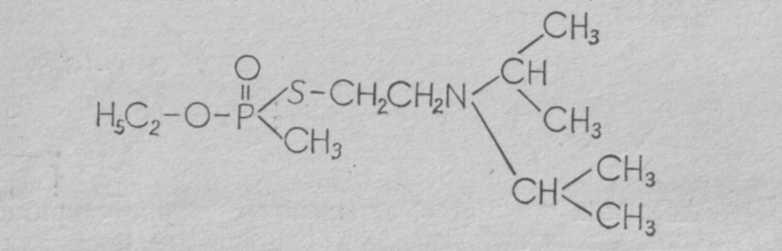
V-газы являются аминотиоловыми эфирами фосфоновых кислот, причем аминотиоловая группа содержит две СН2-группы, как и ацетилхолин. Возможно этим объясняется более высокая токсичность V-газов.
Физические свойства. V-газы представляют собой бесцветную жидкость без запаха. Температура кипения около 300°С, поэтому они обладают очень малой летучестью (0,003 мг/л воздуха) и наибольшей стойкостью на местности. Стойкость V-газов на местности при температуре 15°С может быть до 20 сут, а при —10°С — до 16 нед. Температура плавления V-газов —50°С. В воде они растворяются до 5%, хорошо растворяются в жирах, липидах, органических растворителях.
Характерными особенностями V-газов являются наиболее высокая по сравнению с другими ОВ токсичность и способность хорошо проникать через кожу, вызывая поражения в минимальных дозах. В США предлагают применять V-газы главным образом в аэрозольном состоянии или капельно-жидком виде для создания стойких очагов химического заражения.
Химические свойства. V-газы гидролизуются водой очень медленно. Дегазируются легче веществами, содержащими активный хлор (гипохлоритом кальция), труднее — щелочными веществами.
Бинарные ФОВ. Как уже сообщалось, в США создается бинарное химическое оружие. Внутри бинарного боеприпаса (артхимснаряда или бомбы) в отдельности находятся два неядовитых компонента, разделенных перегородкой. При выстреле или резком ударе перегородка разрушается, компоненты соединяются и реагируют с образованием зарина или V-газов, не отличающихся в принципе от собственно зарина или V-газов. В качестве компонентов для зарина могут быть использованы фтор-хлоран-гидрид-метилфосфоната и изопропиловый спирт:
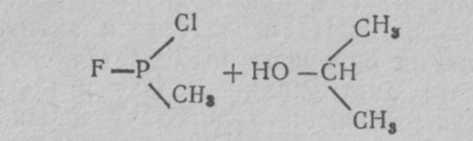
Бинарные ФОВ в США условно получили название gВ-2 и Vх -2.
Фосфорорганические инсектициды широко применяются в сельском хозяйстве и дезстанциях для уничтожения насекомых и вредителей: дихлофос (аэрозоль), хлорофос, карбофос, тиофос и др. При неправильном обращении с ним могут быть тяжелые и смертельные отравления, по клинике мало отличающиеся от поражений ФОВ.
Способы боевого применения. ФОВ могут применяться в химических ракетах, бомбах, артхимснарядах и минах, реактивных химических снарядах, химических фугасах и путем распыления с самолетов из выливных авиационных приборов и различных генераторов аэрозолей.
Токсические свойства. Как уже указывалось, ФОВ являются высокотоксичными веществами (ультраяды) быстрого и смертельного действия. Токсичность их при разных путях поступления в организм на основании обобщения данных литературы представлена в табл. 3 (В. В. Мясников, С. Н. Голиков и др.).
Таблица 3
Токсичность ФОВ
|
Название ОВ
|
Концентрация при ингаляционном поражении, мг/л воздуха, экспозиция 1 мин |
LD50 при попадании в капельном виде | ||||
|
абсолютно смертельная (СL100) |
условно смертельная (СL50) |
средневыводя-щая (IС50) |
вызывающая миоз |
на кожу, мг/кг |
на обмундиро-вание, мг/кг | |
|
V-газы Зоман Зарин |
0,007 0,075 0,1 |
0,001 ,05 0,07 |
0,025 0,055 |
0,0001 0,002 |
0,05—0,1 0,7 5 |
4—5 5 25 |
При длительных экспозициях ФОВ могут вызывать тяжелые поражения в концентрациях 0,0001—0,001 мг/л воздуха. Например, зарин в концентрации 0,001 мг/л при экспозиции 15 мин может вызвать тяжелое поражение. Для создания смертельных концентраций в атмосфере, по данным зарубежных специалистов, достаточно заражать территорию с плотностью заражения 0,1— 0,2 г на 1 м2 поверхности. При попадании на кожу V-газы в дозе 5—10 мг (то есть мельчайшей капельки в 10 раз меньше капли воды) могут вызвать тяжелое поражение человека.