
- •Н.И.Каракчиев
- •© Издательство «Медицина, УзСср, 1988
- •Предисловие
- •Раздел I
- •1.2. Средства применения отравляющих веществ
- •1.3. Физико-химические свойства отравляющих веществ
- •1.4. Классификация отравляющих веществ
- •1.5. Боевые поражающие свойства химического оружия
- •1.6. Факторы, определяющие эффективность химического оружия
- •1.7. Медико-тактическая характеристика очага химического заражения
- •1.8. Предмет и задачи военной токсикологии
- •1.9. Пути поступления отравляющих веществ в организм
- •1.10. Механизм действия отравляющих веществ
- •1.11. Патогенез развития клиники поражения
- •1.12. Цитогенетическое, тератогенное и бластомогенное действие ядов
- •1.13. Методы токсикологических исследовании. Характеристика токсичности ов
- •1.14. Организация профилактики и лечения пораженных ов
- •1.15. Антидотное лечение
- •Глава 2. Фосфорорганические отравляющие вещества (ов нервно-паралитического действия)
- •2.1 Физико-химические и токсические свойства
- •2.2. Механизм действия и патогенез поражения
- •Анионный участок Эстерозный участок
- •Патофизиологические эффекты действия фов, связанные с накоплением ацетилхолина в синапсах и возбуждением холинорецепторов
- •2.3. Клиника поражения
- •2.4. Патологоанатомические изменения
- •2.5. Диагностика поражений фов
- •2.6. Антидоты фов
- •2.7. Симптоматические и патогенетические средства
- •2.8. Первая медицинская помощь
- •2.9. Помощь на этапах медицинской эвакуации
- •Глава 3. Отравляющие вещества общеядовитого действия
- •3.1. Синильная кислота и хлорциан
- •3.1.2. Механизм действия и патогенез поражения
- •3.1.3. Клиника поражения
Глава 3. Отравляющие вещества общеядовитого действия
К ОВ общеядовитого действия относятся синильная кислота и хлорциан. Несмотря на то, что применение синильной кислоты французской армией в первую мировую войну было не эффективным, она привлекает внимание военных химиков капиталистических армий главным образом потому, что может вызывать очень быстрое развитие клиники поражения и гибель в течение нескольких минут на поле боя.
В данной главе рассматриваются также вопросы токсикологии окиси углерода, хотя она не состоит на вооружении в качестве ОВ, но отравления ею возможны как в боевых, так и в мирных условиях. В заключение дается краткое описание токсикологии диоксина, который применялся армией США в Южном Вьетнаме в составе «оранжевого агента».
3.1. Синильная кислота и хлорциан
Синильная кислота и хлорциан состоят на вооружении ряда капиталистических армий в качестве нетабельных (запасных) ОВ. Кроме того, синильная кислота и се соли (цианиды) находят широкое применение в промышленности (для извлечения золота и серебра из руд, золочения и серебрения предметов, крашения и протравливания тканей и т. д.), в сельском хозяйстве и на транспорте для дезинсекции и дератизации и т. п. Поэтому они производятся в большом количестве и могут быть отравления при производстве, транспортировке и использовании синильной кислоты и цианидов. Отравления могут быть при употреблении ядер (семян) косточек горького миндаля, абрикосов, персиков, вишен, слив, груш и других, содержащих глюкозид амигдалнн, в состав которого входит цианистая группа.
3.1.1. ФИЗИКО-ХИМИЧЕСКИЕ И ТОКСИЧЕСКИЕ СВОЙСТВА Синильная кислота (НCN) — бесцветная летучая жидкость с запахом горького миндаля. Температура кипения 26°С, поэтому она быстро испаряется и относится к типичным нестойким ОВ (стойкость на местности в летнее время 20–30 мин). Температура замерзания—14°С. Плотность паров 0,93, то есть пары ее легче воздуха. Синильная кислота хорошо растворяется в воде и органических растворителях, фосгене, иприте и других ОВ.
Синильная кислота, как и другие кислоты, со щелочами образует соли, цианиды; НCN + КОН→КCN + Н2O; НCN + NаОН→NаCN + H2О и др.
Цианиды — это твердые кристаллические вещества, очень ядовитые (смертельная доза при приеме внутрь около 150 мг). С солями железа, кобальта и других тяжелых металлов синильная кислота образует стойкие комплексные соли, К4[Fе(СN)6]; К4[Fе(СN)6]; К4[Аu(СN)6], К4[Со(СN)6] и другие, которые в обычных условиях неядовиты.
Синильная кислота легко присоединяется к альдегидам, например, к формальдегиду, с образованием сравнительно малотоксичиых оксинитрилов (циангидринов), а также к глюкозе (ее альдегидной группе):
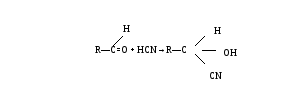
Синильная кислота и цианиды могут вступать в реакцию с активными соединениями серы с образованием малотоксичных роданидов:
НСN + S → НCNS (КСNS, NаСNS).
Синильная кислота легко реагирует с галогенами с образованием галоидцианов: CLCN, ВгCN, FCN, JCN, из которых хлорциан состоит на вооружении как ОВ.
Хлорциан, (СLСN) — бесцветная жидкость с резким раздражающим запахом. Температура кипения 13,4°С; обладает высокой летучестью и поэтому еще меньшей стойкостью. Пары его в два раза тяжелее воздуха. Остальные свойства аналогичны синильной кислоте.
Токсичность. Синильная кислота и хлорциан вызывают главным образом ингаляционные поражения. Опасными для человека являются пары синильной кислоты в концентрации 0,1–0,12 мг/л, которые при экспозиции 15–20 мин вызывают тяжелое поражение. Смертельными считаются концентрации 0,2–0,3 мг/л при экспозиции 5–10 мин; 0,4–0,8 мг/л при экспозиции 2–5 мин вызывают быструю смерть.
Пары хлорциана несколько менее токсичны: 0,4–0,8 мг/л вызывают смертельное поражение при экспозиции 5 мин.
