
- •Предмет колоїдної хімії
- •Класифікація колоїдних систем
- •Класифікація дисперсних систем за агрегатним станом дисперсної фази та дисперсійного середовища.
- •Контрольні питання:
- •Поверхневі явища та їх класифікація
- •Класифікація поверхневих явищ
- •Поверхневий натяг
- •Поверхневий натяг деяких речовин на межі з повітрям при 298к.
- •Методи визначення поверхневого натягу
- •Метод капілярного підняття (метод Жюрена).
- •Метод максимального тиску в бульбашці (метод Ребіндера)
- •Сталометричний метод (метод Траубе)
- •Внутрішня (повна) питома поверхнева енергія. Залежність енергетичних параметрів поверхні від температури
- •Принципи формування поверхневого шару
- •Поверхневий натяг органічних речовин на межі з повітрям при 298к.
- •Адгезія, когезія
- •Змочування і розтікання
- •Розтікання рідин. Ефект Марангоні
- •Контрольні питання:
- •Дисперсність і властивості тіл
- •Характеристика величини і форми поверхні
- •Зміна питомої поверхні при подрібненні речовини.
- •Вплив дисперсності на внутрішній тиск
- •Капілярні явища
- •Дисперсність і реакційна здатність речовин
- •Тиск насиченої пари над викривленою поверхнею
- •Вплив дисперсності на температуру фазового переходу
- •Залежність температури топлення калію і срібла від дисперсності.
- •Вплив дисперсності на розчинність твердих тіл
- •Вплив дисперсності на рівновагу хімічних реакцій
- •Контрольні питання:
- •Адсорбційні рівноваги.
- •Основні поняття та визначення.
- •Природа адсорбційних сил
- •Фундаментальне рівняння адсорбції Гіббса
- •Теплота адсорбції.
- •Швидкість фізичної адсорбції
- •Адсорбція газів на однорідній твердій поверхні.
- •Ізотерма адсорбції (закон) Генрі
- •Теорія адсорбції Ленгмюра
- •Теорія полімолекулярної адсорбції бет
- •Адсорбція газів на пористих тілах
- •Класифікація пористих тіл
- •Теорія капілярної конденсації
- •Теорія об’ємного заповнення мікропор
- •Адсорбція на межі тверде тіло – рідкий розчин.
- •Молекулярна адсорбція
- •Іонна адсорбція
- •Адсорбція поверхнево активних речовин з розчину на межі рідина – газ
- •Контрольні питання.
- •Електричні явища на поверхні
- •Поняття про електрокінетичні явища
- •Механізм утворення подвійного електричного шару
- •Термодинамічні співвідношення між поверхневим натягом і електричним потенціалом
- •Теорії будови подвійного електричного шару.
- •Теорія Гельмгольца Перрена.
- •Теорія Гуї - Чепмена
- •Теорія Штерна.
- •Вплив електролітів на подвійний електричний шар.
- •Вплив індиферентних електролітів на подвійний електричний шар.
- •Вплив неіндиферентних (родинних) електролітів
- •Експериментальне визначення електрокінетичного потенціалу
- •Контрольні питання.
- •Методи одержання та очистки колоїдних систем
- •Диспергаційні методи
- •Конденсаційні методи
- •Термодинаміка утворення нової фази при конденсації.
- •Кінетика утворення нової фази
- •Будова міцел
- •Методи очистки колоїдних розчинів
- •Контрольні питання.
- •Агрегативна стійкість дисперсних систем.
- •Фактори агрегативної стійкості ліофобних дисперсних систем.
- •Ізотермічна перегонка в дисперсних системах.
- •Коагуляція.
- •Теорія стійкості дисперсних систем Дєрягіна, Ландау Фервея і Овербека
- •Кінетика коагуляції
- •Контрольні питання
- •Властивості дисперсних систем
- •Молекулярно – кінетичні властивості дисперсних систем
- •Броунівський рух
- •Дифузія.
- •Седиментація та седиментаційна стійкість.
- •Седиментаційний аналіз дисперсності.
- •Оптичні властивості дисперсних систем.
- •Розсіювання світла.
- •Абсорбція світла.
- •Оптичні методи дослідження дисперсних систем.
- •Структурно-механічні властивості дисперсних систем.
- •Реологічних моделі тіл.
- •Розчини поверхнево – активних речовин.
- •Класифікація пар.
- •Міцели пар.
- •Розчини високомолекулярних сполук
- •Утворення і властивості вмс
- •Взаємодія вмс з розчинниками.
- •Молекулярна маса вмс
- •ГрубоДисперсні системи.
- •Суспензії
- •Емульсії.
- •Класифікація та властивості емульсій.
- •Одержання та руйнування емульсій.
- •Основні характеристики та властивості пін.
- •Одержання та руйнування пін.
- •Аерозолі
- •Класифікація та властивості аерозолів
- •Методи одержання та практичне значення аерозолів
- •Порошки
- •Список літератури
Термодинаміка утворення нової фази при конденсації.
В процесі конденсації нова фаза утворюється на поверхнях, які вже існують - гетерогенна конденсація, або на поверхні зародків, що виникають самочинно в результаті флуктуації концентрації і густини в рідині або парі – гомогенна.
Конденсація, як правило, відбувається на поверхні центрів конденсації або зародків, що мають дуже маленькі розміри, в наслідок чого їх реакційна здатність значно вища за реакційну здатність макрофази. Для того, щоб процес конденсації продовжувався необхідне пересичення пари або рідини в якій відбувається конденсація. В іншому випадку зародки, що утворюються, будуть розчинятись або випаровуватись.
Перегрітий, переохолоджений, пересичений стани називають метастабільними. Їх характеризують ступенем пересичення.
= p/ps, = x/xs ( 6.0)
де ps – тиск насиченої пари,
xs – розчинність макрофази.
Існування метастабільних станів можна пояснити тим, що пара може бути пересиченою по відношенню до плоскої поверхні і ненасиченою по відношенню до краплин.
Ступінь пересичення, при якому пара стає насиченою по відношенню до краплин називається критичним.
При <кр зародки самочинно виникають і відразу зникають.
При =кр виникає нестійка рівновага, при якій число зародків, що виникають дорівнює числу зародків, що зникають.
При >кр відбувається процес виникнення і росту зародків.
Розглянемо зміну енергії Гіббса на межі рідина-пара при утворенні зародку як функцію його радіуса. В найпростішому випадку вона має об’ємну і поверхневу складові.
G = GV + GS = V/VM(р – п) + s ( 6.0)
де р, п - хімічний потенціал рідини та пари відповідно;
VМ - мольний об`єм пари;
V – об’єм зародка.
Конденсація може відбуватися за умови, що р < п.
Якщо зародки, що утворюються мають сферичну форму, то:
 ( 6.0)
( 6.0)
Проаналізуємо одержану залежність на наявність екстремуму:
 ( 6.0
( 6.0
![]() (
6.0)
(
6.0)
Якщо записати хімічні потенціали рідини та пари через відповідні тиски пари, отримуємо:
![]() (
6.0)
(
6.0)
тобто умова екстремуму співпадає з рівнянням Кельвіна.
Проведемо аналіз другої похідної функції.
![]() ( 6.0)
( 6.0)
![]() ( 6.0)
( 6.0)
Від’ємний знак другої похідної означає, що залежність зміни енергії Гіббса при утворенні зародку від радіуса має максимум (рис.48). Максимальна енергія Гіббса і радіус, що їй відповідає, називають критичними.
Поведінку зародків в системах, що знаходяться в метастабільному стані легко зрозуміти з графіка. Оскільки Gкр знаходиться в максимумі, то і при r>rкр і при r<rкр енергія Гіббса зменшується. Це означає, що в усіх випадках будуть відбуватися самочинні процеси.
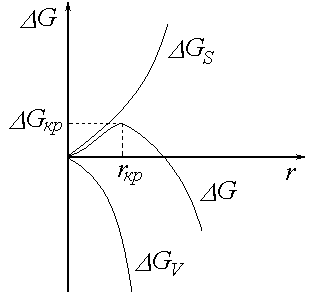
Рис. 48. Залежність енергії Гіббса утворення зародку від його радіусу.
При виникненні зародків з радіусом меншим від rкр в пересиченій парі зародки, що виникають самочинно відразу випаровуються (розчиняються). При виникненні зародків з розміром r=rкр ймовірність виникнення і зникнення зародків однакова, тому число зародків, що виникає, дорівнює числу зародків, що зникає. Отже існує нестійка рівновага. При виникненні зародків з r>rкр відбувається ріст зародків.
Критична енергія Гіббса утворення зародку дорівнює
![]() (6.0)
(6.0)
Таким чином, критична енергія Гіббса утворення зародку дорівнює 1/3 поверхневої енергії.
Підстановка критичного радіуса, вираженого з рівняння Кельвіна в рівняння для розрахунку Gкр приводить до виразу:
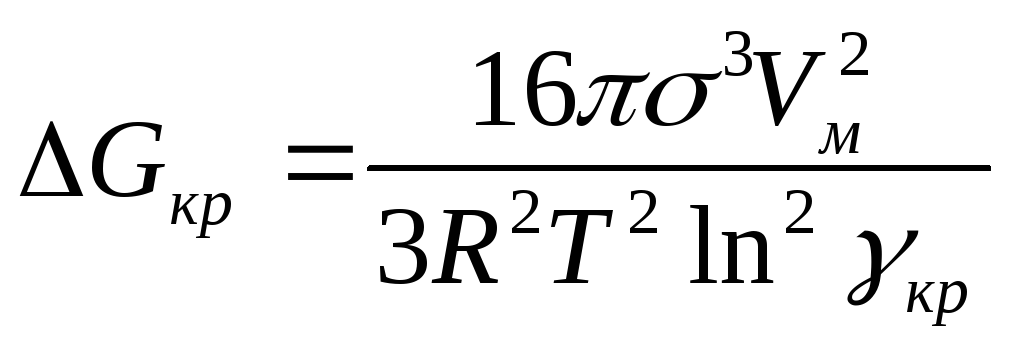 (
6.0)
(
6.0)
Чим вища ступінь пересичення і температура і менший поверхневий натяг, тим менша критична енергія Гіббса утворення зародку.
Розглянуті залежності дозволяють зробити деякі узагальнення про термодинаміку утворення зародків. Конденсація пари в рідину починається з утворення краплин, а рідини в тверду фазу з утворення кристалічних зародків. Але наявність додаткової поверхневої енергії на межі такої неоднорідності робить процес утворення зародків енергетично невигідним, якщо розміри зародку недостатньо великі. Енергія утворення зародку складається з двох конкурентних складових – програшу в поверхневій енергії і виграшу в об’ємній при переході речовини в нову фазу. Другій фактор збільшується з ростом зародків швидше ніж перший і стає, в решті решт, переважаючим. Можна сказати, що утворення зародка нової фази вимагає переходу через своєрідний „потенційний бар’єр”, пов’язаний з поверхневою енергією, що можливо лише для досить крупного зародка.
