
d592cd77_klinicheskie_lektsii_chast_vtoraya
.pdfВдиагностике важное значение имеет указание на недавние роды. В зависимости от фазы течения заболевания при гормональном исследовании выявляется тиреотоксикоз или гипотиреоз. Как правило, обнаруживается повышенный титр АТ-ТПО. Антитела к рецептору ТТГ в клинически значимых количествах не
выявляются. При УЗИ определяется диффузное или мультифокальное снижение эхогенности, при сцинтиграфии ЩЖ – диффузное снижение захвата 99mTcпертехнетата или 123I (при кормлении грудью исследование противопоказано). Очень часто диагноз безболевого тиреоидита устанавливается ретроспективно при динамическом наблюдении пациентов с субклиническим нарушением функции ЩЖ. Следует помнить о том, что наиболее частой причиной нарушения функции ЩЖ в послеродовом периоде является именно послеродовый тиреоидит, а не болезнь Грейвса или хронический АИТ.
Втиреотоксической фазе лечение тиреостатиками не показано, назначается симптоматическая терапия бета-адреноблокаторами. В фазе гипотиреоза назначается заместительная терапия препаратами тироксина («Эутирокс»).
Хронический фиброзный инвазивный тиреоидит (тиреоидит Риделя) –
крайне редкое заболевание ЩЖ, встречается в возрасте от 23 до 78 лет, хотя в большинстве наблюдений возраст больных 40–60 лет. Описан Риделем в 1896 г. Фиброзный тиреоидит составляет 0,05–0,06 % от всех тиреопатий, выявляемых по результатам послеоперационного морфологического исследования. Соотношение мужчин и женщин 1:2–1:4. Он проявляется вначале уплотнением (обычно
содной стороны), постепенно захватывающим большую часть доли или всю железу. При одностороннем поражении весьма затруднительна дифференциальная диагностика со злокачественной опухолью. Для него характерна необычная плотность, которую сравнивают с плотностью дерева или железа. Функция ЩЖ в начале не изменяется, на поздних стадиях развивается гипотиреоз. Некоторое улучшение может наступить даже после обычной биопсии. Тиреоидит Риделя характеризуется замещением тиреоидной паренхимы разрастающейся соединительной тканью с прорастанием в капсулу, прилежащие мышцы, сосуды и нервы.
Вначале заболевания нет никакой симптоматики, кроме ощущения «комка» и давления в области ЩЖ. В последующем, по мере разрастания соединительной ткани и сращения с соседними органами (гортань, пищевод), сосудами, нервами возникают затруднение дыхания, боль при глотании, сухой кашель, осиплость голоса (вплоть до афонии), расстройство регионарного кровообращения. ЩЖ нередко в размерах не увеличивается (даже уменьшается), безболезненная, деревянистая, с гладкой поверхностью. Вследствие выраженного спаечного процесса
сокружающими тканями ее подвижность ограничена или полностью утрачена. В отдельных случаях наблюдаются судороги в результате распространения фиброзного процесса на околощитовидные железы и развития гипопаратиреоза, что подтверждается определением дисбаланса уровней содержания кальция и фосфора в сыворотке крови. Лимфатические узлы не изменены. Температура тела в норме. Тиреоидит Риделя нередко сочетается с медиастинальным и ретроперитонеальным фиброзом (болезнь Ормонда) и артериитом Такаясу, что позволило ряду авторов не относить его к тиреоидитам.
21
При лабораторном и гормональном обследовании в фазе эутиреоза изменений не выявляется. При УЗИ отмечается снижение эхогенности паренхимы ЩЖ. Постановка диагноза должна основываться только на данных гистологическое исследование биоптата ЩЖ.
При симптомах сдавления окружающих тканей, прогрессирующей инвазии и подозрении на злокачественность выполняют тиреоидэктомию. В связи с большой опасностью повреждения окружающих анатомических образований, часто ограничиваются декомпрессионным рассечением или удалением перешейка ЩЖ. При невозможности оперативного лечения ряд авторов указывает на эффективность длительной терапии кортикостероидами. При развитии гипотиреоза назначается заместительная терапия препаратами тироксина («Эутирокс»).
АИТ – аутоагрессивное заболевание, морфологическим проявлением которого является лимфоидная и плазмоцитарная инфильтрация ЩЖ с последующим ее разрушением и замещением соединительной тканью. Обусловлен аутоиммунизацией тиреоидными антигенами. При АИТ генетическая предрасположенность окончательно не доказана. Описан Х. Хасимото в 1912 г., и все еще некоторыми авторами обозначается как тиреоидит Хасимото. Он изучил гистологически ЩЖ, удаленные у 4 больных с диффузным зобом, и выявил специфические морфологические изменения в железах с однотипным наличием 4 характерных признаков: диффузная инфильтрация железы лимфоцитами; образование лимфоидных фолликулов; деструкция эпителиальных клеток и пролиферация фиброзной (соединительной) ткани, которая замещает нормальную ткань. Диффузная инфильтрация лимфоидной ткани, постепенно вытесняя все больше и больше паренхиму, с течением времени нередко приводит к гипотиреозу. У 4-10 % больных отмечается гиперфункция ЩЖ (хаситоксикоз), которая может быть начальным клиническим вариантом заболевания. Эти симптомы нередко ошибочно трактуется в пользу ДТЗ. Поэтому одной из важных задач является оценка клинических проявлений тиреоидного статуса (табл. 7).
АИТ чаще встречается у женщин (соотношение женщин и мужчин составляет 10–15:1) в возрасте 40–50 лет, но может отмечаться и в более молодом возрасте.
Клиническими симптомами являются значительная локальная или диффузная (чаще симметричная) плотность ЩЖ, умеренные боли. Размеры ЩЖ могут быть различными. В зависимости от размеров железы выделяют: 1) гипертрофическую форму АИТ (ЩЖ плотная, диффузная, ее функция в норме или отмечаются умеренные нарушения ее функции – гипотироз или тиреотоксикоз); 2) атрофическую форму (ЩЖ ранее не была увеличенной или отмечалось умеренное ее увеличение, в момент обследования ЩЖ уменьшена, отмечается гипотироз).
Основные жалобы больных объясняются увеличением ЩЖ. При большой плотности и значительном увеличении ее размеров больные предъявляют жалобы на утолщение, чувство давления в области передней поверхности шеи, нередко небольшую болезненность в проекции ЩЖ, и лишь иногда на затруднение при глотании и дыхании. Компрессионные симптомы возникают редко.
При пальпации ЩЖ безболезненная, подвижная (не спаяна с окружающими тканями), умеренной плотности, с ровной, реже бугристой поверхностью за счет локальных уплотнений. Последний признак может обусловить ложную диагностику УЗ.
22
|
Таблица 7 |
|
Клинические проявления тиреотоксикоза и гипотиреоза |
||
Тиреотоксикоз |
Гипотиреоз |
|
Плаксивость и раздражительность. |
Апатия и сонливость. Зябкость и плохая перено- |
|
Чувство жара, плохая переносимость |
симость холода. Увеличение массы тела. Боли в |
|
жары. Нарушение сна. Снижение массы |
мышцах. Отеки лица и конечностей. Выпадение |
|
тела. Избыточная потливость. |
волос, повышение ломкости ногтей. |
|
Наличие зоба (обычно диффузное уве- |
Увеличение или уменьшение (редко) размеров |
|
личение щитовидной железы). |
ЩЖ. |
|
Моложавость (особенно в начале забо- |
Старообразный вид даже у молодых и у детей. |
|
Пастозность и маскообразность лица. Отечность |
||
левания). |
||
кистей. |
||
|
||
«Стройный» скелет, тонкие кости. |
Кости короткие и толстые. |
|
Длинные тонкие пальцы, суживающиеся |
Короткие толстые пальцы, часто утолщенные к |
|
ногтевой фаланге. Тусклые и ломкие волосы, |
||
к ногтевой фаланге. |
деформированные ногти. |
|
|
||
Небольшие атрофичные молочные |
Большие молочные железы со значительным |
|
железы. |
отложением жира. |
|
|
Кожа толстая, бледная, холодная, морщинистая, |
|
Кожа тонкая, влажная, горячая. |
сухая, иногда шелушащаяся. Симптом грязных |
|
|
локтей. |
|
Повышенный аппетит. Склонность к |
Пониженный аппетит. Запоры вследствие гипо- |
|
поносам вследствие гипермоторики |
||
моторики кишок. |
||
желудка и кишечника. |
||
|
||
Повышенная возбудимость центральной |
Заторможенность ЦНС (адинамия). Неуклюжесть |
|
нервной системы (ЦНС), психическое |
и вялость, как двигательная, так и психическая |
|
возбуждение, доходящее иногда до |
безучастность, апатичность. Замедленное мышле- |
|
маниакального состояния (нервозность, |
ние, снижение памяти, «вялая» речь. Грубый, |
|
суетливость). |
сиплый голос. |
|
Неустойчивая температура, иногда |
|
|
субфебрилитет. «Гиперактивная» воспа- |
Снижение температуры тела. Нормо- и гипореак- |
|
лительная реакция при инфекционных |
тивность даже при инфекционных заболевания. |
|
заболеваниях (после его окончания |
||
|
||
длительный субфебрилитет). |
|
|
Повышенная возбудимость вегетативной |
Пониженная возбудимость вегетативной нервной |
|
нервной системы, преимещественно |
системы. Снижение рефлексов. |
|
симпатического отдела. |
||
|
||
Дрожание конечностей (тремор кистей |
|
|
рук), иногда «вибрация» всего тела |
Дрожание конечностей обычно нет. |
|
(симптом «телеграфного столба»). |
|
|
Повышенная подвижность суставов. |
Тугоподвижность суставов. |
|
Тахикардия. Пульс слабого наполнения. |
|
|
В тяжелых случаях мерцательная тахиа- |
Брадикардия. |
|
ритмия. |
|
|
Глазные симптомы (широкие глазные |
Узкие глазные щели. Энофтальм. |
|
щели, экзофтальм и др.). |
||
|
||
Блуждающий, тревожный, иногда гнев- |
Спокойный, без всякого выражения, безучастный |
|
ный взгляд. |
взгляд. Увеличение языка. |
|
Систолическое артериальное давление |
Артериальное давление понижено. Пульсовое |
|
повышено, диастолическое понижено. |
||
давление 40 мм рт ст. или ниже. |
||
Пульсовое давление больше 50 мм рт ст. |
||
|
23 |
|
Напряженность и небольшая болезненность ЩЖ появляются при быстром увеличении ее размеров, что бывает очень редко. При гипертрофической форме АИТ железа увеличена, при атрофической – размеры ее в норме или даже уменьшены. Заболевание может протекать и без каких-либо клинических проявлений, когда ЩЖ не увеличена и мало отличается от нормальной. Такую форму заболевания с наличием эутиреоза называют субклинической. АИТ может сочетаться с другими аутоиммунными болезнями и синдромами: ДТЗ, инфильтративной офтальмопатией, миастенией, синдромом Шегрена, витилиго, алопецией, лимфоидноклеточным гипофизитом, коллагенозами.
Клиническая симптоматика АИТ обусловлена не только «местными» жалобами, но и дефицитом Т3, Т4 и возникающими вследствие этого общеметаболическими сдвигами. С последними связаны различные кардиальные, сосудистые, неврологические, желудочно-кишечные нарушения. В части случаев определяющими в клинической картине являются нарушения сердечно-сосудистой системы.
Гипотиреоз прогрессирует постепенно. Часто вначале обращают внимание лишь на субъективные жалобы: усталость, быструю утомляемость, снижение физической или умственной активности. Последующие проявления гипотиреоза многообразны, многие из них неспецифичны, с чем и связаны определенные трудности в его своевременном распознавании.
Воснове развития гипотироза лежит длительный и выраженный дефицит тиреоидных гормонов со снижением окислительных процессов и термогенеза, накоплением продуктов обмена, что ведет к функциональным нарушениям ЦНС, эндокринной, сердечно-сосудистой, пищеварительной и других систем, а также к своеобразному слизистому отеку различных тканей и органов, включая слизистый выпот в полости плевры и перикарда.
Вбольшинстве случаев внешний вид и жалобы больных АИТ с выраженным гипотиреозом достаточно характерны. Внешне это медлительные, заторможенные, сонливые и апатичные люди с низким хриплым голосом, избыточной массой тела, одутловатым лицом и отечными «подушечками» вокруг глаз (периорбитальный отек), припухшими веками, большими губами и языком, отечными конечностями, сухой, утолщенной, желтого цвета кожей с гиперкератозом в области локтевых и коленных суставов. Волосы тусклые, сухие и ломкие, медленно растут. Отмечается выпадение волос (обычно на голове, бровях, конечностях) и разрушение зубов. Ногти тонкие, с продольной или поперечной исчерченностью. Нарушения со стороны ЦНС проявляются усталостью, сонливостью, замедлением речи, некритичностью к себе и окружающим. В некоторых случаях превалируют жалобы на головные боли, снижение памяти, отсутствие интереса к работе. Клиника выраженной гипотиреоидной миопатии проявляется гипертрофией и псевдомиотонией мышц, отсутствием ахиллового рефлекса, болями в мышцах. Суставной синдром может предшествовать другим симптомам гипотиреоза или развиваться одновременно с ним. Изменения в сердечно-сосудистой системе начинают проявляться достаточно рано. Появляются ноющие и колющие боли в области сердца, одышка при физическом напряжении, у ряда больных отмечается брадикардия. Перестройка фазовой структуры сердечного цикла происходит по типу гиподинамии миокарда. Отклонение электрической оси сердца влево связано со структурными изменениями миокарда (преимущественно левого желудочка) и позиционными сдвигами (ожирение, высокое стояние диафрагмы). Гипоксические изменения, выявляемые на ЭКГ, обратимы после адекватной заместительной терапии тироксином. Физикальное исследование подтверждает наличие
24
брадикардии, выявляет мягкий пульс, увеличение размеров сердца и глухость его тонов, снижение систолического и нормальное или незначительно повышенное диастолическое давление. У 15 – 20 % больных выявляется артериальная гипертензия.
Одними из характерных проявлений гипотиреоза при АИТ являются функциональные и морфологические изменения желудочно-кишечного тракта, вследствие которых возможны тошнота и рвота, запоры, снижение аппетита. При нарушении метаболизма витаминов развивается пернициозная анемия. При тяжелом течении АИТ с выраженным гипотиреозом реально развитие жировой дистрофии печени. Довольно часто отмечается дискинезия желчных путей по гипотоническому типу.
При наличии гипотиреоза содержание Т4 в сыворотке крови снижено, а ТТГ повышено. Отмечаются повышенные титры АТ-ТГ, АТ-ТПО, гиперлипопротеидемия, нормоцитарная (чаще) или макроцитарная анемия. При оценке электрокардиограммы констатируют синусовую брадикардию, снижение амплитуды зубцов, пологий зубец Т.
Влечении АИТ предпочтение сегодня отдаётся консервативной терапии. Обращает внимание частота гипердиагностики узловых образований при АИТ, что приводит к выполнению необоснованных операций на ЩЖ. Показанием к хирургическому лечению являются: большой размер зоба с наличием компрессионного синдрома, сочетание с неопластическими процессами в ЩЖ, неэффективность консервативной терапии тиреоидными гормонами и лазеротерапии. Следует отметить, что сочетание рака ЩЖ и АИТ встречается в 4–6 % наблюдений. У пациентов с хаситоксикозом необходимость в хирургическом лечении может возникнуть при непереносимости тиреостатических препаратов, развитии гранулоцитоза, упорном рецидивирующем течении тиреотоксикоза. Операцией выбора является субтотальная резекция ЩЖ. При подтверждении рака – тиреоидэктомия. Применение радиойодтерапии у пациентов с хаситоксикозом считается нецелесообразным.
Влечении большинства заболеваний ЩЖ большое значение имеет индивидуализация лечебной тактики и рациональный выбор способа коррекции, необходимость которой должна быть веско аргументирована. Увеличение числа оперативных вмешательств на ЩЖ обусловлено ростом выявляемости узловых форм тиреоидной патологии и улучшением ранней диагностики в связи с широким внедрением высокоинформативных диагностических технологий. Вместе с тем, в последние десятилетия отмечается как неоправданное увеличение хирургической активности в отношении некоторых заболеваний ЩЖ, так и расширение показаний к консервативному лечению. Поэтому вопросы, касающиеся определения показаний к оперативному лечению и выбора его адекватного объёма, остаются дискутабельными, а с учётом внедрения новейших наукоёмких технологий (миниинвазивных методов, эндовидеохирургической и лазерной техники), возрастающего значения социально-экономических факторов и коммерциализации медицины, становятся особо актуальными.
Литература
1.Браверман Л. И. (ред.) Болезни щитовидной железы (пер. с англ.). – М. : Медицина, 2000. – 432 с.
2.Брейдо И. С. Хирургическое лечение заболеваний щитовидной железы. - 2-е изд., переработ. и доп. – СПб. : Гиппократ, 1998. – 336 с.
3.Валдина Е. А. Заболевания щитовидной железы. – СПб.: Питер, 2001. – 416 с.
4.Потемкин В. В. Эндокринология. – М. : Медицина, 1999. – 640 с.
25
ЛЕКЦИЯ 2
ЗАБОЛЕВАНИЯ МОЛОЧНОЙ ЖЕЛЕЗЫ
А. В. Щербатых
Анатомия и физиология
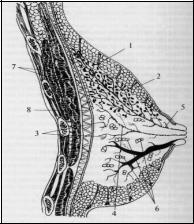
Молочные железы – парный орган, имеющий трубчатоальвеолярное строение и располагающийся на передней поверхности грудной клетки. Состоит из паренхимы – железистой ткани с проходящими в ней протоками различного калибра; стромы – соединительной ткани, разделяющей железы на доли и дольки; жировой ткани, в которою погружены паренхима и строма железы (рис. 1)
Рис. 1. 1 – место прикрепления связки Купера (гребень Дюретта), 2 – подкожная жировая клетчатка, 3 – терминальная часть млечного протока, 4-междольковый млечный проток, 5 – главный млечный проток, 6 – срединный жировой пласт, 7 – большая и малая грудные мышцы, 8 – ретромаммарная жировая клетчатка (сумка Шассиньяка)
Между глубоким листком фасции, покрывающим заднюю поверхность молочной железы, и апоневрозом большой грудной мышцы находится ретромаммарное пространство, выполненное рыхлой клетчаткой, что обусловливает подвижность молочной железы. В зависимости от периода жизни женщины и гормональных изменений в организме молочные железы проходят ряд последовательных стадий развития. Зачаток молочной железы формируется у плода еще в антенатальном периоде (на 10-й нед. внутриутробной жизни). В периоде новорожденности в первые 3-5 дней жизни происходит незначительное увеличение молочных желез за счет гормональной стимуляции циркулирующими в крови материнскими плацентарными гормонами. Иногда отмечается секреция молочной железы. В детском возрасте молочные железы у девочки невыраженные – сосок маленький, непигментированный, незначительно возвышается над ареолой. У 9-10- летней девочки сосок имеет форму цветочного бутона, ареола несколько возвышается, появляется незначительная пигментация соска и ареолы. Среди пучков коллагеновых волокон с жировыми включениями располагаются немногочисленные трубочки (железистые образования) различного диаметра. Молочная железа пребывает в состоянии функционального по-
26
коя. В молочных железах у женщин в репродуктивном периоде процессы пролиферации и обратного развития периодически сменяют друг друга. Смена указанных процессов обусловлена цикличностью синтеза половых стероидных гормонов, которые продуцируются яичниками и надпочечниками, а также гонадотропинов (фолликулостимулирующего (ФСГ) и лютеинизирующего (ЛГ)), вырабатываемых передней долей гипофиза. Функция этой сложной системы регулируется гипоталамическими структурами и корой головного мозга. Экспериментальные исследования показали, что как эстрогены в сочетании с гонадотропинами, так и прогестерон вызывают в молочных железах выраженную гиперплазию клеточных элементов. Однако характер гиперплазии, обусловленный действием различных половых гормонов, неодинаков. Гиперплазия, возникшая под влиянием эстрогенов и ФСГ, характеризуется присоединяющимися секреторными процессами, тогда как при гиперплазии, вызванной воздействием прогестерона, отмечается только пролиферация. Эти различия связаны с тем, что эстрогены и ФСГ обладают ЛТГ стимулирующим действием. А ЛТГ, как известно, вызывает секрецию. Прогестерон лишен названного свойства. Именно этим можно объяснить то обстоятельство, что в лютеиновую фазу, когда отмечается относительно высокий уровень прогестерона, молочные железы несколько увеличиваются в размерах, в них наблюдается признак так называемого предменструального нагрубания. В канун месячных прогестерон и эстрогены, вырабатываемые желтым телом, приводят к резкому торможению продукции ФСГ и ЛГ. В результате наступает гибель желтого тела, прекращается продукция прогестерона и эстрогенов. Вследствие этого происходит отторжение определенных слоев эндометрия, что проявляется в виде менструаций. С окончанием последней начинается новый цикл изменений в системе гормонального гомеостаза. Значительные сдвиги претерпевает эндокринная, в частности репродуктивная, система при наступлении менопаузы. В молочных железах постепенно наступают инволютивные изменения.
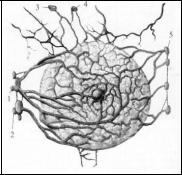
Кровоснабжение осуществляют ветви латеральной грудной артерии (a. thoracica lateralis) и ветви второй и третьей межреберных артерий (a. intercostalis). Венозная сети состоит из поверхностей и глубокой сети. Глубокие вены сопровождают артерии и впадают в подмышечную, внутреннюю грудную, латеральную грудную и межреберные вены. частично в наружную яремную вену. Из поверхностных вен кровь оттекает в кожные вены шеи, плеча, боковой стенки груди и вены эпигастральной области. Поверхностные и глубокие вены образуют сплетения в толще железы, коже, подкожной клетчатке и широко анастомиозируют между собой, с венами соседних областей и противоположной молочной железы Основные пути лимфооттока от молочной железы: 1 – подмышечный; 2 – парастернальный; 3 – подключичный; 4 –надключичный (рис. 2).
27

Лимфоотток от наружных квадрантов молочных желез происходит главным образом в подмышечные лимфатические ходу v. thoracica interna. в парастернальные и интерпекторальные лимфатические узлы. Часть лимфы оттекает между большой и малой грудными мышцами и вливается в глубокие подмышечные и подключичные лимфатические узлы.
Дисгормональные заболевания молочной железы
Термином "мастопатия" обозначают группу диспластических доброкачественных заболеваний молочной железы с гиперплазией ее ткани. По определению ВОЗ (1984) мастопатия – фиброзно-кистозная патология с широким спектром пролиферативных изменений в тканях молочной железы и патологическим соотношением эпителия и соединительнотканных компонентов. Фактически, можно говорить скорее о группе заболеваний — дисгормональных дисплазий молочной железы — имеющих сложную клиническую и гистологическую картину и объединенных общим термином “мастопатия”. Для клинической практики удобна классификация на диффузные и узловые формы изменений в железах.
1.Диффузная фиброзно-кистозная мастопатия:
с преобладанием железистого компонента (аденоз);
с преобладанием кистозного компонента;
с преобладанием фиброзного компонента;
смешанная форма.
2.Узловая фиброзно-кистозная мастопатия.
Детально мастопатия была изучена Reclu (1883-1887). В нашей стране одними из первых стали изучать это заболевание Н. А. Вельяминов (1904) и М. М. Дитерихс (1904). В дальнейшем мастопатии было посвящено большое количество работ зарубежных и отечественных авторов.
Этиология и патогенез
Мастопатия объединяет большую группу различных по морфологическому строению, но общих по этиологии и патогенезу заболеваний молочной железы, являющихся по своему существу дисгормональными пролифератами. Впервые мастопатию описали Cooper (1828) и Aschoff (1832) (цит. по И. Я. Слониму). Большинство исследователей придерживаются мнения о том, что для возникновения фиброаденоматоза необходимы два основных условия: эстрогенная стимуляция молочной железы за счет абсолютного или относительного повышения эстрогенов у молодых женщин (до 40 лет) или наличие прогестероновой недостаточности, наблюдающейся обычно в пременопаузе (после 40 лет). В некоторых исследованиях указано на возможность снижения уровня классических эстрогенов у больных мастопатией (Сидоренко Л. Н., 1986) и соотношение эстрогены/прогестерон, разнообразного спектра регуляторных нарушений в звеньях ги- пофиз-надпочечники, гипофиз-яичники, гипоталамус-гипофиз, ЦНС-гипоталамус- гипофиз, гипофиз-щитовидная железа, нарушение функции печени, т. е. на изменения не только в репродуктивном, но и в адаптационном и энергетическом гомеостазах с самыми разнообразными отклонениями от нормы. Таким образом, многочисленные биохимические исследования секреции и экскреции стероидных гормонов яичников, а также всех известных гормонов, ответственных за формирование и функцию молочной железы (гормоны надпочечников, гипофиза, в том числе ФСГ, ЛГ, СТГ, пролактин, рилизинг-гормоны и т. д.), не показали единых и
28
четко воспроизводимых в различных лабораториях гормональных отклонений у больных мастопатией. Все это дало основание ряду крупных исследователей придти к заключению, что этиология мастопатии до настоящего времени остается невыясненной. Тем не менее необходимо дать какие-то определенные ориентиры для этой группы заболеваний с целью лучшего понимания их сущности, выбора лечения. Главным, естественно, могут служить данные микроскопического исследования. Многообразие форм диспластических процессов и доброкачественных опухолей молочной железы, имеющих разный гисто и морфогенез, свидетельствует о том, что здесь не может быть какой-то единой причины их возникновения. Многочисленные нарушения в репродуктивном, адаптационном и энергетическом гомеостазах приводят к огромному разнообразию дисгормональных гиперплазии и доброкачественных опухолей молочных желез эпителиального, мезенхимального и смешанного происхождений. Вторым ориентиром может служить возраст, в котором встречается различная «доброкачественная» патология молочной железы. Так, у девушек при наступлении полового созревания и включении циклической функции яичников чаще других опухолей встречаются незрелые фиброаденомы, аденомы и аденофибромы. В следующем возрастном периоде (репродуктивный пик), наряду с воспалительными процессами, связанными с особенностями лактации (мастит, галактофорит, галактоцеле) все чаще отмечается появление диффузного двустороннего фиброаденоматоза или аденоза с циклическим менструальным болевым синдромом, набуханием молочных желез, обозначаемых иногда мастодинией. В этой же возрастной группе (25–39 лет) нередки и другие пролиферативные процессы, такие, как интрадуктальная папиллома. По мере приближения к менопаузе (40-49 лет) более характерны возникновение локализованных форм фиброаденоматоза, развитие цистаденопапиллом (рис. 3), интрадуктального папилломатоза, склерозирующего аденоза.
С наступлением менопаузы и особенно в глубокой менопаузе частота пролиферативных процессов и различных форм мастопатии резко сокращается, а большинство из них вообще исчезают. На первое место перемещаются непролиферативные процессы типа дуктэктазии, стеатогранулем, галактофоритов, не связанных с предшествующим маститом. В этом же периоде резко возрастает заболеваемость раком молочной железы. На смену разнообразным формам мастопатии, встречающейся почти у 50 % женщин старше 30 лет, приходит более
грозное заболевание — рак молочной железы (0,1 %). Сама возрастная эволюция доброкачественных заболеваний молочной железы несомненно отражает характер возрастных гормональных изменений от высокого уровня эстрогенов в юном и молодом возрасте (до 25–30 лет) и возникающих на этом фоне фиброаденом до заметного снижения секреции эстрогенов и прогестерона в пременопаузе — излюбленном возрасте появления фиброаденоматоза и цистаденопапиллом. Значение имеет наследственный фактор, в первую очередь — это наличие доб-
Рис. 3. Пневмокистограмма. |
рокачественных и злокачественных заболеваний |
|
Цистоаденопапилллома |
||
у родственниц по материнской линии. Искус- |
||
|
||
|
29 |
ственное прерывание беременности значительно повышает риск развития патологии молочных желез. У женщин, которым произведено 3 искусственных аборта и более, риск развития мастопатий в 7,2 раза выше. Аборт прерывает пролиферативные процессы в молочных железах и ткань подвергается обратному развитию. Эти регрессивные изменения происходят неравномерно, поэтому развитие желез может приобрести патологический характер. Вместе с тем, рассматривая весь спектр «возрастной» патологии молочной железы, нет никаких оснований полагать, что эти заболевания «вытекают» одно из другого. Возрастное отличие характера доброкачественной патологии молочной железы свидетельствует лишь о том, что гормоны имеют существенное значение в механизме их формирования, развития, роста и иногда регрессии.
Хирургическое, гормональное и другие методы лечения мастопатии, проводимые в различных странах в течение многих лет, не привели ни к сокращению, ни к стабилизации показателей заболеваемости раком молочной железы. Одно это вызывает сомнение в утверждении многочисленных авторов в безусловной предраковой природе мастопатии, различные формы которой, по их мнению, отдельные ступени на пути к раку.
Мастодиния
Под этим термином подразумеваются более или менее выраженные болевые ощущения в молочных железах у женщин обычно в детородном возрасте — от 20 до 40 лет. При этом женщины жалуются на боли в одной или обеих молочных железах постоянного характера, особенно усиливающиеся в предменструальный период. Болезненные ощущения нередко достигают очень высокой интенсивности, могут иметь жгучий характер. Боли отдают в соответствующую подмышечную ямку или плечо. В большинстве случаев мастодиния отмечается у женщин не рожавших или мало рожавших. Молочные железы у них умеренно развиты, менструации большей частью нормальные, а у некоторых нерегулярные. При осмотре у женщин, страдающих мастодинией, со стороны молочных желез отмечаются набухание и отек за 10–12 дней до наступления менструаций. Иногда отмечается умеренно выраженное диффузное уплотнение молочной железы. При клиническом исследовании больных мастодонией нередко наблюдаются гипофункция яичников, хронический аднексит. Мастодиния может наблюдаться у больных туберкулезом легких, хроническим холециститом, которые, по видимому, оказывают инфекционно-токсическое воздействие на молочные железы. При лечении мастодинии в тех случаях, когда она обусловлена главным образом нейрогормональными нарушениями, в зависимости от дисфункции яичников, устанавливаемой с помощью вагинальных мазков, назначается гормонотерапия. У более молодых женщин хороший эффект достигается с помощью прегнина или прогестерона, а у женщин в более зрелом возрасте (свыше 35 лет) хорошие результаты дает тестостерон. При мастодинии инфекционно-токсического происхождения необходимо устранение очагов воспалительного процесса в организме больной. В пожилом возрасте, особенно в период менопаузы, болевые ощущения в молочных железах в большинстве случаев обусловлены развитием узловатофиброзной мастопатии в начальных периодах ее возникновения. Известное значение для возникновения болевого симптома имеют также гормональные нарушения, возникающие в этом возрасте и обусловливающие обратную инволюцию молочной железы в виде атрофии ее и развития фиброзной ткани. Иногда этот
30
