
biopolimery (1)
.pdfФедеральное агентство по здравоохранению и социальному развитию РФ Иркутский государственный медицинский университет Кафедра бионеорганической и биоорганической химии
Колесниченко Л.С., Губина Л.П., Ошуркова Н.В.
БИОПОЛИМЕРЫ И ИХ СТРУКТУРНЫЕ КОМПОНЕНТЫ
ИРКУТСК 2011
Федеральное агентство по здравоохранению и социальному развитию РФ Иркутский государственный медицинский университет Кафедра бионеорганической и биоорганической химии
Колесниченко Л.С., Губина Л.П., Ошуркова Н.В.
БИОПОЛИМЕРЫ И ИХ СТРУКТУРНЫЕ КОМПОНЕНТЫ
Рекомендовано УМО по медицинскому и фармацевтическому образованию вузов России в качестве учебного пособия для
студентов медицинских вузов
Иркутск 2011
2
Рецензенты:
Зав. кафедрой химии Сибирского медицинского университета, г.Томск д.х.н. проф. Юсубов М.С.
Зав. кафедрой биохимии и биоорганической химии Читинской медицинской академии д.м.н. проф. Хышиктуев Б.С.
Учебное пособие «Биополимеры и их структурные компоненты» дополняет существующие учебники по биоорганической химии. Оно предназначено для
студентов первого курса всех факультетов медицинских ВУЗов.
Пособие будет полезно для студентов второго и третьего курсов
при изучении биохимии и фармакологии.
3
|
ОГЛАВЛЕНИЕ |
|
|
|
стр. |
|
УГЛЕВОДЫ |
5-24 |
|
Моносахариды |
6-15 |
|
Олигосахариды |
15-18 |
|
Полисахариды |
18-24 |
|
ЛИПИДЫ |
25-42 |
|
Неомыляемые липиды |
27-33 |
|
Омыляемые липиды |
34-42 |
|
АМИНОКИСЛОТЫ, ПЕПТИДЫ И БЕЛКИ |
43-68 |
|
ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ |
69-78 |
НУКЛЕОЗИДЫ. НУКЛЕОТИДЫ. |
|
|
|
НУКЛЕИНОВЫЕ КИСЛОТЫ |
79-88 |
|
ЛИТЕРАТУРА |
89 |
4
УГЛЕВОДЫ
УГЛЕВОДЫ – это оксопроизводные (альдегиды или кетоны)
многоатомных спиртов и продукты их конденсации.
Углеводы входят в состав растительных и животных организмов.
Роль углеводов велика:
1. это источник энергии (в растениях – крахмал, в животных организмах – гликоген); 2. являются структурными компонентами клеточных стенок (целлюлоза),
бактерий (мурамин), грибов (хитин); 3. входят в состав жизненно важных веществ, а именно: нуклеиновых кислот,
коферментов;
4.для синтеза других органических соединений (жиров и заменимых аминокислот);
5.некоторые углеводы являются лекарствами;
6.специфические функции.
|
|
|
|
|
|
|
|
|
|
|
КЛАССИФИКАЦИЯ УГЛЕВОДОВ |
||
Моносахариды: |
лигосахариды |
олисахариды: содержат |
|||||||||||
а) по оксогруппе |
содержат от 2 до |
более 10 остатков |
|||||||||||
|
|
альдозы |
|
|
|
|
кетозы |
10 остатков |
моносахаридов. |
||||
|
|
|
|
|
O |
|
|
|
H2O |
моносахаридов |
1) гомополисахариды |
||
|
|
|
|
|
|
|
|||||||
|
|
C |
H |
|
|
|
C=O |
|
(содержат одинаковые |
||||
|
|
|
|
|
|
||||||||
(H |
|
C |
|
OH)n (H |
|
C |
|
OH)n-1 |
|
||||
|
|
|
|
|
остатки): крахмал, |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
CH2OH |
|
|
|||||||||
|
|
|
|
CH2OH |
|
||||||||
б) по числу атомов углерода: |
|
гликоген, клетчатка, |
|||||||||||
С3 – триозы |
|
|
|
|
|
|
|
декстраны, инулин. |
|||||
С4 – тетрозы |
|
|
|
|
|
|
|
2) гетерополисахариды |
|||||
С5 – пентозы |
|
|
|
|
|
|
|
(состоят из различных |
|||||
С6 - гексозы |
|
|
|
|
|
|
|
остатков). Различают: |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
протеогликаны, |
|
|
|
|
|
|
|
|
|
|
|
|
|
гликопротеиды. |
5

МОНОСАХАРИДЫ (МС) – наиболее принятой номенклатурой является тривиальная с окончанием «оза». Например, глюкоза, фруктоза и т.д.
Исключение составляют триозы (глицериновый альдегид и дигидроксиацетон).
|
|
O |
|
CH2OH |
|
C |
H |
|
|||
|
|
C=O |
|||
C |
|
OH |
|||
|
|||||
|
|
|
|
||
|
CH OH |
CH2OH |
|||
Стереоизомерия – все МС (исключение составляет только дигидроксиацетон)
имеют хиральный центр или асимметрический «С» - это такой атом, у которого все связи заняты различными заместителями. У глицеринового альдегида имеется один хиральный центр, а количество стереоизомеров определяется по формуле 2n, где n число хиральных центров, значит у глицеринового альдегида
2 стереоизомера (21).
|
|
CHO |
|
|
O |
|
|||
D(+)-глицериновый |
H |
|
* |
OH |
HO |
|
* |
H |
L(-)-глицериновый |
|
|
||||||||
|
|
|
|
||||||
|
|
|
|
|
|
|
|
||
альдегид |
|
|
CH2OH |
|
|
CH2OH |
альдегид |
||
|
|
|
|
|
|
|
|
||
Принадлежность к D- или L-стереохимическому ряду определяется путем
сравнения конфигурации последнего асимметрического «С» атома с конфигурацией асимметрического «С» атома D- или L-глицеринового альдегида.
CHO |
HO * H |
* OH |
|
CH2OH |
CH2O |
D(+)-глицериновый альдегид |
L(-)-глицериновый альдегид |
Почти все природные МС, важные для человека, принадлежат к D-ряду.
Наиболее распространены пентозы и гексозы.
Для изображения стереоизомеров МС используются проекционные формулы Фишера, но наибольшее распространение в природе и в организме имеют циклические формы Хеуорса.
6

Примеры альдопентоз:
пол ацет н гидроксил
5
CH2OH β-аномер
H |
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|||
|
|
C |
|
|
H |
|
|
OH |
|
4 |
|
3 |
|
|
1 |
|
|
||||||||
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
C |
|
|
|
|
|
|
|
|
|
2 |
|
|
|
||||||
H |
|
|
* |
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
OH |
|
свободный |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
H |
|
|
* |
|
OH |
|
|
H |
|
|
|
OH |
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
* |
|
|
|
|
H |
|
|
|
|
OH O |
β-D-рибофураноза полуацетальный |
|||||||||||
H |
|
|
|
OH |
|
|
H |
|
|
|
|
|
|
|
5 |
|
|
|
|
|
|
|
гидроксил |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2OH |
|
|
|
|
||||||
|
|
CH2OH |
|
|
|
|
|
|
|
O |
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
CH2OH |
|
|
4 |
|
3 |
1 |
|||||||||||||
|
D-рибоза |
|
|
|
|
|
|
|
2 |
||||||||||||||||
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH α-аномер |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
α-D-рибофураноза |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
переход линейной формы в циклическую |
|
|
|
|||||||||||||||||
H |
|
|
|
|
O |
|
H |
|
|
|
OH |
|
|
|
|
|
|
|
У альдопентоз |
|||||||||||||
|
|
|
C |
|
|
|
|
C |
|
|
|
|
|
|
|
|
|
|
|
имеется 3 |
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
H |
|
|
|
* OH |
|
H |
|
|
|
|
|
OH |
|
|
CH2OH |
|
O |
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
HО |
|
|
|
|
* |
|
H |
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
хиральных |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
HО |
|
|
|
|
|
|
H |
|
|
|
|
OH |
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
H |
|
|
|
* |
|
|
OH |
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
центра (2 |
3 |
) - 8 |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
||||
|
|
|
CH2OH |
|
|
|
|
CH2OH |
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
β-D-ксилофураноза |
стереоизомеров |
||||||||||||||||||||||||
|
|
|
D-ксилоза |
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
Примеры кетопентоз: |
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
H2 |
|
|
|
|
CH2OH |
|
кетопентоз имеется 2 хиральных |
|||||||||||||||||||
|
|
|
|
|
C=O |
|
|
|
|
|
|
C=O |
центра (22) – 4 стереоизомера. |
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
* |
OH |
|
HO |
|
|
|
* |
H |
У альдогексоз имеется 4 хиральных |
||||||||||||||||||
|
|
|
|
|
* |
|
|
|
* |
|||||||||||||||||||||||
|
|
|
|
|
OH |
|
H |
|
|
|
|
OH |
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
центра (24) – 16 стереоизомеров. |
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
CH2OH |
|
|
|
|
CH2OH |
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
D-рибулоза |
|
D-ксилулоза |
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
Стереоизомеры бывают конформационного и конфигурационного типов.
Последние делятся на: а) энантиомеры и б) диастереомеры.
Энантиомеры – это пространственные стереоизомеры, молекулы которых относятся друг к другу, как предмет к своему зеркальному изображению и имеющие, как правило, одинаковые физические и химические свойства.
Диастереомеры – это стереоизомеры, не являющиеся зеркальным отображением один другого и имеющие различные физические и химические
7
свойства. Примером их являются:
|
|
CHO |
|
|
CHO |
|
CHO |
|||||||
O |
|
|
|
|
H |
H |
|
|
OH |
H |
|
|
OH |
|
|
|
|
|
|
|
|
||||||||
O |
|
|
|
|
H |
HO |
|
|
|
H |
HO |
|
|
H |
|
|
|
|
|
|
|
|
|||||||
H |
|
|
|
|
OH |
H |
|
|
OH |
HO |
|
|
H |
|
|
|
|
|
|
|
|
||||||||
H |
|
|
|
|
OH |
H |
|
|
OH |
H |
|
|
OH |
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2OH |
||||||||||
|
CH2OH |
|
|
CH2OH |
|
|
||||||||
D-манноза |
D-глюкоза |
|
D-галактоз |
|||||||||||
Эпимеры – это диастереомеры, различающиеся конфигурацией только одного углеродного атома. Глюкоза и галактоза эпимеры по С4, а глюкоза и манноза -
эпимеры по С2.
Энантиомеры вращают плоскость поляризации света, т.е. обладают оптической активностью. Правовращающий обозначают знаком (+), а левовращающий (-).
Величину и знак угла вращения нельзя предсказать, они определяются с помощью приборов – поляриметров.
CH2OH |
2OH |
|
|
O |
|
|
OH |
O |
|
|
O |
OH |
H |
|
|
|
|
|
|
|||
|
|
|
|
|
OH |
|
|||
|
C1 |
|
OH |
|
C |
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
OH |
|
H |
|
OH |
|
|
|
|
2 |
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
||
H |
* OH |
|
|
OH |
|
|
|
OH |
|
|
3 |
|
|
|
|
|
β-D-глюкопираноза |
||
O |
* H |
|
|
|
|
|
|
|
|
|
4 |
|
|
|
|
|
|
|
|
H |
* OH |
|
|
|
CH2OH |
|
|
|
CH2OH |
|
5 |
|
|
|
|
OH |
|
|
|
H |
* OH |
CH2OH |
|
|
|
H |
|
O |
|
O |
|
OH |
|
|
|||||
|
6 CH2OH |
CHOH |
|
|
C |
|
OH |
||
|
|
OH |
|
H, OH |
OH |
|
O |
OH |
O |
|
|
|
|
|
|||||
D-глюкоза |
|
|
|
|
OH |
|
|
OH |
|
|
OH |
|
|
|
|
α-D-глюкопираноза |
|||
|
|
|
|
|
|
|
|||
D-глюкофураноза
У фруктозы кетогруппа С2 взаимодействует с ОН группой С5 с
образованием пятичленного фуранозного цикла (кольцо фурана):
8

CH2OH |
6CH2OH |
|
1 |
CH2OH |
O |
1 |
|
OH |
OH 2 |
CH2OH |
5 |
CH2OH |
|||
C |
O |
5 4 |
C=O |
4 |
3 OH |
2 |
|
|
3 |
|
|
|
OH |
||
O |
H |
|
|
|
|
|
|
OH |
|
|
OH |
|
|
||
H |
OH |
|
|
α-D-фруктофураноза |
|||
|
|
|
|||||
H |
OH |
|
O |
OH |
|
|
|
CH2OH |
6 |
|
|
|
|||
|
2 |
|
|
|
|||
5 |
OH |
|
|
|
|||
|
|
4 |
|
|
|
|
|
D-фруктоза |
3 |
CH2OH |
|
|
|
||
OH |
|
|
|
|
|||
|
|
OH |
|
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
β-D-фруктопираноза |
|
|
|
||
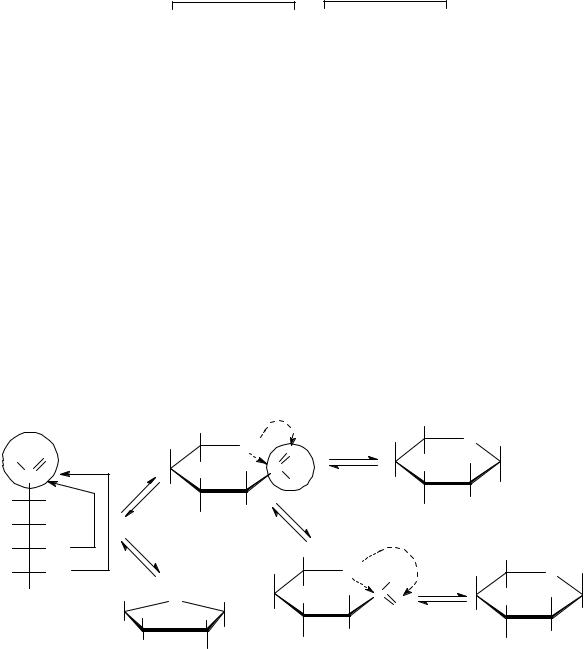
В циклических формах МС возникает еще 2 диастереомера: - и -
аномеры. Если ОН группа С1 находится под плоскостью цикла, то это -
аномер, если над плоскостью - -аномер.
Физико-химические свойства МС МС – это бесцветные, гигроскопичные, твердые кристаллические
вещества. Хорошо растворимы в воде, но нерастворимы в неполярных органических растворителях. Растворы нейтральны на лакмус. Как правило МС сладкого вкуса (исключение -аномер D-маннозы). Обладают оптической активностью.
В кристаллическом состоянии пентозы и гексозы имеют циклическое строение. При их растворении небольшая часть циклов ( 1%) раскрывается в цепь. Происходит взаимопревращение - и -аномеров. Меняется оптическая активность, т.к. - и -аномеры отличаются по физико-химическим свойствам
(как любые диастереомеры). Например,
Глюкоза |
oC плавления |
[ ]Д |
% в водном растворе |
|
|
|
|
-аномер |
46 oC |
112 |
36% |
|
|
|
|
-аномер |
48 150 oC |
8.7 |
64% |
|
|
|
|
Изменение оптической активности свежеприготовленных растворов сахаров называют мутаротацией. Химической основой мутаротации является способность МС существовать в открытой и циклической формах. Этот вид таутомерии называется кольчато-цепной или цикло-оксо-таутомерией.
9
