
- •Тема 1. Кинематика материальной точки.
- •Тема 2.
- •Тема 3. Работа и энергия. Динамика твердого тела
- •Тема 4. Основы релятивистской механики
- •Тема 5. Основы молекулярной физики
- •5.7.3. Диффузия
- •Тема 6. Физические основы термодинамики
- •6.1. Основные понятия и определения
- •6.3. Уравнение состояния идеального газа
- •6.4. Первый закон термодинамики
- •6.5. Рабочая диаграмма Pv. Работа — функция процесса
- •6.7. Зависимость теплоемкости от условий подвода теплоты. Уравнение Майера для идеального газа
- •6.7.1. Изохорная теплоемкость
- •6.7.2. Изобарная теплоемкость
- •6.7.3. Уравнение Майера для идеального газа
- •6.8. Расчет изменения внутренней энергии
- •6.9. Формулы и таблицы для истинных и средних теплоемкостей. Определение количества теплоты по теплоемкости и разности температур
- •6.10Молекулярно-кинетическая теория теплоемкости
- •6.11. Обратимые и необратимые термодинамические процессы
- •6.12. Второй закон термодинамики
- •6.13.Энтропия
- •6.14. Некоторые свойства энтропии
- •6.15. Теория «тепловой смерти Вселенной»
- •6.16.Тепловая диаграмма Ts. Теплота —функция процесса
- •6.17. Изменение энтропии идеального газа
6.14. Некоторые свойства энтропии
Энтропию нельзя измерить, ее смысл практически невозможно продемонстрировать. Но, несмотря на многоликость энтропии, ее можно понять по следующим интерпретациям. Вначале для иллюстрации сказанного используем уже известные определения энтропии, как функции состояния.
1.Энтропия
— индикатор направленности процессов
термического
взаимодействия системы со средой: ds
> 0
при
![]() q
> 0,
ds
< 0 при
q
> 0,
ds
< 0 при
![]() q
< 0,
ds
=
0 при
q
< 0,
ds
=
0 при
![]() = 0.
= 0.
Энтропия — индикатор направленности необратимых процессов в теплоизолированной системе ds > 0 при
 =
0.
=
0.Энтропия— мера необратимости реальных процессов, мера потери работоспособности системы (потери работы вследствие необратимости), мера обесценивания энергии для потребителя, ее деградации, то есть мера рассеивания энергии. Эта характеристика следует из принципа возрастания энтропии — ds > 0. Чем более необратим процесс в изолированной системе, тем больше возрастает энтропия и тем большая часть энергии
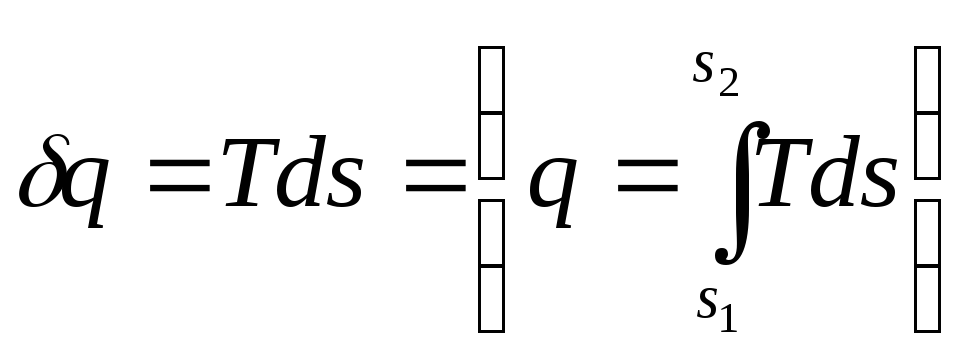 ,не
переходя в работу, рассеивается
в окружающей среде. Следовательно,
энтропия позволяет
оценить
энергетические возможности
термодинамических систем.
,не
переходя в работу, рассеивается
в окружающей среде. Следовательно,
энтропия позволяет
оценить
энергетические возможности
термодинамических систем.
Энтропия — мера трудности возврата системы в первоначальное состояние с начальной энтропией. Под «трудностью возврата» понимают количество энергии, необходимое для этого.
Энтропия — мера вероятности данного состояния системы. В теплоизолированной системе при протекании необратимых процессов состояния меняются так, что термодинамическая вероятность и энтропия возрастают. При обратимых процессах в теплоизолированной системе любое из состояний равновероятно и энтропия системы неизменна.
Энтропия — мера ценности теплоты, ее работоспособности и технологической эффективности. Опыт свидетельствует о том, что чем выше температура теплоносителя при том же количестве теплоты, то есть чем меньше энтропия (s = q/T), тем теплота ценнее, поскольку может быть использована не только для технологических нужд — выплавки металла, выпечки хлеба, отопления, но и для получения работы, например, в силовой установке летательного аппарата.
Таким образом, два энергетически эквивалентных количества теплоты q1 — q2 совсем не эквивалентны по содержащейся в них энтропии: то количество теплоты, которое связано с большей температурой, несет в себе меньше энтропии, чем то, которое связано с меньшей температурой.
7.
Энтропия — мера беспорядка (порядка) в
системе. Это так
называемая структурная энтропия. Она
является мерой неупорядоченности
строения систем. До сих пор приходилось
иметь дело с тепловой энтропией. При
подводе теплоты к системе
энтропия ее возрастает, так как
увеличивается хаотичность
теплового движения микрочастиц, порядок
в системе при этом
уменьшается. Наоборот, охлаждение
системы при постоянном
объеме есть отвод теплоты от системы,
а следовательно, и
энтропии; упорядоченность системы при
этом за счет уменьшения
кинетической энергии и хаотичности
движения микрочастиц
возрастает, а энтропия уменьшается. При
конденсации газа
упорядоченность в расположении молекул
скачком увеличивается,
что соответствует ступенчатому уменьшению
энт- ропии.
При дальнейшем уменьшении температуры
уменьшаются
интенсивность теплового движения,
беспорядок в системе и ее энтропия.
Кристаллизация жидкости приводит к
образованию
правильной кристаллической решетки и
дальнейшему увеличению порядка и
уменьшению энтропии. Подобная зависимость
в изменении температуры, энтропии и
порядка позволяет
предположить, что при нуле абсолютной
температуры
тепловое движение полностью прекратится
Eк
= 3kT/2
=
О и
в системе установится максимальный
порядок, то есть неупорядоченность
и энтропия станут равными нулю. Это
предположение, не поддающееся опытной
проверке, ибо абсолютный
нуль температуры недостижим из-за
необратимости реальных процессов
охлаждения, называют тепловой теоремой
Нернста
или третьим законом термодинамики —
при абсолютном
нуле: максимум порядка, отсутствие
беспорядка, энтропия
равна нулю —
![]() s
= 0.
s
= 0.
8. Энтропия — мера недостатка информации. Это так называемая информационная энтропия. Природные и техногенные
![]() nW
= 0, а термодинамическая
вероятность W
= 1. В этом случае данное
макросостояние системы быть реализовано
только одним микросостоянием, так каждая
молекула, имея скорость, равную нулю,
занимает определенное
положение. Это состояние системы является
предельным и соответствует
кристаллическому состоянию химически
однородного тела, при котором количество
информации .0 системе
максимально. Это значит, что более
организованные системы
способны дать о себе большую информацию,
чем менее организованные.
Таким образом, информацию относят к
исследуемой системе, считая
ее функцией состояния системы, которая
не имеет отношения к интеллекту, памяти
человека. Изложенное наводит
на мысль о связи информации с вероятностью
состояния системы, а следовательно, и
с энтропией. В данном
случае энтропия равна нулю, а информация
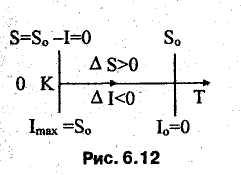
максимальна (рис. 6.12).
nW
= 0, а термодинамическая
вероятность W
= 1. В этом случае данное
макросостояние системы быть реализовано
только одним микросостоянием, так каждая
молекула, имея скорость, равную нулю,
занимает определенное
положение. Это состояние системы является
предельным и соответствует
кристаллическому состоянию химически
однородного тела, при котором количество
информации .0 системе
максимально. Это значит, что более
организованные системы
способны дать о себе большую информацию,
чем менее организованные.
Таким образом, информацию относят к
исследуемой системе, считая
ее функцией состояния системы, которая
не имеет отношения к интеллекту, памяти
человека. Изложенное наводит
на мысль о связи информации с вероятностью
состояния системы, а следовательно, и
с энтропией. В данном
случае энтропия равна нулю, а информация
максимальна (рис. 6.12).
- Рассмотрим противоположную ситуацию: идеальный газ находится при высокой температуре. Положение хаотично движущихся молекул в этих условиях совершенно неопределенно, и о них нельзя получить никакой информации, кроме той, что .они движутся, то есть в этом случае информация близка к нулю, а энтропия — к максимуму (рис. 6.12). Следовательно, информация о микроеостоянии тем меньше, чем больше W, а значит, и энтропия S, Дж/К. Таким образом, энтропия оказывается величиной, изменяющейся противоположно информации I
![]()
где К — постоянная, по физическому содержанию отличная от постоянной Больцмана.
Итак, информация эквивалентна отрицательному изменению энтропии. А. Бриллюэн назвал отрицательную энтропию негэнтропией. И отсюда появляется еще одна характеристика энтропии, как меры неопределенности сообщения.
Относительно изменения этих двух величин предыдущее можно сформулировать следующим образом. Изменение энтропии системы противоположно изменению информации о ней. Информация — мера трудности познания макросостояния системы. Это значит, что из-за незнания микросостояния системы надо затратить много энергии, или, точнее, негэнтропии для возвращения системы в более упорядоченное состояние.
Интересно следующее замечание по данному свойству энтропии. В процессах развития наблюдаются две тенденции: стремление к усложнению организации системы и одновременно — к упрощению. Первая тенденция равносильна накоплению информации, а тенденция к упрощению означает умень-шение информации и накопление энтропии. Ведущей все-таки является тенденция усложнения.
Кстати, энтропийная основа информации была ясна до создания в 1949 г. теории информации.
9. Энтропия — мера жизненного потенциала. Возможность применимости второго закона термодинамики, к биологическим объектам интересует ученых с давних пор. Все живые, как, впрочем, и неживые объекты мира метастабильны. Мета-стабильность обусловлена, прежде всего, тем, что упомянутые объекты имеют определенную форму. Живым существам приходится активно бороться за ее сохранение и даже усложнение. Потеря формы означает смерть. Деятельность поддержания формы у неживых объектов устанавливается степенью активности их энергетического взаимодействия с окружающей средой. Форма, например, алмаза поддерживается неизменной на протяжении миллионов лет. У работающего алмаза продолжительность существования формы значительно меньше. Здесь уместно вспомнить, что термодинамика описывает любые явления, связанные с энергетическими процессами, которые невозможны в бесструктурных системах (системах без формы). Итак, второй закон, как смертный приговор, неукоснительно исполняется в неживой природе.
В 1935 г. Э. Бауэр сформулировал три основные особенности живых систем: самопроизвольное изменение состояния, противодействие внешним силам, постоянная работа против уравновешивания с окружающей средой. Третья особенность является отличительным признаком биологических систем. Она имеет очевидный термодинамический смысл.
Э. Шредингер также считал особенностью биологических объектов их неуравновешенность с окружающей средой, которая поддерживается непрерывным обменом открытой живой системы с окружающей средой, пищей, питьем, дыханием и т. д. Пища и остальные формы обмена представляют собой материал, необходимый для создания нового в системе. Конструирование же нового и выход на иной уровень упорядоченности системы создается, однако, не пищей, а развивающимся организмом.
Основное свойство всего живого состоит в том, что в момент перехода к состоянию равновесия оно поворачивает процесс в обратном направлении, и при этом живая система не просто восстанавливает свою структуру (энтропия системы понижается), но я делается более совершенной. Следовательно, неравновесное состояние биологических объектов поддерживается за счет извлечения ими из окружающей среды отрицательной энтропии — негэнтропии. Это равнозначно сбросу «наработанной» положительной энтропии. Ведь чем выше энтропия, тем больше беспорядок в системе — дряблость кожи, нарушение координации движений, потеря памяти и многое другое. Таким образом, жизнь в энтропийном отображении напоминает возвратно-поступательное движение вдоль энтропийной оси по схеме, вначале до достижения физиологической зрелости: шаг вперед, два шага назад (негэнтропийная тенденция эволюции биологических систем), а затем: два шага вперед, шаг назад (энтропийная тенденция). Получается, что жизнь — это, прежде всего, постоянная и затухающая реакция организма, вызванная изменениями условий окружающей среды и направленная только на возврат к исходному состоянию, то есть на поддержание внутренней среды организма. Другими словами, живую природу от неживой отличает обязательная обратимость физиологических процессов одновременно с естественной и обязательной для неживых систем необратимостью, обусловленной эволюционной морфологией биологического объекта. Именно эволюция объекта, и в том числе живого, приводит к возрастающему образованию структурной энтропии. Кстати, затормозить, сдержать рост энтропии можно уменьшением количества потребляемой пищи и увеличением двигательной активности биологического объекта. Поэтому старение начинается с момента, когда возникает смена негэн-тропийных тенденций на энтропийные. С этого момента организм постепенно утрачивает способность к восстановлению и усложнению своей структуры, вследствие снижения естественной физической активности, когда процессы синтеза перестают быть избыточными. Следует заметить, что окончательно не постигнута тайна, как организм без какого-либо вмешательства извне вначале в течение какого-то периода времени сам творит себя и лишь начиная с определенного времени сам же себя и разрушает. Но еще более загадочной является проблема: жизнь — это случайное или закономерное явление природы.
10. Энтропия — индикатор невозможности обратить течение времени. Природные процессы, как показывает человеческий опыт, являются необратимыми и идут в направлении накопления энтропии. Природой предусмотрен определенный - порядок чередования событий, по которому она, по крайней о мере, в пределах отдельных макрочастей стремится к равновесию. Однако порядок чередования событий в некоторых случаях нельзя смешивать с направлением событий (направление ем времени). Например, точки на прямой линии могут быть расположены в определенном порядке, но направление здесь отсутствует, так как сама линия не обладает каким-либо направлением. В необратимых же процессах приходится иметь в виду и порядок чередования событий, и направление времени в сторону его накопления. Постоянный во времени процесс роста энтропии психологически воспринимается как естественное направление времени. Порядок необратимых процессов во времени находится также во взаимосвязи с причинно-следственным механизмом. В нашем понимании причина и следствие идут во времени так, что сперва действует причина, а уж за нею появляется следствие. Конечно же, отношения между событиями сложнее, но очевидно, что второй закон термодинамики затрагивает глубокие философские вопросы.
Итак, последовательность событий, обусловленная законом возрастания энтропии, и привычная направленность времени приводят к очевидным выводам: время движется от прошлого к будущему; момент «теперь» есть настоящее время, отделяющее прошлое от будущего. Настоящее — это миг в сравнение с бесконечным прошлым и будущим; прошлое никогда не возвращается; нельзя изменись прошлое, но можно изменить будущее; можно иметь летописи прошлого, но не будущего.
