
Калин Физическое материаловедение Том 6 Част 2 2008
.pdfнение состава. Зависимость состава равновесного пара над UO2+х от отношения O/U при 2185 К показана на рис. 24.142.
В зависимости от отношения O/U изменяется как общее давление пара, так и относительное содержание в паре его компонентов. В достехиометрической области основной вклад в равновесное давление вносят молекулы UO и UO2, а в застехиометрической – молекулы UO3 и UO2. Над диоксидом урана, конгруэнтно испаряющегося состава, пар состоит в основном из молекул UO2.
Давление пара урана резко уменьшается, а кислорода – увеличивается при переходе из достехиометрической области в застехиометрическую. Общее равновесное давление пара является минимальным для конгруэнтно испаряющегося диоксида урана. В зависимости от температуры оно описывается уравнением:
lgp (Па) = 11,1741 – |
3,7195 104 |
|
3,5162 106 |
|
2,6178 109 |
. (24.18) |
|||
T |
T |
2 |
T |
3 |
|||||
|
|
|
|
||||||
В области температур 1600 – 2200 К эта зависимость почти линейна, а при более высоких температурах наблюдается отклонение от линейности, вызванное, очевидно, появлением в паре значительных количеств молекул U2O4.
Для жидкого UO2 до температуры 5000 К имеет место следующее соотношение:
lgp (МПа) = 28,650 – 34930/Т – 5,64·lgТ. (24.19)
Вычисленная по (24.19) температура кипения UO2 равна 3660 К, причем теплота испарения при этой температуре составляет
497± 28 кДж/моль.
Вравновесном паре над PuO2-х обнаружены следующие компоненты: O, O2, Pu, PuO и PuO2 (рис. 24.143). Парциальное давление PuO2, которое вносит основной вклад в общее давление, слабо растет с увеличением отношения O/Pu. Парциальное давление PuO уменьшается с ростом O/Pu; при O/Pu < 1,80 оно выше давления
PuO2, а при O/Pu > 1,80 – меньше. Давление чисто кислородных компонентов пара O и O2 вблизи стехиометрического состава существенно превосходит давление других компонентов.
Температурная зависимость равновесного давления пара над
PuO2 описывается зависимостью, подобной (24.18), однако давление пара над PuO2 приблизительно на четыре порядка выше, чем над UO2. В паре, находящемся в равновесии с (U,Pu)О2±x, установ-
241

лено присутствие девяти компонентов: O, O2, U, UO, UO2, UO3, Pu, PuO и PuО2. Состав пара и его давление зависят от отношений О/М, Pu/U и температуры. Давление металлосодержащих компонентов пара в до- и застехиометрической областях составов при 2000К, полученное расчетным путем, показано на рис. 24.144. Основным компонентом пара над застехиометрическим топливом является
UО3, а не, хотя UО2 преобладает в паре над UО2,000. Причина этого заключается в значительно большем парциальном давлении кисло-
рода над застехиометрическим топливом по сравнению со стехиометрическим.
|
Рис. 24.144. Равновесное давление ме- |
Рис. 24.143. Зависимость состава |
таллосодержащих компонентов пара |
равновесного пара над PuO2-х |
над смешанным оксидом |
от отношения O/Pu |
(U0,85Pu0,15)O2±х при температуре 2000 К |
Отношение U/Pu в равновесной паровой фазе над застехиометрическими оксидами выше, чем в твердой фазе. Длительное испарение обогащает твердую фазу плутонием. В случае достехиометрических оксидов, наоборот, паровая фаза обогащена плутонием по сравнению с твердой. При О/М = 1,96 соотношение тяжелых металлов в паровой и твердой фазах одинаково, т.е. испарение оксида такого состава носит конгруэнтный характер. Конгруэнтно испаряющийся состав топлива определяется главным образом отноше-
242
нием О/М; зависимость его от отношения Pu/U и температуры значительно слабее. Паровая фаза обычно содержит больше кислорода на атом тяжелого металла, чем твердая оксидная фаза, вследствие чего в результате испарения смешанные оксиды становятся более достехиометрическими.
Важной особенностью процесса испарения смешанного оксидного топлива является то обстоятельство, что его неконгруэнтный характер приводит к образованию на поверхности оксидов тонкого поверхностного слоя толщиной от 0,1 до 10 мкм, концентрации металлических компонентов в котором могут заметно отличаться от их средних значений по объему образца. Наличие такого слоя может оказывать заметное влияние на измеряемые величины коэффициентов диффузии, скорости испарения, поверхностной энергии и других физико-химических свойств оксидов, а также на скорость миграции пор и перераспределение компонентов оксидов в неоднородном температурном поле по механизму испарениеконденсация.
Теплофизические свойства топливных оксидов
Температура плавления. Величина температуры плавления является важной характеристикой ядерного топлива, так как она определяет допустимую мощность твэла. Температура плавления смешанных оксидов урана и плутония плавно понижается от температуры плавления UО2 (2847 ± 30 ºС) до температуры плавления PuО2 (2428 ± 35 ºC) по мере повышения в них концентрации оксида плутония (рис. 24.145).
Отклонение от стехиометрического состава в области доили застехиометрии, а также выгорание снижают температуру плавления смешанных оксидов. Последнее обстоятельство обусловлено физико-химическим взаимодействием матрицы топлива, как с продуктами деления, так и с оксидом америция Am2O3, температура плавления которого составляет 2197 ± 15 ºC.
Принято считать, что при выгорании 100 ГВт сут/т температура плавления МОХ-топлива снижается приблизительно на 100 ºC. Экспериментальные результаты по определению температуры плавления облученного МОХ-топлива показаны на рис. 24.146.
243

Рис. 24.145. Температура плавления смешанных уран-плутониевых оксидов
Рис. 24.146. Влияние выгорания на температуру плавления смешанного оксидного топлива
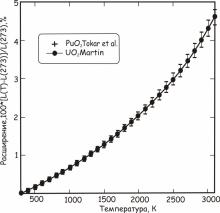
Термическое расширение. Коэффициенты термического расширения топлива и оболочки определяют величину зазора между ними при выходе твэла на мощность. Коэффициенты термического расширения UO2, PuO2 и МОХ-топлива имеют близкие значения (рис. 24.147) и могут быть с хорошей точностью описаны следующими выражениями:
L(T) |
2,66 10 3 9,802 10 6 Т |
|
L(273) |
||
(24.20) |
2,705 10 10 Т 2 4,391 10 13 Т 3;
244
L(T) L(273) (9,9734 10 1 9,802 10 6 Т |
(24.21) |
||
2,705 10 10 Т2 4,391 10 13 Т3), |
|||
|
|||
ср 9,828 10 6 6,39 10 10 |
Т |
(24.22) |
|
1,33 10 12 Т2 1,757 10 17 |
, |
||
Т3 |
|
||
для температурного интервала от 273 до 923 К, а для более высоких температур, вплоть до температуры плавления:
|
L(T) |
3,28 10 3 1,179 10 5 Т |
|
||
|
|
(24.23) |
|||
|
L(273) |
|
|
||
|
2,429 10 9 Т2 |
1,219 10 12 Т3, |
|
||
L(T) L(273) (9,9672 10 1 1,179 10 5 Т |
(24.24) |
||||
|
2,429 10 9 Т2 1,219 10 12 Т3), |
||||
|
|
||||
|
ср 1,1833 10 5 |
5,013 |
10 9 Т |
(24.25) |
|
|
3,756 10 12 Т2 |
6,125 |
10 17 Т3. |
||
|
|
||||
Рис. 24.147. Термическое расширение диоксида урана и диоксида плутония
Отклонение от стехиометрии в сторону застехиометрии повышает коэффициенты термического расширения оксидного топлива, а в сторону достехиометрии – понижает. Влияние нестехиометрии может быть учтено с помощью следующего множителя
245

[1+(3,9±0,9)·x], где х – отклонение от стехиометрии. Для смешанных уран-плутониевых оксидов термическое расширение при температуре Т определяется как средняя величина из соответствующих значений для UО2 и PuО2, пропорциональная их массовым долям. Увеличение концентрации плутония в МОХ-топливе приводит к снижению коэффициента термического расширения при низких температурах и повышению его при высоких (рис. 24.148).
Рис. 24.148. Термическое расширение смеси оксидов UO2 и PuO2 в зависимости от содержания PuO2.
Экспериментальные значения коэффициента термического расширения для таблеток состава 75 % UО2 – 25 % PuО2 приведены в табл. 24.22.
Таблица 24.22
Коэффициент термического расширения таблетки 75 % UО2 – 25 % PuО2
Температурный интервал, ºC |
20 – 300 |
20 – 600 |
20 – 800 |
20 – 1000 |
, 10-6 град.-1 |
8,2 |
9,9 |
10,5 |
11,4 |
Теплоемкость. Удельная теплоемкость топлива Ср имеет важное значение для оценки поведения реактора в переходных режимах; кроме того, она связана с теплопроводностью топлива1. Теплоемкость оксидного топлива можно представить в виде суммы различных составляющих, которые обусловлены фононами, даю-
1 Физическое материаловедение. Т. 1. – М.: МИФИ, 2007. П. 3.7.2.
246
щими основной вклад в теплоемкость, ангармоническим смещением анионов, термическим расширением, дефектами Шотки и электронными дефектами.
Выражение, описывающее зависимость теплоемкости UO2 от температуры включает в себя три слагаемых, которые имеют физическое обоснование. Первое учитывает вклад фононов, второе – вклад теплового расширения, а третье – электронный вклад. Это выражение может быть записано в следующем виде и справедливо в интервале температуры от 300 до 3120 К:
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
exp Т |
|
|
|
|
C E |
a |
|
|
E |
a |
|
||
C |
p |
(T) C |
|
|
|
|
|
|
2 C |
2 |
T |
3 |
|
exp |
|
|
, (24.26) |
||
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
1 |
|
|
|
|
|
2 |
|
|
T |
2 |
|
|
|
T |
||||
|
|
|
T2 |
|
|
|
|
|
|
||||||||||
|
|
|
exp |
|
1 |
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
Т |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
где |
С1 = 302,27 |
Дж·кг-1·К-1; |
С2 = 8,463·10-3 |
Дж·кг-1·К-2; С3 = |
|||||||||||||||
= 8,741·107 Дж·кг-1; Θ = 548,68 К; Ea = 18531,7 К. |
|
|
|
|
|||||||||||||||
|
Теплоемкость диоксида плутония описывается тем же выраже- |
||||||||||||||||||
нием, но константы в этом случае будут следующими: С1 = 322,49
Дж·кг-1·К-1; С2 = 1,4679·10-2 Дж·кг-1·К-2; С3 = 0 Дж·кг-1; Θ = 587,41 К; Ea = 18531,7 К.
Теплоемкость смешанного уран-плутониевого оксидного топлива (МОХ-топлива (UyPu1-y)O2) может быть рассчитана исходя из
закона аддитивности (Коппа – Ноеманна):
Cp (T,(U1 yPuy )O2) (1 y) Cp (T,UO2) y Cp (T,PuO2) , (24.27)
где Ср(Т,UO2) – теплоемкость UO2 при температуре Т, а Ср(Т, PuO2)
– теплоемкость PuO2 при этой же температуре.
Температурные зависимости теплоемкости UО2 и PuО2 изображены на рис. 24.149 и 24.150, из которых видно, что значения теплоемкости этих двух оксидов имеют близкие значения во всем интервале температуры вплоть до температуры плавления. Выше ~1800 К происходит аномальный рост теплоемкости, и ее величина оказывается приблизительно в 2 раза больше значения, даваемого законом Дюлонга–Пти. Этот рост обусловлен электронными дефектами, количество которых значительно возрастает по мере приближения к температуре плавления.
247
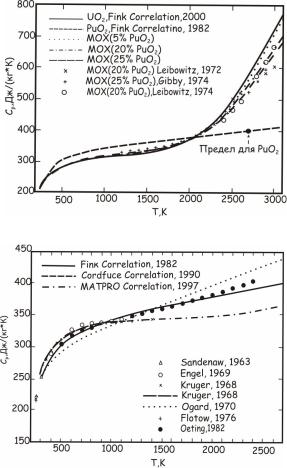
Рис. 24.149. Температурная зависимость теплоемкости диоксида урана
Рис. 24.150. Температурная зависимость теплоемкости диоксида плутония
Теплоемкость топливных оксидов растет не только с увеличением температуры, но и с отклонением от стехиометрии, что обусловлено, по-видимому, повышением концентрации дефектов кристаллической решетки. Влияние отклонения от стехиометрии (x) на теплоемкость UO2+x изучено не так широко. В графической форме экспериментальные температурные зависимости теплоемкости для интервала температуры 373÷1673 К и различных значений х представлены на рис. 24.151.
248

Рис. 24.151. Экспериментальные значения теплоемкости UO2+x.
Из представленного рисунка видно, что с ростом отклонения от стехиометрии значения теплоемкости UO2+x слегка увеличиваются. Кроме того, на экспериментальных зависимостях теплоемкости UO2,035 и UO2,084, в интервале температуры 673÷873 К наблюдаются пики, которые по видимому, связаны с растворением фазы U4O9 в
UO2+x.
Теплоемкость легированного диоксида урана так же как и теплоемкость МОХ-топлива можно рассчитать по закону аддитивно-
сти (24.27).
Данные по влиянию выгорания на теплоемкость диоксида урана в литературе крайне ограничены. Оценка влияния выгорания на теплоемкость диоксида урана по данным, полученным на модель-
ном ядерном топливе (МЯТ).
МЯТ содержит твердые имитаторы продуктов деления (ИПД), концентрация которых соответствует заданному уровню выгорания, но не содержит газообразные и легколетучие ПД. Было показано, что с увеличением концентрации ИПД (что эквивалентно увеличению выгорания) теплоемкость диоксида урана слегка повышается. Отмечается, что измеренные значения теплоемкости МЯТ хорошо совпадают с результатами, рассчитанными по закону аддитивности. На основании полученных данных было предложено выражение для расчета теплоемкости UO2 с учетом влияния выго-
249

рания. Это выражение основано на уравнении (24.26), в котором для учета влияния выгорания эмпирический коэффициент С2 заменен на C2 :
C2 C2 (1 0,011 b) , |
(24.28) |
где С2 – эмпирический коэффициент, равный 2,43·10-2 Дж·кг-1·К-2, а b – величина выгорания топлива в ат. %. Влияние выгорания для образцов МЯТ стехиометрического состава с имитацией выгорания 0,3 и 8 ат. %, представлено на рис. 24.152.
Рис. 24.152. Температурные зависимости теплоемкости UO2 с имитацией выгорания 0, 3 и 8 ат.%
Таким образом, выгорание приводит к незначительному повышению теплоемкости диоксида урана.
Теплопроводность. Радиальное распределение температуры в топливном сердечнике, а так же максимальная температура в центре твэла определяется теплопроводностью λ, которая зависит от температуры, пористости, стехиометрического состава, размера зерен, характера и количества примесей и т.д. оксидного топлива.
Теплопроводность1 оксидного топлива можно рассматривать, по крайней мере, как сумму трех составляющих: фононной или решеточной проводимости λф, фотонной или радиационной λр и электронной (включая амбиполярную – вызванную совместным пере-
1 Физическое материаловедение. Т. 1. – М.: МИФИ, 2007. П. 3.7.3.
250
